Willkommen bei der Zeitschrift für Infektionstherapie!
INFEKTIO aktuell
Aktuelle Informationen zur Infektionstherapie
++ Up to date bleiben: Newsletter-Anmeldung ++
Ab Januar 2025 – Die neue App für Ihr Digital-Abo
Alle neuen Ausgabe der Zeitschrift für Infektionstherapie finden Sie ab 2025 nur noch auf der neuen digitalen Abo-Plattform – als App oder im Browser!
Die Vorteile:
- Responsives Design
- Tag- und Nacht-Lesemodus
- Vorlesefunktion
- SPECIAL: Fragen Sie den Wissens-Chat, das integrierte KI-Tool, nach Suchbegriffen und fachlichen Antworten!
Hier geht's...
Fragen? Schauen Sie in unsere FAQ-Liste.
Trends bei der Langzeit-Antibiotikaverordnung nach gezielten ambulanten Antibiotic-Stewardship-Maßnahmen
Bis zu 90 % des Antibiotikaverbrauchs entfallen auf den ambulanten Bereich, wobei schätzungsweise die Hälfte aller Verordnungen suboptimal oder unnötig ist. Übermäßig lange Therapiedauern finden
sich je nach Syndrom in 40–85 % der Verordnungen und tragen maßgeblich zur Entwicklung von Antibiotikaresistenzen bei. Die Mayo Clinic implementierte im Januar 2020 ein ambulantes
Antibiotic-Stewardship-Programm (ASP), das sich auf Primärversorgung und Akutversorgung (Urgent Care) konzentrierte und jährlich syndromspezifische Verbesserungsziele verfolgte – etwa die Reduktion
unnötiger Antibiotikaverordnungen bei viralen oberen Atemwegsinfektionen (URI) und die Optimierung der Verordnungspraxis bei Harnwegsinfektionen (UTI). Eine retrospektive, multizentrische
Kohortenstudie untersuchte nun, ob diese fokussierten Maßnahmen auch mit breiteren Reduktionen von Langzeit-Antibiotikaverordnungen (LDAP; definiert als > 7 Tage) korrespondierten.
Insgesamt wurden 675.526 Antibiotikaverordnungen aus 642.579 Patientenkontakten im Zeitraum November 2020 bis Juni 2025 eingeschlossen; 42,2 % wiesen eine Verordnungsdauer > 7 Tage auf.
ASP-Einrichtungen machten 83,0 % aller Kontakte aus. ASP-Verordnungspanels wurden in 10,5 % aller Kontakte genutzt, wobei 99,2 % der Nutzung auf ASP-Einrichtungen entfielen. Bei Panel-Nutzung lag die
LDAP-Rate bei 30,1 % gegenüber 44,2 % ohne.
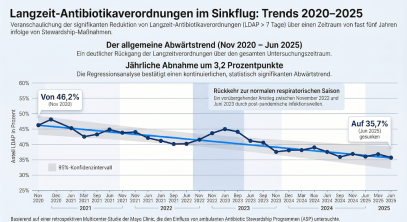
Abbildung 1 zeigt den Gesamttrend der LDAP über den Studienzeitraum von November 2020 bis Juni 2025, dargestellt als monatlicher Anteil aller ambulanten Kontakte mit einer Antibiotikaverordnung >
7 Tage. Der Anteil sank von 46,2 % im November 2020 auf 35,7 % im Juni 2025, was einer absoluten Differenz von −10,5 Prozentpunkten (pp) bzw. einer relativen Reduktion von 22,7 % entspricht. Die
lineare Regressionslinie modelliert eine geschätzte jährliche Abnahme von −3,2 pp. Auffällig ist ein vorübergehender Anstieg der LDAP von etwa November 2022 bis Juni 2023, der mit der Rückkehr zu
einer „normalen“ respiratorischen Virussaison in den USA nach der COVID-19-Pandemie korrespondiert.
Abbildung 1: Gesamtanteil ambulanter Kontakte mit Antibiotikaverordnungen > 7 Tage über die Zeit (November 2020 – Juni 2025). Die blaue Trendlinie modelliert die geschätzte jährliche Abnahme von −3,2 Prozentpunkten; der grau schattierte Bereich zeigt das zugehörige 95-%-Konfidenzintervall.
Eigene Darstellung basierend auf Daten aus: [1], erstellt mit NotebookLM
Die Subgruppenanalysen zeigten, dass sowohl ASP- als auch Nicht-ASP-Einrichtungen signifikante Rückgänge der LDAP über den Studienzeitraum verzeichneten, wobei die Verbesserungen in
ASP-Einrichtungen deutlich ausgeprägter waren. Die LDAP in ASP-Einrichtungen sank von 46,8 % auf 34,8 % (Differenz −12 pp), während Nicht-ASP-Einrichtungen einen Rückgang von 45,5 % auf 39,1 %
verzeichneten (Differenz −6,4 pp). In der linearen Regression zeigten Nicht-ASP-Einrichtungen eine signifikante jährliche Abnahme von 2,4 pp (95-%-Konfidenzintervall [KI] 1,8 bis 2,9; P < 0,001).
Für ASP-Einrichtungen betrug die jährliche Abnahme 3,4 pp (95-%-KI 2,9 bis 3,9; P < 0,001) – 1,0 pp mehr als in Nicht-ASP-Einrichtungen (95-%-KI 0,26 bis 1,8; P = 0,009). Bei ausschließlicher
Betrachtung der Nicht-Prioritätsdiagnosen war die Abnahme in ASP-Einrichtungen mit 4,1 pp pro Jahr (95-%-KI 3,8 bis 4,5; P < 0,001) signifikant größer als in Nicht-ASP-Einrichtungen mit 2,7 pp
(95-%-KI 2,3 bis 3,0; P < 0,001), mit einer Differenz von 1,4 pp (95-%-KI 0,9 bis 1,9; P < 0,001). Innerhalb der ASP-Einrichtungen wiesen Nicht-Prioritätsdiagnosen eine jährliche Abnahme von
4,1 pp auf (95-%-KI 3,3 bis 4,9; P < 0,001), während Prioritätsdiagnosen eine Abnahme von 2,6 pp zeigten (95-%-KI 1,9 bis 3,4; P < 0,001), wobei die Differenz 1,5 pp betrug (95-%-KI 0,4 bis
2,6; P = 0,010). Innerhalb Nicht-ASP-Einrichtungen nahmen Nicht-Prioritätsdiagnosen um 2,7 pp pro Jahr ab (95-%-KI 2,0 bis 3,4; P < 0,001), während Prioritätsdiagnosen mit einer geschätzten
jährlichen Veränderung von −0,4 pp stabil blieben (95-%-KI −1,1 bis 0,3; P = 0,281). Die Differenz zwischen den beiden Gruppen betrug 2,3 pp (95-%-KI 1,3 bis 3,3; P < 0,001).
Bemerkenswert war, dass in ASP-Einrichtungen auch bei Nicht-Prioritätsdiagnosen – also Syndromen, die nie direkt vom ASP adressiert wurden – signifikante LDAP-Reduktionen auftraten. In
Nicht-ASP-Einrichtungen hingegen blieben Prioritätsdiagnosen hinsichtlich der LDAP stabil. Respiratorische Diagnosen außerhalb der URI-Prioritätsgruppe zeigten mit 7,4 pp pro Jahr (95-%-KI 6,6 bis
8,2; P < 0,001) die größte jährliche Abnahme.
Folgerung der Autoren
Die Befunde deuten auf vorteilhafte „Off-Target“-Effekte hin: Obwohl die Interventionen syndromspezifisch ausgerichtet waren, korrelierte die Präsenz des ASP in ASP-Einrichtungen mit Verbesserungen
der Verordnungspraxis auch bei nie adressierten Syndromen. Klinische Entscheidungsunterstützungsinstrumente wie Verordnungspanels mit standardisierten Therapiedauern ≤ 7 Tage trugen wahrscheinlich
wesentlich zur LDAP-Reduktion bei. Die LDAP erweist sich als praktikable Benchmark-Metrik für ambulante ASPs. Weitere Studien sind erforderlich, um diese Ergebnisse zu bestätigen.
Kommentar der Herausgeber
Die meisten Antibiotika werden im ambulanten Sektor verordnet. Diese Arbeit zeigt, dass auch hier mit ASP sehr viel erreicht und ein Kulturwandel bewirkt werden kann. Jetzt müssen wir nur noch
entsprechende Strukturen aufbauen und fördern.
[1] Ilges, D. et al. Trends in Long Duration Antibiotic Prescribing Following Focused Outpatient Antimicrobial Stewardship Efforts Across a Large Healthcare Enterprise. Clin Infect Dis. 2025; published online first April 09, 2026. doi: 10.1093/cid/ciag244
06.05.2026
Sterblichkeitstrends bei Patienten mit schwer behandelbaren, antibiotikaresistenten Gram-negativen Infektionen im Zeitalter neuer Antibiotika in den USA
Gram-negative Infektionen mit schwer behandelbarer Resistenz (Difficult-to-treat Resistance, DTR) sind definiert als Resistenz gegenüber sämtlichen First-Line-Antibiotika, d.h. allen β-Lactamen
einschließlich Carbapenemen sowie Fluorchinolonen, und weisen eine um 40 % höhere Sterblichkeit auf als empfindliche Infektionen. Historisch erforderten DTR-Infektionen den Einsatz von Antibiotika
wie Aminoglykosiden, Polymyxinen oder Tigecyclin, die mit suboptimalen Behandlungsergebnissen assoziiert sind. Seit 2014 wurden in den USA mehrere neue Antibiotika mit Aktivität gegen resistente
Gram-negative Erreger zugelassen, darunter Ceftazidim-Avibactam, Ceftolozan-Tazobactam, Meropenem-Vaborbactam, Imipenem-Relebactam, Cefiderocol und Eravacyclin. Ob diese Substanzen tatsächlich zu
verbesserten Überlebensraten bei Patienten mit DTR-Infektionen geführt haben, war bislang unklar.
Eine retrospektive Kohortenstudie untersuchte anhand der PINC-AI Healthcare Database, ob und warum sich die Sterblichkeit bei Patienten mit DTR-Gram-negativen Infektionen seit Einführung dieser
neueren Antibiotika verändert hat. Eingeschlossen wurden erwachsene stationäre Patienten (Alter ≥ 18 Jahre), die zwischen dem 1. Januar 2016 und dem 31. August 2023 entlassen wurden und bei denen ein
mikrobiologischer Nachweis einer DTR-Infektion durch Enterobacterales, Pseudomonas aeruginosa oder Acinetobacter baumannii vorlag, verbunden mit einer Antibiotikatherapie über
mindestens drei konsekutive Tage. Im Studienzeitraum wurden 8 319 398 stationäre Aufenthalte aus 471 Krankenhäusern erfasst, von denen 9384 (0,11 %) einen DTR-Erregernachweis aufwiesen. Davon
erfüllten 5065 (54,0 %) Aufenthalte aus 262 Krankenhäusern die Einschlusskriterien. Das mittlere Alter betrug 59,9 Jahre (Standardabweichung 16,2), 59,5 % waren männlich. Eine Sepsisdiagnose lag bei
64,8 % vor, 45,7 % erforderten eine Intensivaufnahme, 31,7 % eine maschinelle Beatmung und 24,8 % Vasopressoren. Die häufigsten Erreger waren P. aeruginosa (46,6 %), A. baumannii
(28,6 %) und Enterobacterales (24,8 %).
Die Verfügbarkeit neuerer Antibiotika nahm im Studienzeitraum deutlich zu: Der Anteil der Krankenhäuser mit Einsatz mindestens eines neueren Antibiotikums stieg von 12 % (23 von 198) im Zeitraum
2016–2018 auf 63 % (103 von 163) im Zeitraum 2021–2023; der Anteil mit Empfindlichkeitstestungen für neuere Antibiotika von 4 % (8 von 198) auf 71 % (116 von 163). Der Anteil der Patienten, die ein
neueres Antibiotikum als Initialtherapie erhielten, stieg von 4 % (21 von 589) im Jahr 2016 auf 15 % (34 von 234) im Jahr 2023. Dennoch erhielten in der Mehrzahl der Fälle (196 [84 %] von 234) die
Patienten auch 2023 weiterhin eine in-vitro-diskordante initiale Antibiotikatherapie. Insgesamt war bei 3775 von 4875 Aufenthalten (77,4 %) die Initialtherapie inadäquat. Von den 1100 Aufenthalten
mit adäquater Therapie wurde in 783 Fällen (71,2 %) dennoch ein traditionelles DTR-aktives Antibiotikum eingesetzt.
Die Krankenhaussterblichkeit wurde mittels eines generalisierten linearen gemischten Modells (GLMM) analysiert, adjustiert für patienten-, krankenhaus- und COVID-19-pandemiebezogene Faktoren. Über
den gesamten Zeitraum gemittelt betrug die geschätzte Sterblichkeitswahrscheinlichkeit 20 % (95-%-Konfidenzintervall [KI] 18 bis 23) für Enterobacterales, 20 % (95-%-KI 18 bis 22) für P.
aeruginosa und 25 % (95-%-KI 23 bis 28) für A. baumannii. Zwischen 2016 und 2023 wurde keine Veränderung des durchschnittlichen marginalen Effekts auf die adjustierte Sterblichkeit
beobachtet – weder für Enterobacterales (0,1 %; 95-%-KI −1,1 bis 1,4) noch für P. aeruginosa (−0,7 %; 95-%-KI −1,7 bis 0,3) oder A. baumannii (−0,4 %; 95-%-KI −1,8 bis 0,9).
Bei Stratifizierung nach Infektionsort zeigte sich einzig für DTR-P. aeruginosa-Blutstrominfektionen eine Abnahme der adjustierten Sterblichkeit (−4,5 % pro Jahr; 95-%-KI −8,2 bis −0,6),
während alle anderen Erreger-Infektionsort-Kombinationen unverändert blieben. Im GLMM war weder der Erhalt eines neueren Antibiotikums (adjustierte Odds Ratio [aOR] 1,11; 95-%-KI 0,89 bis 1,40) noch
eine in-vitro-diskordante vs. konkordante Initialtherapie (aOR 1,12; 95-%-KI 0,91 bis 1,38) mit einer veränderten Sterblichkeit assoziiert. Auch die Verfügbarkeit neuerer Antibiotika auf
Krankenhausebene zeigte keinen signifikanten Zusammenhang mit der Sterblichkeit.
Folgerung der Autoren
Trotz erheblich gestiegener Verfügbarkeit und Verordnung neuerer Antibiotika in US-amerikanischen Krankenhäusern zwischen 2016 und 2023 wurde bei der Mehrzahl der DTR-Gram-negativen Infektionen keine
Reduktion der Sterblichkeit beobachtet. Die initiale Antibiotikatherapie bleibt überwiegend diskordant; selbst bei konkordanter Therapie werden häufig suboptimale traditionelle DTR-aktive Substanzen
eingesetzt. Die konventionelle Empfindlichkeitstestung benötigt durchschnittlich 92,2 Stunden, was eine erhebliche Verzögerung der zielgerichteten Therapie bedeutet. Die Entwicklung und
Implementierung schneller diagnostischer Plattformen zur frühzeitigen Erkennung resistenter Phänotypen, klinische Studien mit stärkerer Repräsentation von DTR-Patienten sowie die Erforschung
nicht-antimikrobieller, wirtgerichteter Therapieansätze könnten entscheidende Schritte zur Senkung der Sterblichkeit bei resistenten Infektionen darstellen.
Kommentar der Herausgeber
Obwohl die neueren, deutlich teureren Antibiotika in Zulassungsstudien nahezu durchweg mit einem besseren Outcome assoziiert sind als ältere Substanzen, zeigen die enttäuschenden Ergebnisse aus der
Praxis – begründet in der offensichtlichen Bevorzugung billigerer alter Substanzen und der zu langsamen Diagnostik und des dadurch verzögerten Einsatzes – deutlich, dass der durch Studien belegte
Vorteil dieser neuen Mittel nur durch einen entsprechend gut gesteuerten Einsatz in einen klinischen Vorteil für die Patienten überführt werden kann.
Walker, M. K. et al. Survival trends in patients with difficult-to-treat, antibiotic-resistant, Gram-negative infections in the era of next-generation antibiotics in the USA: a retrospective cohort study. Lancet Infect Dis. 2026; published online first March 25, 2026. doi: 10.1016/S1473-3099(26)00020-4
06.05.2026
Neue S3-Leitlinie zur Tuberkuloseprävention bei neu zugewanderten Menschen in Deutschland
Tuberkulose ist in Deutschland mit einer Inzidenz von etwa
5 / 100.000 Einwohnerinnen und Einwohnern selten, doch rund 75 % der Betroffenen sind nicht in Deutschland geboren. Für 2022 wurden 4.076 Fälle gemeldet, 71 % der 116 Todesfälle betrafen Menschen mit nicht-deutscher Staatsangehörigkeit. Die Inzidenz für eine extrapulmonale Tuberkulose ist 64-fach höher bei ausländischer vs. deutscher Staatsangehörigkeit.
Das Deutsche Zentralkomitee zur Bekämpfung der Tuberkulose (DZK) hat unter Beteiligung von 16 Fachgesellschaften nun die erste deutsche S3-Leitlinie zur Tuberkuloseprävention bei neu zugewanderten Menschen vorgelegt (AWMF-Register 020-029, Version 1.0, September 2025).
Die Leitlinie umfasst 31 konsensbasierte Empfehlungen für das Screening auf Tuberkuloseinfektion (TBI), die präventive Therapie, das Screening auf aktive Tuberkulose, die Implementierungsvoraussetzungen sowie Kommunikationsstrategien.
Dabei verwendet sie ein dreistufiges Empfehlungsschema: „soll" (starke Empfehlung) bedeutet, dass Evidenz und Nutzen-Risiko-Abwägung klar sind; „sollte" (schwache Empfehlung) signalisiert eingeschränkte Evidenz, bei der individuelle Faktoren berücksichtigt werden sollten; „kann" (offene Empfehlung) wird bei unsicherer Evidenzlage ausgesprochen.
TBI-Screening – altersabhängig abgestuft:
- 15–35 Jahre, Herkunftsland-Inzidenz > 100 / 100.000, Einreise innerhalb der letzten 2 Jahre: soll angeboten werden (starker Konsens 100 %)
- 35–45 Jahre, gleiche Kriterien: sollte angeboten werden (Konsens 95 %)
- > 45 Jahre, Inzidenzschwellenwert > 150 / 100.000: kann nach individueller Nutzen-Risiko-Abwägung angeboten werden (Konsens 82 %)
- Komplexe Migrationsbedingungen (z.B. lange Fluchtrouten, Kriegs-/Krisenregionen): kann unabhängig von Alter und Inzidenz angeboten werden (starker Konsens 100 %)
Die abgeschwächte Empfehlung für über 45-Jährige begründet sich durch die ansteigende Rate toxisch bedingter Hepatitiden unter Isoniazid und das abnehmende Lebenszeitprogressionsrisiko.
Populationsbasierte Kohortenstudien zeigten eine Reduktion der Tuberkulose-Inzidenz durch Screening und präventive Therapie (HR 0,76; 95-%-Konfidenzintervall [KI] 0,63 bis 0,91). Das kumulative
2-Jahres-Progressionsrisiko ohne Therapie beträgt 4,1 % (95-%-KI 1,3 bis 12,0), wobei 81,6 % des 5-Jahres-Risikos in den ersten 2 Jahren auftreten.
Präventive Therapie – bevorzugte Regime:
- 4R (Rifampicin 4 Monate): gleiche Wirksamkeit wie 9H, höhere Abschlussraten (+157 / 1.000), weniger UAW Grad 3–5
- 3HR (Isoniazid + Rifampicin 3 Monate): Effektivität vs. Placebo OR 0,53 (95-%-KI 0,36 bis 0,78), weniger UAW vs. 6-9H, höhere Abschlussraten (+389 / 1.000)
- 6-9H nur bei Kontraindikation/Unverträglichkeit von Rifampicin
- Bei MDR-/RR-Tuberkulose-Rate > 10 % im Herkunftsland (v.a. postsowjetische Staaten): individuelle Abwägung mit spezialisiertem Zentrum
- Kontaktpersonen bei Fluorchinolon-empfindlichem MDR-/RR-Stamm: Levofloxacin 6 Monate (Risikoreduktion: Kinder 56 %, Erwachsene/Jugendliche 45 %)
Tuberkulose-Screening:
- Ab 15 Jahren, Herkunftsland-Inzidenz > 100 / 100.000, geplanter Aufenthalt > 3 Monate: TBI-Screening sollte zeitnah nach Einreise angeboten werden
- Bei zusätzlichen Risikofaktoren oder in Settings mit Ausbruchspotential oder in vulnerablen Gruppem: TBI-Screening soll angeboten werden bei Herkunftsland-Inzidenz > 100 / 100.000 oder MDR-/RR-Prävalenz > 10%
- Methode: Kombination Symptom-Screening + Thoraxröntgen
- Entdeckung > 84 % der prävalenten Fälle;
- Fallfindungsrate bei Asylsuchenden in Deutschland: 347 / 100.000, NNS: 288
Kinder und Jugendliche (< 15 Jahre):
- TBI-Screening bei Herkunft aus Ländern mit Inzidenz > 100 / 100.000 (TBI-Rate durchschnittlich 11,1 %; bei unbegleiteten minderjährigen Geflüchteten 18,0 %)
- Geflüchtete Kinder < 5 Jahre: immer Screening, auch ohne weitere Risikofaktoren
Implementierung:
- Screening nach Einreise, kostenfrei, freiwillig, unabhängig vom Aufenthaltsstatus
- Fallmanagement über die gesamte Versorgungskaskade
- Monitoring und Evaluation hinsichtlich Kosteneffektivität und epidemiologischem Impact
Kommunikationsstrategien:
- Schulung von Fachpersonal zu Tuberkulose, Versorgungskette sowie kultursensibler und diskriminierungsfreier Kommunikation
- Aufklärung zur Entkräftung kultureller Fehleinschätzungen und Vermittlung zentraler Botschaften (Tuberkulose ist heilbar; klare Trennung von Screening und Aufenthaltsrecht)
- Zielgruppenorientierte, sprach- und kultursensible Kommunikation unter Einbezug von Sprachmittlung oder Übersetzungshilfen
Die Leitliniengruppe betont, dass die erfolgreiche Umsetzung aller Empfehlungen eine kostendeckende Finanzierung sämtlicher Screeningkomponenten sowie eine bundesweite, systematische Evaluation der
Versorgungskaskade voraussetzt, um die Maßnahmen evidenzbasiert weiterzuentwickeln und langfristig zur Tuberkulose-Elimination in Deutschland beizutragen.
Häcker, B. et al. S3-Leitlinie Tuberkuloseprävention bei neu zugewanderten Menschen (TB-Risk); AWMF-Register Nr. 020-029. 2025; Version 1.0, September 2025. URL: https://register.awmf.org/de/leitlinien/detail/020-029
08.04.2026
Neue Surviving Sepsis Campaign 2026: Was Infektiologen und ABS-Experten wissen müssen
Die SSC-Leitlinie ist die weltweit meistzitierte und einflussreichste Leitlinie zum Management der Sepsis – getragen von der Society of Critical Care Medicine (SCCM) und der European Society of Intensive Care Medicine (ESICM), mit 69 Panelisten aus 23 Ländern. Die aktuelle Version 2026 umfasst 129 Empfehlungen und Statements und adressiert erstmals Themen wie prähospitale Antibiotikagabe, Betablocker-Einsatz und selektive Darmdekontamination.
Die SSC 2026 enthält einige neue Empfehlungen, die für Antibiotic Stewardship (ABS) und infektiologische Beratung unmittelbar relevant sind.
Anaerobier-wirksame Therapie
Bei Patienten ohne Risikofaktoren für anaerobe Infektionen – insbesondere bei pulmonalem oder urologischem Fokus – soll keine routinemäßige anaerobier-wirksame Therapie erfolgen (bedingte Empfehlung).
Selektive Darmdekontamination (SDD)
Erstmals empfiehlt die SSC 2026 SDD bei beatmeten Patienten – jedoch ausdrücklich nur in Einrichtungen mit niedriger MRE-Prävalenz (bedingte Empfehlung). Die S3-Leitlinie 2025 enthält hierzu keine Empfehlung. Für Deutschland ist die Indikation an lokalen Resistenzstatistiken zu orientieren.
Procalcitonin
PCT wird von der SSC 2026 zur Steuerung der Therapiedauer empfohlen (bedingte Empfehlung), zur Einleitung der Antibiotikatherapie hingegen nicht. Die S3-Leitlinie spricht zur Therapiedauer eine starke Empfehlung aus.
Fungale Biomarker
Sowohl Beta-D-Glucan als auch Mannan werden von der SSC 2026 nicht zur Einleitung oder Beendigung einer empirischen Antimykotikatherapie empfohlen. Die S3-Leitlinie nennt Beta-D-Glucan als einen von mehreren Risikofaktoren, ohne eine biomarkergesteuerte Strategie formal zu empfehlen.
Prescott, H. C. et al. Surviving Sepsis Campaign: international guidelines for management of sepsis and septic shock 2026. Intensive Care Med. 2026; published online first. doi: 10.1007/s00134-026-08361-1
08.04.2026
Zulassungsempfehlung für ersten Kombinationsimpfstoff gegen COVID-19 und Influenza
Nachdem erst kürzlich der neue mRNA-Impfstoff gegen COVID-19 mNEXSPIKE (Moderna) in Europa zugelassen wurde, könnte dieser bald auch in Kombination mit einem Grippeimpfstoff zur Verfügung stehen [1]. Der Ausschuss für Humanarzneimittel (CHMP) bei der europäischen Arzneimittelbehörde EMA empfiehlt nach seiner Sitzung am 26. Februar die Zulassungserteilung für mCOMBRIAX, den ersten kombinierten Impfstoff gegen COVID-19 und saisonale Influenza für Menschen ab 50 Jahren [2].
Die durch COVID-19 und Influenza verursachten Atemwegsinfektionen verlaufen in den meisten Fällen leicht bis mittelschwer, bei älteren Menschen und Personen mit geschwächtem Immunsystem können jedoch
schwere Verläufe auftreten, insbesondere bei einer Koinfektion mit Influenza und SARS-CoV-2 [3]. In Deutschland wurden seit Beginn der Saison 2025/2026 etwa 225.000 Influenza-Fälle (26 %
hospitalisiert) und 111.000 COVID-19-Fälle (36 % hospitalisiert) gemäß Infektionsschutzgesetz an das Robert Koch-Institut gemeldet [4]. Unter den ca. 1.500 bzw. 1.400 Todesfällen mit bestätigter
Influenza- bzw. SARS-CoV-2 Infektion waren 95 % bzw. 96 % 60 Jahre oder älter.
mCOMBRIAX (mRNA-1083) ist eine Kombination aus mNEXSPIKE (mRNA-1283), dem gegen SARS-CoV2-gerichteten mRNA-Impfstoff der zweiten Generation, und mRNA-1010, dem gegen die Influenza-Viren A/H1N1,
A/H3N2 und B/Victoria gerichteten Grippeimpfstoff [2,5].
mCOMBRIAX enthält pro Einzeldosis insgesamt 40 µg mRNA, verkapselt in Lipid-Nanopartikeln [5]. Im Gegensatz zu allen vorherigen mRNA-basierten Impfstoffen gegen COVID-19 codiert die in mNEXSPIKE
enthaltenen mRNA nicht für das volle Spike-Protein, sondern nur für die membrangebundene N-terminale Domäne und die rezeptorbindende Domäne [2, 5]. Die in mRNA-1010 enthaltenen mRNA-Sequenzen
codieren hingegen für die vollständigen membrangebundenen Hämagglutinin-Glykoproteine der saisonalen Influenzaviren [2,5].
Die Zulassungsempfehlung basiert auf den Ergebnissen einer randomisierten, beobachterverblindeten, aktiv kontrollierten Phase-III-Studie an 8015 Personen ab 50 Jahren, die die Immunogenität und
Sicherheit des neuen Kombinationsimpfstoffs untersuchte [5]. Alle Personen erhielten 1:1 randomisiert entweder eine intramuskuläre Injektion mit mCOMBRIAX (+ gleichzeitige Injektion mit
Placebo) oder eine Injektion mit dem COVID-19-Impfstoff Spikevax (mRNA-1273), gleichzeitig verabreicht mit einem zugelassenen quadrivalenten saisonalen Grippeimpfstoff. Personen im Alter von 50-64
Jahren wurden mit FLUARIX (Standarddosis) geimpft, in der Altersgruppe ≥ 65 Jahre wurde hingegen Efluelda (Hochdosis) eingesetzt. Zur Beurteilung der Immunogenität wurden 28 Tage nach der Impfung die
Antikörpertiter mittels Hämagglutinationshemmtest bzw. Pseudovirus-Neutralisationstest sowie die Serokonversion von Anti-Hämagglutinin-Antikörpern und Seroresponse von neutralisierenden Antikörpern
bestimmt. Für mCOMBRIAX konnte gegenüber allen enthaltenen Virusstämmen eine Nichtunterlegenheit der durch die Impfung ausgelösten Immunantworten im Vergleich zur Applikation der jeweiligen
Einzelimpfstoffe gezeigt werden. Darüber hinaus war die durch mCOMBRIAX ausgelöste Immunantwort gegen SARS-CoV-2 (alle Altersgruppen) und alle vier (bei 50-64-Jährigen) bzw. drei (bei ≥ 65-Jährigen)
Influenzastämme stärker als nach der einzelnen Applikation der Impfstoffe. Der einzige Stamm, für den bei Erwachsenen ab 65 Jahren keine statistisch signifikant höhere Immunantwort beobachtet werden
konnte, war B/Yamagata, der entsprechend aktuellen Empfehlungen nicht mehr in saisonalen Grippeimpfstoffen enthalten ist.
Die Impfung mit mCOMBRIAX zeigte ein akzeptables Sicherheits- und Verträglichkeitsprofil. Im Vergleich zur Applikation der Einzelimpfstoffe waren Häufigkeit und Schwere der berichteten Nebenwirkungen
in beiden Alterskohorten zwar numerisch höher (≥ 65 Jahre: 83,5 % und 78,1 %; 50–64 Jahre: 85,2 % und 81,8 %), die meisten waren jedoch von Schweregrad 1 und 2 und von kurzer Dauer [5]. Die
häufigsten Nebenwirkungen von mCOMBRIAX sind Schmerzen an der Injektionsstelle, Müdigkeit, Muskelschmerzen, Gelenkschmerzen, Kopfschmerzen, Schüttelfrost, geschwollene Lymphknoten, Übelkeit und
Erbrechen sowie Fieber [3].
Als erster kombinierter COVID-19/Influenza-Impfstoff bietet mCOMBRIAX Personen ab 50 Jahren die Möglichkeit, sich mit einer einzigen jährlichen Impfung gegen beide Krankheiten zu schützen, wofür
derzeit zwei Injektionen mit Einzelimpfstoffen nötig sind. Für die Zulassungserteilung in Europa ist noch die Zustimmung der Europäischen Kommission ausstehend. Die zum Zeitpunkt der klinischen
Studien untersuchte Impfstoffzusammensetzung (Omicron XBB.1.5, A/H1N1, A/H3N2, B/Victoria, B/Yamagata) basierte auf den Empfehlungen der Weltgesundheitsorganisation für die Saison 2023/2024. Analog
anderen COVID-19- und Grippeimpfstoffen wird auch bei mCOMBRIAX eine jährliche Anpassung an die zirkulierenden Virusstämme erwartet [3].
1 Moderna, Inc. Moderna Receives European Commission Marketing Authorization for COVID-19 Vaccine mNEXSPIKE. Published online Feb 17, 2026. URL: https://feeds.issuerdirect.com/news-release.html?newsid=8201845178897387&symbol=MRNA
2 European Medicines Agency (EMA). mCOMBRIAX – summary of opinion. EMADOC-1829012207-43023. Published online Feb 26, 2026. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-mcombriax_en.pdf
3 European Medicines Agency (EMA). First combined COVID-19 and influenza vaccine for people 50 years and older. Published online Feb 27, 2026. URL: https://www.ema.europa.eu/en/news/first-combined-covid-19-influenza-vaccine-people-50-years-older
4 Robert Koch-Institut (RKI). ARE-Wochenbericht KW 9/2026. doi: 10.25646/13921. URL: https://edoc.rki.de/bitstream/handle/176904/13486/ARE-Wochenbericht_KW09_2026.pdf?sequence=1&isAllowed=y
5 Rudman Spergel, A.K. et al. Immunogenicity and Safety of Influenza and COVID-19 Multicomponent Vaccine in Adults ≥50 Years: A Randomized Clinical Trial. JAMA 2025; 333(22):1977-1987. doi: 10.1001/jama.2025.5646
11.03.2026
Antibiotikatherapie schwerer Infektionen mit multiresistenten Bakterien – Neue S3-Leitlinie
Die Deutsche Gesellschaft für Hygiene und Mikrobiologie (DGHM) hat gemeinsam der Paul-Ehrlich-Gesellschaft für Infektionstherapie, der Deutschen Gesellschaft für Infektiologie und der Österreichischen Gesellschaft für Infektiologie und Tropenmedizin sowie weiteren Fachgesellschaften eine neue S3-Leitlinie zur Antibiotikatherapie schwerer Infektionen mit multiresistenten Bakterien entwickelt. Die Leitlinie gibt evidenzbasierte Empfehlungen für die Behandlung dieser zunehmend herausfordernden Infektionen.
Diagnostik als Grundlage
Ein zentraler Aspekt der Leitlinie ist die Betonung einer qualifizierten mikrobiologischen Diagnostik. Bei der erstmaligen Charakterisierung eines Isolats mit Verdacht auf Multiresistenz während
eines stationären Aufenthaltes soll der Einsatz von jeweils zwei Verfahren zur Erregeridentifizierung und zur Bestimmung der den MRE-Status bestimmenden Resistenzen erfolgen (Empfehlung 2.1.1). Bei
schweren MRE-Infektionen sollten Labororganisation und Verfahren so gestaltet werden, dass die Zeitdauer von der Gewinnung des Untersuchungsmaterials bis zur vorläufigen Befundmitteilung möglichst
kurzgehalten wird (Empfehlung 2.1.2). Bei Verdacht auf eine schwere MRE-Infektion kann eine mikrobiologische Schnelldiagnostik direkt aus dem Untersuchungsmaterial wie Blut oder Liquor mit
Nukleinsäure-basierten Testmethoden erwogen werden (Empfehlung 2.1.3).
Von besonderer Bedeutung bei multiresistenten Gram-negativen Bakterien ist die Produktion von Carbapenemasen. Bei schweren MRE-Infektionen durch Gram-negative Bakterien soll eine Bestimmung des
Resistenzmechanismus, mindestens aber ein Nachweis oder Ausschluss von Metallo-β-Lactamasen (MBL) und gegebenenfalls der nachgewiesenen Carbapenemasen, erfolgen (Empfehlung 2.1.4).
Therapeutische Empfehlungen
Die Leitlinie gibt differenzierte Empfehlungen für die wichtigsten multiresistenten Erreger:
| Erreger | Erste Wahl | Alternative/Besonderheiten |
| CRE (Carbapenem-resistente Enterobacterales) | Ceftazidim-Avibactam, Meropenem-Vaborbactam oder Imipenem-Relebactam (sofern keine MBL) |
Bei Resistenz oder MBL-Nachweis: Cefiderocol oder Aztreonam-Avibactam. |
| DTR-P. aeruginosa (Difficult-to-Treat Resistance) |
Ceftolozan-Tazobactam (bevorzugt unter ABS-Aspekten) |
Ceftazidim-Avibactam, Imipenem-Relebactam, Cefiderocol (bei MBL vorbehalten).
|
| CRAB (Carbapenem-resistente A. baumannii) | Cefiderocol | Sulbactam-Durlobactam in Kombination mit Carbapenem (keine EU-Zulassung). Alternativen: Sulbactam kombiniert mit Levofloxacin, Tigecyclin oder Colistin |
| MRSA-Blutstrominfektion | Daptomycin oder Vancomycin i.v. (Auswahl nach Infektionsfokus und Nephrotoxizitätsrisiko) | Bei Kontraindikation: Teicoplanin, Linezolid oder Ceftobiprol |
| MRSA-Endokarditis | Daptomycin oder Vancomycin i.v. | Bei Kunstklappen: zusätzlich Fosfomycin oder Rifampicin |
| MRSA-Pneumonie | Linezolid oder Vancomycin i.v. | Auswahl nach Toxizitätsrisiko und Co-Medikation |
| MRSA-Haut-/Weichgewebe | Linezolid oder Daptomycin | Tedizolid, Ceftarolin, Ceftobiprol, Delafloxacin oder Vancomycin/Teicoplanin plus Rifampicin/Fosfomycin. Sequenz: Dalbavancin oder Oritavancin |
| VRE-BSI (Vancomycin-resistente Enterokokken) | Linezolid i.v. oder Daptomycin (10 bis 12 mg/kg/Tag) |
Daptomycin nicht bei MHK > 2 mg/l. Tigecyclin/Eravacyclin nicht bei BSI. |
Die Definition der DTR bei P. aeruginosa wurde 2021 von Tamma et al. eingeführt und beschreibt eine gleichzeitige Nichtempfindlichkeit gegenüber allen klinisch relevanten antipseudomonalen Erstlinienantibiotika. Im Unterschied zu den früheren Klassifikationen MDR, XDR und PDR bildet die DTR-Kategorie therapieentscheidende Resistenzmuster praxisnäher ab.
Zur evidenzbasierten Weiterentwicklung der Therapie von Infektionen durch multiresistente Erreger sind prospektive, randomisierte Studien mit klar definierten mikrobiologischen Einschlusskriterien
dringend erforderlich. Besonderes Augenmerk sollte auf die vergleichende Wirksamkeit neuer Substanzen, den Stellenwert von Kombinationstherapien, die optimale Dosierung mit therapeutischem Drug
Monitoring sowie den Einsatz molekularer Diagnostik gelegt werden. Da Erreger und ihre Resistenzen ständigen Veränderungen unterliegen, kann die Leitlinie nur den Stand bis zu ihrem Erscheinen
abbilden.
11.03.2026
Welttuberkulosetag 2026: Ja! Wir können TB beenden!
Die WHO hat den Welttuberkulosetag 2026 unter das Motto „Yes! We can End TB! Led by countries. Powered by people.“ (zu deutsch: „Ja! Wir können TB besiegen! Angeführt von Ländern. Angetrieben von Menschen.“) gestellt. Der am 24. März begangene Aktionstag unterstreicht die zentrale Bedeutung nationaler Strategien und zivilgesellschaftlichen Engagements im Kampf gegen Tuberkulose.
Tuberkulose bleibt eine der führenden infektiösen Todesursachen weltweit. Mit der End-TB-Strategie verfolgt die WHO das Ziel, die Tuberkulose-Epidemie bis 2030 zu beenden – dies bedeutet eine Reduktion der Tuberkulose-bedingten Sterblichkeit um 90 % und der Inzidenz um 80 % im Vergleich zu 2015.
Die Kampagne betont die essenzielle Rolle der einzelnen Länder bei der Implementierung evidenzbasierter Tuberkuloseprogramme sowie die unverzichtbare Bedeutung betroffener Menschen und Gemeinschaften
als treibende Kräfte für Veränderung. Besondere Aufmerksamkeit gilt vulnerablen Populationen mit erhöhtem Tuberkuloserisiko, einschließlich Menschen mit HIV-Koinfektion, Diabetes mellitus und
Unterernährung.
Zur Unterstützung stellt die WHO verschiedene Ressourcen bereit: Der Global TB Report 2025 liefert umfassende epidemiologische Daten, die WHO Academy bietet spezialisierte Kurse für medizinisches
Personal, und am 18. März findet eine Online-Talkshow statt. Die Entwicklung neuer diagnostischer Verfahren, therapeutischer Optionen und die Bekämpfung multiresistenter Tuberkulose bleiben
wissenschaftliche Prioritäten.
>> Mehr Informationen zum Report 2025, zu den Kursen und zur Online-Talkshow
11.03.2026
Leitlinien zur präoperativen Dekolonisierung und Prophylaxe bei multiresistenten Gram-positiven Erregern
Die Europäische Gesellschaft für Klinische Mikrobiologie und Infektionskrankheiten (ESCMID) hat Leitlinien zur präoperativen Dekolonisierung und gezielten Antibiotikaprophylaxe bei erwachsenen Patienten mit multiresistenten Gram-positiven Bakterien (MDR-GPB) vor Operationen veröffentlicht. Die Empfehlungen basieren auf einer systematischen Literaturübersicht und wurden nach dem GRADE-System bewertet.
Für MRSA-Träger ergaben sich folgende Hauptempfehlungen:
- Ein Screening auf S. aureus vor elektiven Herz- und orthopädischen Operationen wird als gute klinische Praxis empfohlen (unbewertet).
- Eine Dekolonisierung mit Mupirocin ± Chlorhexidin wird vor Herz- und orthopädischen Operationen stark empfohlen (moderate Evidenz), für andere Operationen bedingt empfohlen (niedrige Evidenz).
- Eine gezielte perioperative Prophylaxe wird vor Herz-, orthopädischen und neurochirurgischen Eingriffen bedingt empfohlen (niedrige Evidenz).
- Kombinierte Interventionen (Dekolonisierung plus gezielte Prophylaxe) werden vor Herz- und orthopädischen Operationen bedingt empfohlen (sehr niedrige Evidenz).
Für VRE, Methicillin-resistente koagulase-negative Staphylokokken und pan-resistente Gram-positive Bakterien konnten aufgrund unzureichender Evidenz keine Empfehlungen gegeben werden.
| Intervention | Art der OP | Empfehlungsstärke | Evidenzgrad |
| Screening auf S. aureus | Herz-/orthopädische OP | Gute klinische Praxis | unbewertet |
| Dekolonisierung mit Mupirocin ± Chlorhexidin | Herz-/orthopädische OP | Stark | moderat |
| Dekolonisierung mit Mupirocin ± Chlorhexidin | andere OPs | Bedingt | niedrig |
| Gezielte Prophylaxe | Herz-/orthopädische/Neuro-OP | Bedingt | niedrig |
| Kombinierte Interventionen | Herz-/orthopädische OP | Bedingt | sehr niedrig |
Die Autoren betonen, dass die Umsetzung der Empfehlungen an die lokale Epidemiologie und verfügbare Ressourcen angepasst werden sollte. Wichtige Forschungslücken bestehen insbesondere bei:
- Entwicklung von Mupirocin-Resistenzen
- Alternativen Dekolonisierungsstrategien
- Optimaler Teicoplanin-Dosierung
- Interventionen zur VRE-Prävention bei Hochrisikopatienten
Die Leitlinien unterstreichen die Bedeutung eines multidisziplinären Ansatzes zur Infektionsprävention, der neben spezifischen Interventionen bei MDR-GPB-Trägern auch allgemeine Maßnahmen wie
Personalschulung, optimale OP-Techniken und Antibiotic Stewardship umfasst.
Folgerung der Autoren
Die Reduktion postoperativer Infektionen erfordert einen umfassenden Ansatz mit Schulung aller Beteiligten, bewährten chirurgischen Praktiken und einem sorgfältigen Antibiotikamanagement. Die Empfehlungen müssen im Kontext lokaler Gegebenheiten und unter Berücksichtigung möglicher Resistenzentwicklungen umgesetzt werden.
11.02.2026
ESCMID/EUCIC-Leitlinien zur perioperativen Antibiotikaprophylaxe bei MDR-GNB-kolonisierten Patienten
Die Europäische Gesellschaft für Klinische Mikrobiologie und Infektionskrankheiten (ESCMID) und das Europäische Komitee für Infektionsprävention und -kontrolle haben Leitlinien zur perioperativen Antibiotikaprophylaxe (PAP) bei Patienten veröffentlicht, die vor einer Operation mit multiresistenten Gram-negativen Bakterien (MDR-GNB) kolonisiert sind. Die evidenzbasierten Empfehlungen basieren auf einer systematischen Überprüfung von Studien von Januar 2010 bis April 2022.
Die Leitlinien adressieren das Screening auf MDR-GNB vor Operationen, die Anpassung der PAP bei kolonisierten Patienten und die optimale Dauer der PAP. Die Qualität der Evidenz und die Stärke der Empfehlungen wurden nach dem GRADE-Ansatz bewertet.
Wichtige Empfehlungen:
| PAP-Empfehlung MDR-GNB | Screening-Empfehlung | PAP-Empfehlung |
| ESCR-E | Rektales Screening vor kolorektalen OPs und Lebertransplantationen (bedingt, niedrige Evidenz) | Gezielte PAP empfohlen (bedingt, niedrige bis sehr niedrige Evidenz) |
| CRE | Rektales Screening vor Lebertransplantationen (bedingt, niedrige Evidenz) | Keine Empfehlung aufgrund unzureichender Evidenz |
| CRAB | Rektales Screening vor Lebertransplantationen (bedingt, niedrige Evidenz) | Keine Empfehlung aufgrund unzureichender Evidenz |
| FQR-E | Rektales Screening vor TRUSPB (bedingt, moderate Evidenz) | Gezielte PAP empfohlen (bedingt, moderate Evidenz) |
Allgemeine Empfehlungen:
- Screening innerhalb von 3 Wochen vor der Operation (Good Practice)
- PAP-Beendigung innerhalb von 24 Stunden nach OP (stark, moderate Evidenz)
- Bei Transplantationen (außer Niere) PAP-Verlängerung auf 48-72 Stunden möglich (Good Practice)
Die Leitlinien betonen die Notwendigkeit einer sorgfältigen Abwägung zwischen Unter- und Überdiagnose von MDR-GNB-Kolonisationen. Die Implementierung von Screening-Verfahren sollte die lokale
Epidemiologie, mikrobiologische Kapazitäten und verfügbare Ressourcen berücksichtigen.
Folgerung der Autoren
Erhebliche Wissenslücken wurden identifiziert. Gut durchgeführte randomisierte kontrollierte Studien sind dringend erforderlich, insbesondere für CRE- und CRAB-Träger bei Hochrisiko-Operationen.
Zukünftige Studien sollten die Wirksamkeit gezielter PAP und die postoperative MDR-GNB-Kolonisation untersuchen. Ein umfassender Ansatz zur Reduzierung von Wundinfektionen, der sowohl
Antibiotika-basierte Interventionen als auch bewährte chirurgische Praktiken einschließt, wird empfohlen.
11.02.2026
Kommentar der Herausgeber zu beiden Beiträgen
Diese Leitlinien wurden lange erwartet. Die zunehmende Resistenzentwicklung und die wachsende Zahl von Patienten mit multiresistenten Erregern machen deutlich, dass pauschale perioperative
Antibiotikastrategien an ihre Grenzen gestoßen sind. Die neuen Empfehlungen der European Society of Clinical Microbiology and Infectious Diseases (ESCMID) schließen hier eine wichtige Lücke, indem
sie das Problem gezielt aus der Perspektive multiresistenter Erreger adressieren.
Auch in Deutschland zeichnet sich ein Paradigmenwechsel ab: Die aktuelle S3-Leitlinie der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften empfiehlt zunehmend eine individualisierte perioperative Antibiotikaprophylaxe. Die ESCMID-Leitlinien gehen jedoch einen entscheidenden Schritt weiter, indem sie differenziert nach MDR-GNB- und MDR-GPB-Kolonisationen, Operationsart und Evidenzlage vorgehen und damit die klinische Realität in Hochrisikokollektiven besser abbilden.
Gleichzeitig legen die Leitlinien schonungslos die bestehenden Defizite offen. Insbesondere fehlt weiterhin ein tragfähiges Konzept zur Sanierung der intestinalen Kolonisation mit VRE und
multiresistenten gramnegativen Erregern. Für diese Patienten bleibt die perioperative Strategie ein Balanceakt zwischen Infektionsprävention und Vermeidung weiterer Resistenzselektion.
Unser Fazit: Die ESCMID-Leitlinien setzen einen überfälligen, wichtigen Akzent. Sie stärken die individualisierte Entscheidungsfindung, ohne falsche Sicherheit zu suggerieren – und unterstreichen
zugleich den dringenden Bedarf an gezielter klinischer Forschung, gerade dort, wo wir bislang keine wirksamen Sanierungsstrategien haben.
11.02.2026
INFEKTIO_Podcast | Neues aus den Leitlinien – Globale Leitlinie zu Diagnose und Management der Candidiasis
Der Podcast consilium infectiorum bietet medizinischem Fachpersonal praxisrelevante Themen der klinischen Infektiologie und unterstützt dabei, evidenzbasierte Behandlungsoptionen für Patienten
auszuwählen.
In jeder Folge diskutiert Infektiologe Prof. Mathias Pletz aus Jena mit einem Expertengast einen klinischen Schwerpunkt – fundiert und dennoch in entspannter Gesprächsatmosphäre.
Besonders praktisch: Für jede Folge können Sie bis zu einem Jahr nach Veröffentlichung CME-Punkte sammeln, indem Sie die zugehörigen CME-Fragen beantworten.
In der aktuelle Folge ist Prof. Oliver Cornely aus Köln zu Gast. Gemeinsam widmen sie sich der globalen Leitlinie zur Diagnose und Management der Candidiasis.
11.02.2026
GeoSentinel-Analyse der Antibiotikaresistenzmuster bei Reisedurchfall
Reisedurchfall ist eine häufige Erkrankung bei internationalen Reisenden, die je nach Reiseziel, Dauer und Jahreszeit 20 % bis 88 % der Reisenden betrifft. In einer aktuellen Querschnittsstudie des GeoSentinel-Netzwerks wurden die Antibiotikaresistenzmuster von vier häufigen Durchfallerregern bei 859 internationalen Reisenden mit akutem Durchfall untersucht, die zwischen April 2015 und Dezember 2022 an 58 Standorten erfasst wurden. Das mediane Alter der Patienten betrug 30 Jahre, 51 % waren männlich. Die häufigsten Reiseregionen waren Subsahara-Afrika (25 %), Südostasien (24 %) und Südamerika (17 %).
Die Analyse der Resistenzmuster zeigte folgende Ergebnisse:
- Campylobacter-Isolate
- Hohe Fluorchinolonen-Resistenz: 75 %
- Höchste Resistenzraten bei Reisenden nach Südzentralasien (88 %) und Südostasien (80 %)
- Makrolid-Resistenz: 12 %
- Höchste Makrolid-Resistenzraten in Südzentralasien (24 %) und Südostasien (11 %)
- Non-Typhus Salmonellen (NTS)-Isolate
- Fluorchinolonen-Resistenz: 32 %
- Höchste Fluorchinolon-Resistenzraten in der Karibik (62 %) und Südzentralasien (45 %)
- Makroliden-Resistenz: 16 %
- Resistenz gegen Cephalosporine der dritten Generation: 5 %
- Shigella-Isolate
- Fluorchinolonen-Resistenz: 22 %
- Auffällig hohe Fluorchinolon-Resistenz von 79 % bei Fällen aus Südzentralasien
- Makroliden-Resistenz: 35 %
- Resistenz gegenüber Cephalosporinen der dritten Generation: 8 %
- Hohe Makrolid-Resistenz von 78 % bei Fällen aus Südamerika
- Diarrhöische E. coli-Stämme
- Fluorchinolon-Resistenz: 18 %
- Resistenz gegenüber Cephalosporinen der dritten Generation: 13 %
- Die meisten E. coli-Isolate stammten von einem einzelnen Standort in Peru
Die Studie zeigt deutliche regionale Unterschiede in den Resistenzmustern. Aufgrund der hohen Fluorchinolon-Resistenz bei Campylobacter und Shigella in Süd- und Südostasien erscheint die Empfehlung
von Makroliden als First-Line-Therapie für diese Regionen gerechtfertigt. In Südamerika, wo eine hohe Makrolid-Resistenz bei Shigella auftrat, kann eine breitere antibiotische Abdeckung erforderlich
sein. In Subsahara-Afrika, wo Campylobacter-Infektionen häufig waren, sind Makrolide aufgrund der 60%igen Fluorchinolon-Resistenz ebenfalls zu bevorzugen.
Folgerung der Autoren
Die Ergebnisse unterstreichen die Bedeutung einer kontinuierlichen Überwachung der Antibiotikaresistenz bei Durchfallerregern durch kulturelle Anzucht und Resistenztestung. Dies ist besonders wichtig angesichts der zunehmenden Verwendung kulturunabhängiger Diagnostikmethoden, die keine Resistenzdaten liefern. Eine sorgfältige Antibiotika-Stewardship und eine gezielte empirische Therapie basierend auf regionalen Resistenzmustern sind entscheidend, um die Entwicklung und Ausbreitung von Antibiotikaresistenzen einzudämmen.
Kommentar der Herausgeber
Die Daten belegen, dass bei Reiserückkehrern aus entsprechenden Risikoregionen (insbesondere Südostasien aber teils auch Lateinamerika) bei Diarrhö oftmals resistente Erreger zugrunde liegen können und eine antibiotische Therapie schwierig ist. Wichtig: In der Regel sind Antibiotika bei Reisediarrhö nicht erforderlich – meist reicht eine orale Rehydrierung aus. Eine Reisediarrhö sollte nur behandelt werden, wenn sie schwer ist, bei blutigen Stühlen, Anzeichen einer systemischen Infektion (Fieber) oder bei immunsupprimierten Patienten.
Amatya, B. et al. GeoSentinel Analysis of Traverls‘ Diarrhea Antimicrobial Restistance Patterns. JAMA Netw Open. 2025; 8(12):e2551089. doi: 10.1001/jamanetworkopen.2025.51089
14.01.2026
Der „One Health“-Zoonose-Bericht 2024 der Europäischen Union
Die Europäische Behörde für Lebensmittelsicherheit (EFSA) und das Europäische Zentrum für die Prävention und die Kontrolle von Krankheiten (ECDC) haben ihren jährlichen „One Health“-Zoonose-Bericht 2024 veröffentlicht. Er fasst die Ergebnisse der Überwachungsaktivitäten zu Zoonosen und zoonotischen Erregern bei Menschen, Tieren, Lebensmitteln und Futtermitteln zusammen, die in den EU-Mitgliedstaaten, dem Vereinigten Königreich (Nordirland) sowie weiteren Ländern erhoben wurden.
Der Bericht beschreibt mehrere zentrale Zoonosen, die in der folgenden Tabelle in abnehmender Häufigkeit dargestellt sind und sich hinsichtlich Krankheitslast und klinischer Bedeutung deutlich unterscheiden.
| Zoonose | Bestätigte Fälle | Melderate pro 100.000 Einwohner | Besonderheiten |
| Campylobacteriose
|
168.396 | 55,3 | Häufigste gemeldete Zoonose; Hauptquelle Geflügelfleisch |
| Salmonellose | 79.703 | 18,6 | Zweithäufigste Zoonose; häufige Ursache lebensmittelbedingter Ausbrüche, v. a. Eier |
| Shiga-Toxin-produzierende Escherichia coli (STEC)-Infektionen | 11.738 | 3,5 | Relevante Ursache schwerer gastrointestinaler Erkrankungen |
| Listeriose Schwerwiegendste Zoonose mit höchstem Anteil an Krankenhausaufenthalten (97,3 %) und 301 Todesfällen | 3.041 | 0,69 | Schwerwiegendste Zoonose; höchste Hospitalisierungs- (97,3 %) und Sterblichkeitsrate (15,6 %) |
Für alle vier Zoonosen wurde in den vergangenen fünf Jahren ein signifikanter Anstieg der gemeldeten Fallzahlen beobachtet.
Auch die Zahl lebensmittelbedingter Ausbrüche nahm 2024 weiter zu: Im Jahr 2024 wurden insgesamt 6.558 Ausbrüche gemeldet, die zu 62.481 Krankheitsfällen, 3.336 Krankenhausaufenthalten und 53 Todesfällen führten. Salmonella war der am häufigsten identifizierte Erreger bei Ausbrüchen mit bekanntem Verursacher (1.238 Ausbrüche) und verursachte die meisten Krankenhauseinweisungen (1.823) sowie zusammen mit Listeria monocytogenes die meisten Todesfälle (jeweils 17). Noroviren und andere Caliciviren waren für die höchste Zahl an Krankheitsfällen verantwortlich (14.297). Die Kombination von Salmonella in „Eiern und Eiprodukten“ wurde als besonders problematisch identifiziert und verursachte die meisten Ausbrüche mit starker Evidenz (83 Ausbrüche).
Im Bereich der Tiergesundheit erfüllten 14 Mitgliedstaaten sowie das Vereinigte Königreich die Zielvorgaben zur Reduzierung der Salmonella-Prävalenz in Geflügelpopulationen. Mehrere Staaten verfehlten jedoch weiterhin die Vorgaben in einzelnen Geflügelkategorien. Auffällig waren zudem deutliche Unterschiede zwischen amtlichen Kontrollen und Eigenkontrollen der Lebensmittelunternehmer: Behördlich entnommene Proben wiesen bei Campylobacter und Salmonella deutlich höhere Überschreitungs- bzw. Prävalenzraten auf als Eigenkontrollen.
Der Bericht enthält zudem aktuelle Daten zu Brucellose, Echinokokkose, Trichinellose, Tuberkulose durch Mycobacterium bovis und Tollwut sowie zu anderen zoonotischen Bakterien, Viren und Parasiten in Lebensmitteln und bei Tieren.
>> Hier geht es zum gesamten Bericht
14.01.2026
INFEKTIO_Podcast | Ersatzteilprobleme – Fremdkörperassoziierten Infektionen
Der Podcast consilium infectiorum bietet medizinischem Fachpersonal praxisrelevante Themen der klinischen Infektiologie und unterstützt dabei, evidenzbasierte Behandlungsoptionen für Patienten
auszuwählen.
In jeder Folge diskutiert Infektiologe Prof. Mathias Pletz aus Jena mit einem Expertengast einen klinischen Schwerpunkt – fundiert und dennoch in entspannter Gesprächsatmosphäre.
Besonders praktisch: Für jede Folge können Sie bis zu einem Jahr nach Veröffentlichung CME-Punkte sammeln, indem Sie die zugehörigen CME-Fragen beantworten.
In der aktuelle Folge ist Prof. Andrej Trampuz aus Brisbane (Australien) zu Gast. Gemeinsam widmen sie sich dem Thema fremdkörperassoziierte Infektionen.
14.01.2026
β-Lactam-Allergie-Label und ihre klinischen Auswirkungen
β-Lactam-Antibiotika gehören zu den am häufigsten eingesetzten Antibiotikaklassen, allerdings werden bei 10–15 % der erwachsenen Bevölkerung weltweit β-Lactam-Allergie-Label (BAL) dokumentiert. Diese Label sind jedoch überwiegend nicht verifiziert – bei mehr als 95 % handelt es sich nicht um echte IgE-vermittelte Allergien mit Anaphylaxie und über 90 % der als allergisch gekennzeichneten Patienten vertragen β-Lactame.
Eine aktuelle systematische Übersicht und Meta-Analyse untersuchte die Assoziation zwischen BAL und klinischen Outcomes. Die Analyse basierte auf einer systematischen Literaturrecherche in PubMed, der Cochrane Central Register of Controlled Trials (CENTRAL) und Embase für den Zeitraum Januar 2000 bis November 2024. Eingeschlossen wurden 63 Beobachtungs- und Interventionsstudien, die klinische Outcomes bei Patienten mit und ohne BAL verglichen.
Von den eingeschlossenen Studien stammten 60 (95 %) aus Ländern mit hohem Einkommen, 41 (65 %) aus Amerika, 15 (24 %) aus Europa und 7 (11 %) aus der westpazifischen Region. Die Stichprobengrößen variierten zwischen 86 und 36.856.032 Patienten. 52 Studien (82 %) wurden im stationären Setting durchgeführt und 59 (94 %) untersuchten erwachsene Patienten.
Die Meta-Analyse zeigte signifikante Assoziationen zwischen BAL und verschiedenen negativen klinischen Outcomes:
- Ein um 60 % erhöhtes Risiko für postoperative Wundinfektionen (Odds Ratio [OR] 1,60; 95-%-Konfidenzintervall [KI] 1,27–2,01)
- Ein um 42 % erhöhtes Risiko für Infektionen oder Kolonisation mit multiresistenten Erregern (OR 1,42; 95-%-KI 1,22–1,64)
- Ein um 26 % erhöhtes Risiko für Clostridioides-difficile-Infektionen (OR 1,26; 95-%-KI 1,16–1,37)
Während kein signifikanter Zusammenhang mit der Gesamtmortalität, der Krankenhaussterblichkeit oder der 30-Tage-Sterblichkeit gefunden wurde, zeigte sich bei der Mortalität nach ≥ 180 Tagen ein um
38 % erhöhtes Risiko (OR 1,38; 95-%-KI 1,04–1,85). Die Krankenhausverweildauer war bei Patienten mit BAL statistisch signifikant länger (standardisierte mittlere Differenz 0,06 Tage; 95-%-KI
0,05–0,08) bei jedoch fraglich klinischer Relevanz.
Folgerung der Autoren
Die vorliegende Meta-Analyse zeigt, dass BAL mit einer Reihe von negativen Gesundheitsoutcomes assoziiert sind, insbesondere mit postoperativen Wundinfektionen sowie Infektionen oder Kolonisation
mit multiresistenten Erregern und C. difficile. Obwohl BAL auch statistisch mit längeren Krankenhausaufenthalten assoziiert waren, war der beobachtete Unterschied minimal. Die Heterogenität
und methodischen Limitationen der eingeschlossenen Studien könnten die Generalisierbarkeit und Robustheit einiger Schlussfolgerungen einschränken. Die Ergebnisse unterstreichen jedoch die
Notwendigkeit, Public-Health-Initiativen zur Reduktion inakkurater Allergie-Label zu entwickeln und zu evaluieren, um die unnötige Vermeidung von First-Line-β-Lactam-Antibiotika zu reduzieren.
Kommentar der Herausgeber
Einmal mehr unterstreicht eine große Studie, wie wichtig es in der klinischen Praxis ist, bei allen Patienten eine vermeintliche Antibiotikaallergie zu überprüfen. Wenngleich die vorliegende Arbeit
nur Assoziationen und keine Kausalität etablieren konnte, so sind dennoch die Resultate plausibel und die verschiedenen negativen Auswirkungen erheblich. Hier besteht noch ein enormes
Verbesserungspotential.
Fu, M. et al. The burden of β-lactam allergy labels in health care: a systematic review and meta-analysis. Lancet Infect Dis. 2025; 25(8):896-908. doi: 10.1016/S1473-3099(25)00019-2
17.12.2025
Zulassungsempfehlung für monovalenten Pertussis-Impfstoff
Der Ausschuss für Humanarzneimittel (CHMP) bei der europäischen Arzneimittelbehörde EMA gab nach seiner Sitzung am 13. November 2025 eine positive Stellungnahme für die Zulassung von VacPertagen ab, einem neuen Impfstoff zum Schutz vor Pertussis (Keuchhusten) [1].
Pertussis ist eine hochkontagiöse bakterielle Atemwegserkrankung, die durch Bordetella pertussis verursacht wird. Es besteht keine lebenslange Immunität; sowohl nach natürlicher Infektion als auch nach Impfung nimmt der Schutz innerhalb weniger Jahre deutlich ab, was zu häufigen Reinfektionen im Erwachsenenalter führt [2,3]. In Deutschland liegt das mittlere Alter der gemeldeten Patienten bei etwa 40 Jahren [4,5]. Bei Erwachsenen verläuft die Erkrankung meist mild mit wochenlangem, hartnäckigem Husten, während Säuglinge besonders gefährdet sind und oft einen klassischen Verlauf in drei Stadien zeigen (katarrhalisch, paroxysmal, konvaleszent) [2,6,7]. Die größte Gefahr besteht darin, dass Erwachsene als Hauptreservoir die Infektion auf ungeimpfte Säuglinge übertragen, bei denen schwere Komplikationen und Todesfälle auftreten können [3,7]. Seit März 2013 besteht in Deutschland eine bundesweite Meldepflicht für Pertussis; zuvor war die Meldepflicht auf die östlichen Bundesländer beschränkt [8]. Auch in Österreich ist die Erkrankung meldepflichtig, in der Schweiz hingegen nicht. Im Jahr 2024 wurde dem Robert Koch-Institut die bislang höchste jährliche Fallzahl seit Einführung der Meldepflicht gemeldet, nach einem pandemiebedingten Rückgang in den Vorjahren [9]. Die Infektionsschutzmaßnahmen während der COVID-19-Pandemie führten zu einem deutlichen Rückgang der Pertussis-Fälle, der nach Aufhebung der Maßnahmen wieder anstieg [9].
Zur Prävention werden in Deutschland, Österreich und Schweiz die Impfung von Schwangeren zur passiven Immunisierung des Neugeborenen sowie die Grundimmunisierung im Säuglings- und Kleinkindalter, gefolgt von regelmäßigen Auffrischimpfungen im Kinder-, Jugend- und Erwachsenenalter empfohlen. Die Diagnostik erfolgt bevorzugt mittels PCR [6]. Die konsequente Umsetzung dieser Maßnahmen ist entscheidend, um schwere Verläufe und Todesfälle bei Säuglingen zu verhindern.
Der neue Impfstoff VacPertagen soll als Suspension zur Injektion in einer Fertigspritze erhältlich sein und ist vorgesehen für die Auffrischimpfung gegen Pertussis bei Personen ab 12 Jahren und zum passiven Schutz gegen Pertussis im frühen Säuglingsalter nach mütterlicher Immunisierung während der Schwangerschaft [1]. VacPertagen enthält zwei gereinigte Pertussis-Antigene: rekombinantes Pertussis-Toxin (PTgen) und filamentöses Hämagglutinin (FHA). Nach intramuskulärer Applikation induziert VacPertagen eine Verstärkung der PT- und FHA-spezifischen Antikörperreaktionen. Maternale Antikörper werden auf Säuglinge übertragen, wenn eine Impfung im zweiten oder dritten Schwangerschaftstrimester erfolgt ist.
VacPertagen wurden in drei klinischen Studien untersucht, die zeigten, dass der Impfstoff 28 Tage nach der Impfung bei Erwachsenen und Jugendlichen die Produktion von Antikörpern auslöste, die bei Erwachsenen bis zu drei Jahre und bei Jugendlichen bis zu fünf Jahre anhielten [1]. Diese Immunantwort wurde auch bei schwangeren Frauen 28 Tage nach der Impfung im zweiten oder dritten Trimester ausgelöst. Die bei der Geburt auf die Säuglinge übertragenen Pertussis-Antikörper blieben bis zu einem Alter von zwei Monaten bestehen. Zu den häufigsten Nebenwirkungen von VacPertagen zählen Schmerzen an der Injektionsstelle, Kopfschmerzen, Müdigkeit, Myalgie, Arthralgie, Unwohlsein und Übelkeit.
Folgt die Europäische Kommission der Empfehlung des CHMP und wird VacPertagen in Europa zugelassen, wäre es aktuell der einzige monovalente Pertussis-Impfstoff. Seit der Marktrücknahme früherer monovalenter Impfstoffe in Deutschland vor etwa 20 Jahren stehen für die Immunisierung gegen Pertussis hierzulande, sowie in Österreich und Schweiz, ausschließlich verschiedene Kombinationsimpfstoffe (als 3-, 4-, 5- oder 6-fach-Impfstoffe) zur Verfügung, die gleichzeitig gegen Diphtherie, Tetanus, Poliomyelitis, Hepatitis B und Haemophilus influenzae Typ b schützen.
1 European Medicines Agency (EMA). VacPertagen - summary of opinion. EMA/CHMP/354843/2025; published online Nov 14, 2025. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-vacpertagen_en.pdf
2 Zepp, F. et al. Rationale for Pertussis Booster Vaccination Throughout Life in Europe. Lancet Infect Dis 2011; 11(7):557-70. doi: 10.1016/S1473-3099(11)70007-X
3 Sheng, Y. et al. Pertussis Resurgence: Epidemiological Trends, Pathogenic Mechanisms and Preventive Strategies. Front Immunol. 2025; 16:1618883. doi: 10.3389/fimmu.2025.1618883
4 Hellenbrand, W. et al. The Epidemiology of Pertussis in Germany: Past and Present. BMC Infect Dis. 2009; 9:22. doi: 10.1186/1471-2334-9-22
5 Hitz, D.A. et al. Seasonal Bordetella Pertussis Pattern in the Period From 2008 to 2018 in Germany. BMC Infect Dis. 2020; 20(1):474. doi: 10.1186/s12879-020-05199-w
6 Kline, J.M. et al. Pertussis: Common Questions and Answers. Am Fam Physician 2021; 104(2):186-192. URL: https://www.aafp.org/pubs/afp/issues/2021/0800/p186.html
7 Kandeil, W. et al. A Systematic Review of the Burden of Pertussis Disease in Infants and the Effectiveness of Maternal Immunization Against Pertussis. Expert Rev Vaccines. 2020; 19(7):621-638. doi:
10.1080/14760584.2020.1791092
8 Schielke, A. et al. Marked Underreporting of Pertussis Requiring Hospitalization in Infants as Estimated by Capture-Recapture Methodology, Germany, 2013-2015. Pediatr Infect Dis J. 2018;
37(2):119-125. doi: 10.1097/INF.0000000000001698
9 Gorringe, A. et al. Global Incidence of Pertussis After the COVID-19 Pandemic. JAMA Netw Open. 2025; 8(12):e2545963. doi: 10.1001/jamanetworkopen.2025.45963
17.12.2025
INFEKTIO_Podcast | Vom Bock zum Gärtner – Borrelien richtig diagnostizieren und behandeln
Der Podcast consilium infectiorum bietet medizinischem Fachpersonal praxisrelevante Themen der klinischen Infektiologie und unterstützt dabei, evidenzbasierte Behandlungsoptionen für Patienten
auszuwählen.
In jeder Folge diskutiert Infektiologe Prof. Mathias Pletz aus Jena mit einem Expertengast einen klinischen Schwerpunkt – fundiert und dennoch in entspannter Gesprächsatmosphäre.
Besonders praktisch: Für jede Folge können Sie bis zu einem Jahr nach Veröffentlichung CME-Punkte sammeln, indem Sie die zugehörigen CME-Fragen beantworten.
In der aktuellen Folge ist Dr. Volker Fingerle vom nationalen Referenzzentrum für Borrelien zu Gast. Gemeinsam widmen sie sich dem Thema Borrelien-Infektionen.
17.12.2025
Neue Impfempfehlungen für immunsupprimierte Patienten: COVID-19, Influenza und RSV
Die Infectious Diseases Society of America (IDSA) hat neue Leitlinien für die Impfung immunsupprimierter Patienten gegen COVID-19, Influenza und das Respiratorische Synzytialvirus (RSV) veröffentlicht. Die Empfehlungen richten sich an Patienten mit hämatologischen Malignomen, primären Immundefekten, Autoimmunerkrankungen unter Immunsuppressiva oder Biologika sowie HIV-Patienten mit schwerer Immunsuppression. Auch Empfänger von soliden Organtransplantaten, hämatopoetischen Stammzelltransplantationen und CAR-T-Zell-Therapien werden berücksichtigt.
Für die COVID-19-Impfung zeigten Studien eine Impfwirksamkeit von 33 % bis 56 % hinsichtlich der Verhinderung von Krankenhausaufenthalten. Die Wirksamkeit gegen kritische Erkrankungen lag bei 40 % (95-%-Konfidenzintervall [KI] 26–51 %) und gegen COVID-19-bedingte Sterblichkeit bei 61 % (95-%-KI 36–77 %). Schwerwiegende unerwünschte Ereignisse traten selten auf.
Bei der Influenza-Impfung wurde eine Wirksamkeit von 32 % (95-%-KI 7–50 %) gegen influenzabedingte Hospitalisierungen bei immunsupprimierten Erwachsenen nachgewiesen. Die Wirksamkeit gegen Aufnahmen auf Intensivstationen betrug 41 % (95-%-KI 31–50 %). Die Sicherheitsdaten zeigten kein erhöhtes Risiko für das Guillain-Barré-Syndrom oder andere schwerwiegende Nebenwirkungen.
Die RSV-Impfung erwies sich als besonders effektiv mit einer Wirksamkeit von 70 % (95-%-KI 66–73 %) gegen RSV-assoziierte Hospitalisierungen. Gegen kritische Erkrankungen, definiert als Intensivaufnahme oder Tod im Krankenhaus, lag die Wirksamkeit bei 81 % (95-%-KI 52–92 %). Es wurde ein leicht erhöhtes Risiko für das Guillain-Barré-Syndrom mit 11,2 zusätzlichen Fällen pro 1 Million Impfdosen beobachtet.
Die IDSA empfiehlt für alle drei Impfungen eine altersgerechte Verabreichung (starke Empfehlung, moderate Evidenzqualität). Die Impfungen können gleichzeitig verabreicht werden. Für eine optimale Wirksamkeit sollte der Impfzeitpunkt an die individuelle immunsuppressive Therapie angepasst werden. Bei Organtransplantationen wird die Impfung idealerweise mindestens 2 Wochen vor der Transplantation oder frühestens 1–3 Monate danach empfohlen. Nach hämatopoetischer Stammzelltransplantation oder CAR-T-Zell-Therapie sollte mindestens 3 Monate gewartet werden.
Folgerung der Autoren
Die IDSA-Leitlinien unterstreichen die Bedeutung der Impfungen gegen COVID-19, Influenza und RSV bei immunsupprimierten Patienten. Trotz möglicherweise reduzierter Impfantwort überwiegt der Nutzen
deutlich die Risiken. Individuelle Impfstrategien, einschließlich der Berücksichtigung von Therapieplänen und Risikofaktoren, sind essenziell für einen optimalen Schutz dieser vulnerablen
Patientengruppe.
19.11.2025
Kurz gefragt: Wie lesen Sie Fachinformationen?
Fachinformationen lassen sich heute auf ganz unterschiedlichen Wegen nutzen. Daher interessiert uns, wie Sie solche Inhalte in Ihrem Alltag am liebsten lesen – egal ob digital oder gedruckt. Ihre
kurze Rückmeldung hilft uns zu verstehen, über welches Medium Sie Fachinformationen am häufigsten nutzen.
Bitte nehmen Sie sich ca. 1 Minute Zeit, um uns Ihr Feedback mitzuteilen. Als Dank erhalten Sie das Whitepaper zum Thema „Antibiotic Stewardship”.
19.11.2025
ECDC startet neue Berichte und Leitlinien zu mückenübertragenen Krankheiten in Europa
In diesem Jahr hat das Europäische Zentrum für die Prävention und die Kontrolle von Krankheiten (ECDC) eine neue Reihe wöchentlicher Überwachungsberichte gestartet. Diese sollen Gesundheitsbehörden dabei unterstützen, mückenübertragene Krankheiten wie Chikungunya, Dengue, Zika und West-Nil-Virus zeitnah zu überwachen. Durch die Bereitstellung konsistenter, nahezu Echtzeit-epidemiologischer Daten können die Berichte nationale und regionale Kontrollstrategien unterstützen, insbesondere da Europa aufgrund des Klimawandels mit längeren und intensiveren Mückensaisons konfrontiert ist.
Die Hauptvektoren, die in Europa Anlass zur Sorge geben, sind Aedes albopictus, Aedes aegypti und Culex pipiens. Aedes albopictus ist derzeit in 16 Ländern und 369
Regionen etabliert – deutlich mehr als noch vor einem Jahrzehnt. Im vergangenen Jahr wurden in Europa 304 Fälle von lokal erworbenem Dengue-Fieber und 1.436 Fälle von West-Nil-Virus-Infektionen
registriert, was die wachsende Ausbreitung dieser Krankheiten unterstreicht.
Um die Vorbereitungsmaßnahmen weiter zu unterstützen, veröffentlicht das ECDC auch neue Leitlinien für das öffentliche Gesundheitswesen zu lokal erworbenen Aedes-übertragenen Krankheiten in Europa.
Das Dokument beschreibt praktische Überwachungs-, Präventions- und Kontrollmaßnahmen, basierend auf vier Risikoniveaus.
19.11.2025
Weltweite Aktionswoche zur World Antimicrobial Awareness Week 2025
Die Weltgesundheitsorganisation WHO ruft zur World Antimicrobial Resistance Awareness Week 2025 auf, die vom 18. bis zum 24. November stattfindet. Diese globale Kampagne soll das Bewusstsein für antimikrobielle Resistenzen (AMR) schärfen und zu verantwortungsvollem Umgang mit Antibiotika sensibilisieren. Die WHO stellt dafür Kampagnenmaterialien zur Verfügung und lädt zur Teilnahme an der „Go Blue for AMR“-Initiative ein.
19.11.2025
Respiratorische Virusinfektionen aktivieren metastatische Brustkrebszellen in der Lunge
Brustkrebs ist weltweit die häufigste Krebserkrankung bei Frauen, wobei die meisten Todesfälle durch Metastasen verursacht werden. Oft bleiben disseminierte Tumorzellen über lange Zeiträume hinweg in einem Ruhezustand, bevor es zu einer metastatischen Progression kommt. Das Verständnis der Mechanismen, die diesen Ruhezustand durchbrechen, ist entscheidend für die Behandlung von Metastasen. Infektionen durch respiratorische Viren wie Influenza und SARS-CoV-2 lösen sowohl lokale als auch systemische Entzündungsreaktionen aus.
In einer aktuellen Studie konnten Forscher in Mausmodellen zeigen, dass Infektionen mit Influenza- und SARS-CoV-2-Viren zum Verlust des Ruhephänotyps von Brustkrebszellen in der Lunge führen. Dies führte innerhalb weniger Tage nach der Infektion zu einer Proliferation der Krebszellen und innerhalb von zwei Wochen zu einer massiven Expansion zu metastatischen Läsionen. Diese phänotypischen Übergänge und Expansionen erwiesen sich als Interleukin-abhängig.
Die Studie verwendete verschiedene Mausmodelle für Brustkrebs, darunter MMTV-PyMT und MMTV-Her2 Mäuse, die jeweils die Onkogene Polyomavirus mittleres T-Antigen (PyMT) bzw. Her2 exprimieren. MMTV-Her2 Mäuse (FVB) wurden mit IL-6-Knockout (KO) Mäusen gekreuzt. Für ein orthotopes Modell des Brustkrebses wurden E0771 Brustkrebszellen in die vierte rechte und linke Brustdrüse injiziert. Acht Wochen alte MMTV-PyMT und 12-14 Wochen alte MMTV-Her2 weibliche Mäuse wurden mit 500 PFU Influenza A/PR/8/34 H1N1 IAV oder SARS-CoV-2 intranasal infiziert.
Die Studie zeigte, dass virale respiratorische Infektionen (Influenza und SARS-CoV-2) die Aktivierung von Lungen T-Zellen beeinträchtigen und dass CD4+ T-Zellen die pulmonale metastatische Last nach der Influenzainfektion aufrechterhalten, indem sie die Aktivierung und Zytotoxizität von CD8+T-Zellen hemmen. Diese experimentellen Befunde stimmen mit Analysen von Daten zu Krebsüberlebenden aus den US-Datenbanken überein.
Analysen der SEER-Medicare-Datenbank für alle Krebsarten und der Flatiron Health-Datenbank für Brustkrebs zeigten, dass eine SARS-CoV-2-Infektion das Risiko für krebsbedingte Mortalität und Lungenmetastasen im Vergleich zu nicht infizierten Krebsüberlebenden deutlich erhöhte. Bei der Analyse der SEER-Medicare-Daten wurden 13,3 Millionen Medicare-Begünstigte im Alter von 65 Jahren oder älter eingeschlossen, von denen 3,14 Millionen eine Krebsdiagnose hatten. Von diesen hatten 164.507 (5,24 %) eine SARS-CoV-2-Diagnose. In der Flatiron Health-Datenbank wurden 69.256 Brustkrebspatienten analysiert, von denen 5.602 (8,1 %) eine SARS-CoV-2-Diagnose hatten.
Folgerung der Autoren
Diese Entdeckungen unterstreichen den erheblichen Einfluss respiratorischer Virusinfektionen auf das Wiederauftreten metastatischer Krebserkrankungen. Sie liefern neue Erkenntnisse über den Zusammenhang zwischen Infektionskrankheiten und Krebsmetastasen. Die Ergebnisse deuten darauf hin, dass respiratorische Virusinfektionen wie Influenza und SARS-CoV-2 nicht nur eine unmittelbare Gesundheitsbedrohung darstellen, sondern auch langfristige Auswirkungen auf Krebspatienten haben können, insbesondere in Bezug auf die Entwicklung von Lungenmetastasen. Die Autoren betonen die Notwendigkeit weiterer Forschung zur Entwicklung gezielter Präventions- und Behandlungsstrategien für Krebspatienten mit respiratorischen Virusinfektionen.
Kommentar der Herausgeber
Eine weitere spannende Studie, die belegt, dass Infektionen nicht-infektiöse Folgeerkrankungen auslösen oder aggravieren können. Es gibt – neben dem klar belegten Zusammenhang zwischen HPV und Zervixkarzinomen – Daten zu Influenza, RSV und Pneumokokken und kardiovaskulären Ereignissen und Herpes Zoster und Demenz. Solche Daten zu erwünschten Impfwirkungen könnten helfen, die Impfbereitschaft zu steigern.
Chia, S. B. et al. Respiratory viral infections awaken metastatic breast cancer cells in lungs. Nature. 2025; 625(7993):572-581. doi: 10.1038/s41586-024-07003-0
22.10.2025
In eigener Sache
Update der S3-Leitlinie Sepsis 2025: Neue Empfehlungen für die Praxis
Die Deutsche Sepsis-Gesellschaft hat gemeinsam mit 15 weiteren Fachgesellschaften die S3-Leitlinie zur Sepsis grundlegend überarbeitet. Das Update bringt wichtige Neuerungen für Prävention, Diagnose, Therapie und Nachsorge. Besonders bedeutsam sind die Empfehlungen zum frühen Sepsis-Screening, zur antimikrobiellen Therapie und zur Nachsorge von Sepsis-Überlebenden. Die neuen Leitlinien orientieren sich an aktuellen internationalen Standards und bieten konkrete Handlungsempfehlungen für die klinische Praxis.
Lesen Sie hier als Abonnent:in weiter
Sie haben noch kein Abo?
» Hier informieren und Zugang zu allen Fachartikeln erhalten.
Zulassungsempfehlung für weiteren Antikörper zur RSV-Prophylaxe
In Deutschland sind Infektionen mit dem Respiratorischen Synzytial-Virus (RSV) die häufigste Ursache für Krankenhauseinweisungen von Säuglingen, bei denen insbesondere in den ersten sechs Lebensmonaten ein erhöhtes Risiko für schwere Krankheitsverläufe besteht [1]. Seit Juni 2024 empfiehlt die Ständige Impfkommission (STIKO) am Robert Koch-Institut (RKI) daher allen Neugeborenen und Säuglingen in ihrer ersten RSV-Saison eine Prophylaxe mit dem monoklonalen Antikörper Nirsevimab [1]. Dass diese Strategie Wirkung zeigt, legt eine erste Auswertung von Meldedaten aus Deutschland nahe [2]. Seit der Einführung der RSV-Prophylaxe konnte die Krankheitslast bei Säuglingen < 1 Jahr deutlich reduziert werden: im Vergleich zur Vorsaison sank die Inzidenz der an das RKI übermittelten laborbestätigten RSV-Fälle 2024/2025 um 54 %. Nachdem der Ausschuss für Humanarzneimittel (CHMP) bei der europäischen Arzneimittelbehörde EMA im September 2025 das Präparat ENFLONSIA der Firma Merck Sharp Dohme zur Zulassung empfohlen hat, könnte demnächst ein weiterer monoklonaler Antikörper zur RSV-Prophylaxe von Neugeborenen und Säuglingen in Europa zur Verfügung stehen [3].
ENFLONSIA enthält Clesrovimab, ein neutralisierender humaner monoklonaler IgG1κ-Antikörper, der gegen das RSV-Fusionsprotein F gerichtet ist [3]. Das Fusionsprotein auf der Oberfläche des Virus ist maßgeblich an der Infektion des Körpers beteiligt, indem es die Fusion mit den Schleimhautepithelzellen des Respirationstraktes ermöglicht. Die Bindung von Clesrovimab an das Fusionsprotein blockiert den entscheidenden Membranfusionsschritt und verhindert das Eindringen des Virus in die Zellen [3, 4]. Durch eine Modifizierung der Aminosäuresequenz in der FC-Region des Antikörpers ist die Bindung an den neonatalen FC-Rezeptor erhöht und damit die Serumhalbwertszeit auf etwa 44 Tage verlängert [3, 4].
In einer randomisierten, doppelblinden, placebokontrollierten Phase-IIb/III-Studie erhielten 3614 gesunde Säuglinge entweder eine intramuskuläre Einzeldosis von 105mg Clesrovimab (n = 2411) oder Placebo (n = 1203) [5]. Die Inzidenz medizinisch behandelter RSV-Infektionen der unteren Atemwege innerhalb von 150 Tagen nach der Injektion betrug 2,6 % unter Clesrovimab gegenüber 6,5 % unter Placebo, entsprechend einer Wirksamkeit der Prophylaxe von 60,4 % (95 %-Konfidenzintervall (KI) 44,1-71,9 %; p < 0,001). Auch RSV-assoziierte Hospitalisierungen konnten nach der Applikation von Clesrovimab innerhalb des Beobachtungszeitraums signifikant reduziert werden (Wirksamkeit 84,2 %; 95 %-KI 66,6-92,6 %; p < 0,001). Die Sicherheitsprofile waren vergleichbar, wobei schwerwiegende unerwünschte Ereignisse bei 11,5 % der mit Clesrovimab behandelten Säuglinge gegenüber 12,4 % in der Placebogruppe berichtet wurden.
In einer weiteren randomisierten, teilweise verblindeten Phase-III-Studie wurde die Wirksamkeit und Sicherheit einer Einzeldosis Clesrovimab (n = 450) im Vergleich zur monatlichen Applikation von Palivizumab (n = 451) bei Säuglingen und Kindern mit erhöhtem Risiko für schwere RSV-Erkrankungen untersucht [6]. Erste Zwischenergebnisse für den Zeitraum von 150 Tagen nach der (ersten) Injektion zeigten eine ähnliche Inzidenz medizinisch behandelter RSV-Infektionen der unteren Atemwege (3,6 % bzw. 3,0 %) und RSV-assoziierter Hospitalisierungen (1,3 % bzw. 1,5 %) unter Clesrovimab und Palivizumab bei vergleichbarem Sicherheitsprofil.
Zu den häufigsten Nebenwirkungen zählen Schmerzen, Erytheme und Schwellungen an der Injektionsstelle sowie Hautausschlag.
Wenn die Europäische Kommission der positiven Stellungnahme des CHMP folgt und die Zulassung für ENFLONSIA erteilt, ist Clesrovimab der dritte monoklonale Antikörper zur RSV-Prophylaxe in Europa und der erste, der unabhängig vom Gewicht des Säuglings als einmalige Fixdosis verabreicht wird. Clesrovimab bindet an der hochkonservierten Stelle IV des RSV-Fusionsproteins, was sich von den RSV-Antikörpern Palivizumab (Stelle II) und Nirsevimab (Stelle Ø) unterscheidet. Aufgrund der verlängerten Halbwertszeit bietet eine Dosis Clesrovimab, ähnlich wie Nirsevimab, bis zu fünf Monate lang passive Immunität, was die Dauer einer üblichen RSV-Saison in Europa abdeckt.
1 Koch, J. et al. Beschluss und wissenschaftliche Begründung zur Empfehlung der STIKO zur spezifischen Prophylaxe von RSV-Erkrankungen mit Nirsevimab bei Neugeborenen und Säuglingen in ihrer 1. RSV-Saison. Epid Bull 2024; 26:3-29. doi: 10.25646/12198 [24.09.2025]
2 Schönfeld, V. et al. The incidence of RSV infection since the introduction of monoclonal antibody prophylaxis: An analysis of reported case data across Germany for the seasons 2023/24 and 2024/25.
Dtsch Arztebl Int. 2025; 122:472–3. doi: 10.3238/arztebl.m2025.0111
3 European Medicines Agency (EMA). Enflonsia - summary of opinion. EMA/CHMP/274513/2025; published online Sep 19, 2025. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-enflonsia_en.pdf [24.09.2025]
4 U.S. Food & Drug Administration (FDA). ENFLONSIA (Clesrovimab-cfor): Full Prescribing Information. Jun 2025. URL: https://www.accessdata.fda.gov/drugsatfda_docs/label/2025/761432s000lbl.pdf [24.09.2025]
5 Zar, H. J. et al. Clesrovimab for Prevention of RSV Disease in Healthy Infants. N Engl J Med. 2025; published online first Sep 17, 2025. doi: 10.1056/NEJMoa2502984
6 Zar, H. J. et al. Clesrovimab in Infants and Children at Increased Risk for Severe RSV Disease. N Engl J Med 2025; published online first Sep 17, 2025. doi: 10.1056/NEJMc2506107
22.10.2025
Ausbruch von Corynebacterium diphtheriae bei Migranten in Europa
Ein ungewöhnlicher Anstieg von Infektionen mit Corynebacterium diphtheriae wurde ab Sommer 2022 in europäischen Aufnahmezentren für Migranten beobachtet. Ein pan-europäisches Konsortium untersuchte die klinischen, epidemiologischen und mikrobiologischen Merkmale dieses Ausbruchs, der den größten Anstieg von Diphtherie-Fällen in Westeuropa seit 70 Jahren darstellt.
In die Analyse wurden 363 toxigene C. diphtheriae-Isolate von 362 Patienten aus 10 europäischen Ländern einbezogen, die zwischen Januar und November 2022 gemeldet wurden. Die meisten Fälle traten in Deutschland (118), Österreich (66), Großbritannien (59), der Schweiz (52) und Frankreich (30) auf. Das mediane Alter der Patienten betrug 18 Jahre, wobei 176 Patienten (48,6 %) zwischen 16 und 20 Jahre alt waren. Die große Mehrheit der Betroffenen (98,1 %) war männlich. Bei 348 Patienten (96,1 %) lag eine kürzliche Migrationsgeschichte vor oder sie hatten engen Kontakt zu Migrantenpopulationen. 174 Patienten (48,1 %) waren in Migrantenzentren untergebracht.
Klinische Daten lagen für 346 Patienten (95,6 %) vor: 268 Patienten (77,5 %) wiesen eine kutane Diphtherie auf, 53 (15,3 %) eine respiratorische Form (11 davon mit Pseudomembran) und 9 (2,6 %) zeigten sowohl respiratorische als auch kutane Symptome. Ein Patient mit Pseudomembran verstarb. Bei drei Patienten wurde eine genitale Beteiligung festgestellt. Der Impfstatus konnte aufgrund unvollständiger medizinischer Dokumentation häufig nicht zuverlässig ermittelt werden. Nur bei 4 Patienten war eine Impfung dokumentiert, bei 10 Patienten wurde eine fehlende Impfung vermerkt und bei 290 Patienten war der Impfstatus unbekannt.
Von 17 hospitalisierten Patienten hatten 5 eine kutane und 12 eine respiratorische Diphtherie (7 mit Pseudomembran). Alle 12 Patienten mit respiratorischer Diphtherie erhielten Diphtherie-Antitoxin zusammen mit Antibiotika. Die Antitoxin-Dosen lagen zwischen 5000 und 100.000 IE, wobei 8 Patienten Dosen über 60.000 IE erhielten. Die Behandlung erfolgte im Durchschnitt 2,8±1,5 Tage nach Symptombeginn, die meisten (9) Patienten wurden innerhalb von 3 Tagen behandelt.
Die molekulargenetische Analyse identifizierte vier Hauptcluster, was auf die multiklonale Natur des Ausbruchs hinweist. Das ermX-Gen (kodiert für Erythromycin-Resistenz) sowie die Gene pbp2m und blaOXA-2 (kodieren für β-Lactam-Resistenz) wurden in einer Untergruppe von Isolaten nachgewiesen. Isolate mit ermX waren resistent gegen Erythromycin, während Isolate mit pbp2m resistent gegen Penicillin, aber empfindlich gegenüber Amoxicillin waren.
Im Jahr 2023 wurden in den beteiligten Ländern weitere 169 Fälle von C. diphtheriae-Infektionen mit toxigenen Isolaten gemeldet: 112 in Deutschland, 17 in den Niederlanden, 16 in Frankreich, 13 in Großbritannien, 8 in der Schweiz und 3 in Österreich, mit zwei weiteren Todesfällen bei Migranten. Obwohl weniger Fälle als 2022 gemeldet wurden, lag die Gesamtzahl deutlich über den Vorjahren.
Folgerung der Autoren
Die Verteilung der genetischen C. diphtheriae-Cluster über mehrere europäische Länder zeigt eine wiederholte grenzüberschreitende Ausbreitung. Die hohe Anzahl von C. diphtheriae-Infektionen bei Migranten ist besorgniserregend, insbesondere da Antibiotikaresistenz-Phänotypen die Wirksamkeit von First-Line-Behandlungen gefährden. Die Ergebnisse unterstreichen die Notwendigkeit verbesserter Präventionsmaßnahmen, einschließlich gründlicher Impfprotokolle für Migranten und lokale Bevölkerungen, klinische Überwachung von Risikopersonen, schnelle Diagnose bei symptomatischen Personen sowie Screening von Kontaktpersonen.
Kommentar der Herausgeber
Die Diphtherie ist in Deutschland, Österreich und der Schweiz meldepflichtig und kann potenziell tödlich verlaufen. Bei häufig ungeimpften Migranten mit kutanen oder pharyngealen Symptomen ist es wichtig, an diese wichtige Differentialdiagnose zu denken. Entscheidend ist eine rasche Gabe von Antibiotika und, in toxin-positiven Fällen, aber auch bereits bei klinischem Verdacht auf eine respiratorische Diphtherie, frühzeitig von Antitoxin. Bei kutaner Diphtherie wird eine Antitoxin-Gabe in der Regel nicht empfohlen, außer bei Ulcera von mehr als 2 cm². Ebenso essenziell sind die Implementierung infektpräventiver und postexpositioneller Maßnahmen. Dieser multinationale Ausbruch einer alten, beinahe vergessenen Infektion führt eindrücklich vor Augen, wie wichtig eine gute Durchimpfungsquote ist, gerade angesichts grassierender Falschinformationen hinsichtlich der Sicherheit von Impfungen.
Hoefer, A. et al. Corynebacterium diphtheriae Outbreak in Migrant Populations in Europe. N Engl J Med. 2025; 392(23):2334-2345. doi: 10.1056/NEJMoa2311981
10.09.2025
WHO-Bericht deutet auf wahrscheinlichen zoonotischen Ursprung von COVID-19 hin
Ein kürzlich veröffentlichter Bericht der Weltgesundheitsorganisation (WHO) präsentiert neue Erkenntnisse zum Ursprung von COVID-19. Die Wissenschaftliche Beratergruppe für den Ursprung neuartiger Krankheitserreger (SAGO) hat die verfügbaren Beweise ausgewertet und kommt zu dem Schluss, dass ein zoonotischer Ursprung des SARS-CoV-2-Virus am wahrscheinlichsten ist. [1]
Der SAGO-Bericht stützt sich auf begutachtete Studien, Expertenbriefings und unveröffentlichte Daten. Die Gruppe betont, dass ein Übertritt des Virus von Tieren auf den Menschen die plausibelste Erklärung für den Ausbruch darstellt. Allerdings schließt der Bericht die Möglichkeit eines Laborunfalls nicht vollständig aus, da chinesische Behörden Anfragen zu Forschungsaktivitäten und Biosicherheitsverfahren in Laboren in Wuhan nicht beantwortet haben. [1,2]
Als stärkstes Indiz für einen zoonotischen Ursprung wird eine metagenomische Analyse von Tier- und Umweltproben aus dem Huanan-Markt in Wuhan angeführt. Diese bestätigte die Anwesenheit von für
SARS-CoV-2 anfälligen Tierarten in Marktständen mit hoher Virusbelastung. Insbesondere wurden DNA-Spuren von Marderhunden, Bambusratten und Schleichkatzen in Proben mit hoher SARS-CoV-2-Konzentration
nachgewiesen. [2,3]
Der Bericht hebt hervor, dass trotz umfangreicher Forschung weiterhin entscheidende Daten fehlen, um den genauen Zeitpunkt und Ort des ersten Übertritts auf den Menschen zu bestimmen. Es bleibt
unklar, ob der Huanan-Markt tatsächlich der Ursprungsort war oder ob er lediglich als Verstärker für die Virusausbreitung diente. [1,2]
SAGO fordert weitere Untersuchungen, insbesondere zu Tieren und Tierhändlern mit Verbindungen zum Huanan-Markt sowie zu Zuchtbetrieben in der Region. Auch empfiehlt die Gruppe, die Suche nach frühen
COVID-19-Fällen vor Dezember 2019 fortzusetzen. [1,3]
Der Bericht betont die Notwendigkeit internationaler Zusammenarbeit und Transparenz bei der Erforschung von Krankheitsausbrüchen. Er unterstreicht zudem die Bedeutung des „One Health“-Ansatzes, der
die Verbindungen zwischen Mensch, Tier und Umwelt berücksichtigt. [1,2]
Obwohl der zoonotische Ursprung als wahrscheinlichste Hypothese gilt, mahnt SAGO zur Vorsicht bei endgültigen Schlussfolgerungen. Die Gruppe bleibt offen für neue Erkenntnisse und betont die
Wichtigkeit weiterer Forschung zur Klärung des COVID-19-Ursprungs. [1,2,3]
1 WHO Scientific Advisory Group for the Origins of Novel Pathogens (SAGO). Independent assessment of the origins of SARS-CoV-2. World Health Organization. 2025. URL: https://cdn.who.int/media/docs/default-source/documents/epp/sago/independent-assessment-of-the-origins-of-sars-cov-2-by-sago.pdf?sfvrsn=b0f90ad4_4, zuletzt abgerufen am: 05.09.2025
2 Schneider L. WHO report suggests likely zoonotic origin of Covid-19, doesn't rule out lab leak. JAMA. 2025; 334(8):661-662. doi: 10.1001/jama.2025.10976
3 Crits-Christoph A. et al. Genetic tracing of market wildlife and viruses at the epicenter of the COVID-19 pandemic. Cell. 2025; 187(19):5468-5482.e11. doi: 10.1016/j.cell.2024.08.010
10.09.2025
STIKO-Empfehlung für Impfung gegen Chikungunya
Die Ständige Impfkommission am Robert-Koch-Institut (STIKO) hat in Zusammenarbeit mit der Deutschen Gesellschaft für Tropenmedizin, Reisemedizin und Globale Gesundheit e.V. (DTG) eine Empfehlung zur Chikungunya-Impfung erarbeitet [1]. Ziel der Empfehlung ist die Verhinderung von Erkrankungen, schweren Krankheitsverläufen und Tod durch eine Chikungunya-Infektion.
Chikungunya-Fälle wurden in Deutschland bisher nur bei Reiserückkehrern detektiert. Das allgemeine Risiko bei Reisen in Endemiegebiete wird zwar als gering eingestuft, steigt aber bei einer Reise in ein aktuelles Ausbruchsgebiet. Derzeit kommen verhältnismäßig viele infizierte Reisende aus Ländern mit Chikungunya-Ausbrüchen nach Deutschland zurück: im Vergleich zu normalerweise 2-5 Chikungunya-Fällen pro Monat in den Vorjahren, wurden dem RKI zwischen April und Juni 2025 bereits insgesamt 75 Fälle gemeldet, fast ausschließlich erworben auf Mauritius (33 %), La Réunion (29 %) und Sri Lanka (9 %).
Die STIKO empfiehlt die Reiseimpfung gegen Chikungunya daher allen Personen ≥ 12 Jahren,
- die in ein Gebiet reisen, für das ein aktuelles Chikungunya-Ausbruchsgeschehen bekannt ist,
- die einen längeren Aufenthalt (> 4 Wochen) oder wiederholte Kurzzeitaufenthalte in Chikungunya-Endemiegebieten planen und bei denen ein erhöhtes Risiko für eine Chronifizierung oder einen schweren Verlauf der Erkrankung besteht (z.B. Alter 60 Jahre oder eine schwere internistische Grunderkrankung).
Zudem wird Personen, die gezielte Tätigkeiten mit Chikungunya-Viren ausüben (z.B. in Forschungseinrichtungen oder Laboratorien), eine beruflich indizierte Impfung empfohlen.
Für die aktive Immunisierung ist eine Impfstoffdosis der beiden in Deutschland verfügbaren Impfstoffe VIMKUNYA oder IXCHIQ notwendig. Der Totimpfstoff VIMKUNYA ist für alle Personen ab 12 Jahren zugelassen und empfohlen, der attenuierte Lebendimpfstoff IXCHIQ soll gemäß STIKO-Empfehlung nur im Alter von 12 bis 59 Jahren eingesetzt werden. Innerhalb dieser Altersbereiche gelten beide Impfstoffe allgemein als gleichwertig.
Aufgrund eines unterschiedlichen Wirksamkeits- und Sicherheitsprofils kann bei häufigeren Reisen oder längeren beruflichen Einsätzen in Endemiegebieten der Lebendimpfstoff IXCHIQ bevorzugt werden, sofern keine Kontraindikationen wie eine bestehende oder geplante Schwangerschaft oder Immundefizienz bestehen. Da VIMKUNYA in den Zulassungsstudien ein günstigeres Sicherheitsprofil aufwies, ist für einmalige Reisen oder bei erhöhter Relevanz möglicher Nebenwirkungen eher der Totimpfstoff VIMKUNYA zu erwägen.
Zum Zeitpunkt der Veröffentlichung der STIKO-Empfehlung (10.07.2025) war die Anwendung von IXCHIQ bei Personen ≥ 65 Jahren vorübergehend kontraindiziert, nachdem im Frühjahr 2025 eine Reihe von Fallberichten über schwerwiegende Nebenwirkungen in dieser Altersgruppe bekannt geworden waren [2]. Nach Abschluss der Überprüfung durch den Sicherheitsausschuss (PRAC) der europäischen Arzneimittelbehörde EMA wurde am 11. Juli 2025 die Aufhebung der Altersbeschränkung bekannt gegeben, da das Nutzen-Risiko-Verhältnis des Impfstoffes weiterhin grundsätzlich positiv ist [3]. Dennoch sollte der Impfstoff bei Menschen aller Altersgruppen nur bei einem erheblichen Risiko für eine Infektion und nach sorgfältiger Nutzen-Risiko-Abwägung eingesetzt werden. Dies betrifft insbesondere vorerkrankte Personen über 65 Jahre, bei denen eine erhöhte Reaktogenität des Impfstoffes zu beobachten war und die gleichzeitig ein erhöhtes Risiko für einen schweren Verlauf der Infektion und eine Chronifizierung der Symptome aufweisen.
In Österreich wird die Impfung gegen Chikungunya Reisenden in Endemiegebiete ab dem vollendeten 12. Lebensjahr, bei epidemiologischem Risiko und exponiertem Laborpersonal empfohlen. Basierend auf dem vermutlich günstigeren Nebenwirkungsprofil, soll der Totimpfstoff VIMKUNYA bei Verfügbarkeit und entsprechender Indikation vor allem bei älteren Menschen und Personen mit Grunderkrankungen bevorzugt werden [4]. In der Schweiz sind derzeit noch keine Impfstoffe gegen Chikungunya zugelassen.
1 Kling, K. et al. Beschluss und wissenschaftliche Begründung der STIKO-Empfehlung zur Impfung gegen Chikungunya. Epid Bull 2025; 28:3-38. doi: 10.25646/13274
2 European Medicines Agency (EMA). EMA starts review of Ixchiq (live attenuated chikungunya vaccine); published online May 7, 2025. URL: https://www.ema.europa.eu/en/news/ema-starts-review-ixchiq-live-attenuated-chikungunya-vaccine [03.08.2025]
3 European Medicines Agency (EMA). Ixchiq: temporary restriction on vaccinating people 65 years and older to be lifted; published online Jul 11, 2025. URL: https://www.ema.europa.eu/en/news/ixchiq-temporary-restriction-vaccinating-people-65-years-older-be-lifted [03.08.2025]
4 Bundesministerium für Arbeit, Soziales, Gesundheit, Pflege und Konsumentenschutz. Impfempfehlung Chikungunya (Stand 25.07.2025). URL: https://www.sozialministerium.gv.at/dam/jcr:0c5032e7-6bac-4264-b538-a20fda08477e/Impfplan%20Chikungunya_25.07.2025.pdf [03.08.2025]
13.08.2025
Update zur Einstufung und Nutzenbewertung von Reserveantibiotika gemäß §35a SGB V (2025)
Version 2.2 (RKI/BfArM) aktualisiert Kriterien und Erregerliste für die indikations- und erregerspezifische Einstufung von Reserveantibiotika, die in Deutschland von der Zusatznutzenbewertung freigestellt sind.
Wichtigste Änderungen der aktuellen Version (2025)
- Datengrundlagen: Anpassung der Surveillance-Daten (ARS, Antibiotika-Resistenz-Surveillance) und Einbeziehung aktueller Resistenztrends sowie Bewertung der klinischen Relevanz.
- Kriterienanpassung: Die Einstufung eines Reserveantibiotikums erfolgt stärker erregerspezifisch und indikationsbezogen (entsprechend der Erregerliste), ohne Einschränkung auf den Schweregrad der Infektion oder die Patientengruppe.
- Indikatortabelle: Der unspezifische Begriff „potenziell schwerwiegend“ wurde gestrichen; nur klar definierte und überprüfbare Kriterien bleiben erhalten.
- Checkliste und Flowchart: Überarbeitung zur eindeutigen Zuordnung für Antragstellung und Bewertung beim G-BA.
Einstufung eines neuen Reserveantibiotikums – Kriterien des G-BA
Ein neues Antibiotikum erhält den Reserveantibiotika-Status, wenn:
- Es wirksam gegen mindestens einen relevanten multiresistenten Erreger der Erregerliste ist UND
- Nur eingeschränkte klinisch gleichwertige Therapieoptionen bestehen.
- Der Antrag muss aussagekräftige in-vitro- und in-vivo-Wirksamkeitsdaten (mindestens 10 Patienten), Leitlinienprüfung der Therapieoptionen sowie eine Bezugnahme auf die nationale Resistenzsituation enthalten.
Fazit für die Praxis
Die Einstufung erfolgt gezielt nach Erreger und Indikation. Für die Zulassung als Reserveantibiotikum sind limitierte Therapiealternativen und belegte Wirksamkeit gegen aktuelle MRE entscheidend. Die
Erregerliste dient unmittelbar als Orientierungshilfe in Klinik, Forschung und bei G BA-Anträgen.
13.08.2025
Rifaximin zusätzlich zu Antibiotika bei akuter hepatischer Enzephalopathie bei kritisch kranken Patienten mit Leberzirrhose
Die hepatische Enzephalopathie (HE) ist eine potenziell reversible Komplikation des Leberversagens, die durch unterschiedliche Grade kognitiver Beeinträchtigungen gekennzeichnet ist und häufig eine Aufnahme auf der Intensivstation (ICU) erfordert. Kritisch kranke Patienten mit Leberzirrhose erhalten auf der ICU üblicherweise Breitspektrum-Antibiotika aufgrund vermuteter Infektionen oder gemäß Krankenhausprotokoll. Bisher war unklar, ob zusätzliches Rifaximin einen synergistischen Effekt mit Breitspektrum-Antibiotika bei ICU-Patienten mit akuter manifester HE hat.
In einer doppelblinden, randomisierten kontrollierten Studie in Indien wurden zwischen Februar 2022 und April 2023 Patienten mit manifester HE auf der ICU entweder der Gruppe mit alleiniger Antibiotikatherapie (AB) oder der Gruppe mit Antibiotika plus Rifaximin (AB + R) zugeteilt. Die Baseline-Charakteristika und Schweregrad-Scores waren in beiden Gruppen (je 92 Patienten) vergleichbar. Carbapenem- und Cephalosporin-Antibiotika mit β-Lactamase-Inhibitoren waren die am häufigsten eingesetzten Antibiotika.
In der Kaplan-Meier-Analyse erreichten 44,6 % (41/92; 95-%-Konfidenzintervall [KI] 32–70,5) in der AB-Gruppe und 46,7 % (43/92; 95-%-KI 33,8–63) in der AB + R-Gruppe den primären Endpunkt einer Reduktion der HE um 2 Grade oder komplette Resolution (p = 0,84). Die Zeit bis zum Erreichen des primären Endpunkts war mit 3,65 ± 1,82 Tagen vs. 4,11 ± 2,01 Tagen vergleichbar (p = 0,27). Auch die Krankenhaussterblichkeit unterschied sich nicht signifikant zwischen den Gruppen (62 % vs. 50 %; p = 0,13). Nosokomiale Infektionen traten bei 7 % in der AB-Gruppe und 13 % in der AB + R-Gruppe auf (p = 0,21). Die Endotoxin-Spiegel wurden durch Rifaximin nicht beeinflusst.
In der Subgruppenanalyse zeigte sich bei Patienten mit dekompensierter Zirrhose unter Rifaximin eine niedrigere Krankenhaussterblichkeit (Hazard Ratio 0,39; 95-%-KI 0,2–0,76), nicht jedoch bei Patienten mit akut-auf-chronischem Leberversagen (Hazard Ratio 0,99; 95-%-KI 0,6–1,63). Dies war auf eine reduzierte Rate nosokomialer Infektionen zurückzuführen.
In der multivariaten Cox-Regressionsanalyse waren nur der Serum-Bilirubinspiegel (Hazard Ratio 0,96; 95-%-KI 0,94–0,99; p = 0,005), der Serum-Albuminspiegel (Hazard Ratio 1,68; 95-%-KI 1,12–2,5; p
= 0,01) und der SOFA-Score (Hazard Ratio 0,88; 95-%-KI 0,82–0,95; p = 0,002) bei Aufnahme prädiktiv für eine Verbesserung der HE.
Folgerung der Autoren
Die Rückbildung einer manifesten HE bei Patienten unter Antibiotikatherapie war vergleichbar mit der bei Patienten, die zusätzlich Rifaximin erhielten. Rifaximin zeigte keinen signifikanten Beitrag zur Auflösung der HE bei kritisch kranken Patienten mit Leberzirrhose auf der ICU, die bereits Lactulose und andere Antibiotika erhielten.
Kommentar der Herausgeber
Rifaximin zeigte in dieser Studie etwas überraschend außer in der Subgruppe von Patienten mit dekompensierter Leberzirrhose, keinen klinischen Nutzen. Dies könnte zum einen daran liegen, dass die Patienten insgesamt schwer krank waren und bereits bei Einschluss Infektionen hatten, und andererseits, dass Rifaximin insbesondere über die Darmmikrobiota und eine Epithelstabilisierung wirkt, aber weniger Effekte auf bakterielle Translokation und Inflammation hat.
Kulkarni, A. V. et al. Antibiotics With or Without Rifaximin for Acute Hepatic Encephalopathy in Critically Ill Patients With Cirrhosis: A Double-Blind, Randomized Controlled (ARiE) Trial. Am J
Gastroenterol. 2024; 119(5):864-874.
doi: 10.14309/ajg.0000000000002575
17.07.2025
Welt-Hepatitis-Tag 2025
Der Welt-Hepatitis-Tag am 28. Juli 2025 steht unter dem internationalen Motto „Let's break it down" und wird in Deutschland mit dem Slogan „Lass uns Klartext reden" umgesetzt. Ziel des Aktionstages ist es, Mythen und Vorurteile zu Hepatitis-Viren, Ansteckungswegen, Verläufen und Therapien aufzuklären.
Weltweit leben laut WHO-Schätzungen 254 Millionen Menschen mit Hepatitis B und 50 Millionen mit Hepatitis C – viele, ohne es zu wissen. Unbehandelt können chronische Hepatitis-Infektionen zu Zirrhose und Leberkrebs führen. Es gibt fünf verschiedene Hepatitis-Viren (A bis E), die unterschiedlich übertragen werden.
Hepatitis A und E sind meist harmlos, während Hepatitis B und C und bei Immunsupprimierten auch Hepatitis E chronisch werden können. Gegen Hepatitis A und B gibt es Impfungen, Hepatitis C ist heute fast immer heilbar. Gegen Hepatitis E sind verschiedene Impfkandidaten gegen die in Entwicklungsländern aber nicht bei uns vorherrschenden Hepatitis E Serotypen 1 und 4 zugelassen oder in Entwicklung. Hepatitis D ist zwar selten, aber besonders gefährlich. Viele Hepatitis-Infektionen verlaufen unbemerkt. Ab 35 Jahren können sich Krankenversicherte einmalig kostenfrei auf Hepatitis B und C testen lassen.
17.07.2025
Thymosin α1 zeigt keine Wirksamkeit bei Sepsis
Eine aktuelle multizentrische, doppelblinde, placebokontrollierte Phase-3-Studie untersuchte die Wirksamkeit und Sicherheit von Thymosin α1 bei der Behandlung von Sepsis. Die TESTS-Studie (The Efficacy and Safety of Thymosin α1 for Sepsis) wurde zwischen September 2016 und Dezember 2020 in 22 Zentren in China durchgeführt und umfasste 1106 erwachsene Patienten im Alter von 18 bis 85 Jahren mit einer Sepsis-Diagnose nach Sepsis-3-Kriterien.
Die Patienten wurden im Verhältnis 1:1 randomisiert und erhielten entweder Thymosin α1 (n = 552) oder Placebo (n = 554). Die Randomisierung erfolgte stratifiziert nach Alter (< 60 und ≥ 60 Jahre) und Zentrum. Thymosin α1 wurde alle 12 Stunden über 7 Tage subkutan injiziert, sofern die Behandlung nicht aufgrund einer Entlassung von der Intensivstation, des Todes oder eines Widerrufs der Einwilligung vorzeitig beendet wurde.
Der primäre Endpunkt war die 28-Tage-Gesamtmortalität nach Randomisierung. In die modifizierte Intention-to-treat-Analyse wurden 1089 Patienten eingeschlossen, die mindestens eine Dosis der Studienmedikation erhalten hatten (Thymosin α1-Gruppe n = 542, Placebo-Gruppe n = 547). Das mediane Alter betrug 65 Jahre (Interquartilsbereich 52–73) und 68,9 % der Teilnehmer waren männlich.
Die 28-Tage-Gesamtmortalität trat bei 127 Patienten (23,4 %) in der Thymosin α1-Gruppe und bei 132 Patienten (24,1 %) in der Placebo-Gruppe auf (Hazard Ratio 0,97; 95-%-Konfidenzintervall 0,76 bis 1,24; P = 0,93 im Log-Rank-Test). Auch für die sekundären Endpunkte wie 90-Tage-Gesamtmortalität (Hazard Ratio 0,95; 95-%-KI 0,77 bis 1,17), Intensivstationsmortalität, Auftreten neuer Infektionen innerhalb von 28 Tagen und Änderung des SOFA-Scores an Tag 7 zeigten sich keine statistisch signifikanten Unterschiede zwischen den Gruppen.
In der präspezifizierten Subgruppenanalyse zeigte sich ein potenzieller differenzieller Effekt von Thymosin α1 auf den primären Endpunkt in Abhängigkeit vom Alter (< 60 Jahre: Hazard Ratio 1,67; 95-%-KI 1,04 bis 2,67; ≥ 60 Jahre: 0,81; 0,61 bis 1,09; P für Interaktion = 0,01) und Diabetes (mit Diabetes: 0,58; 0,35 bis 0,99; ohne Diabetes: 1,16; 0,87 bis 1,53; P für Interaktion = 0,04).
Insgesamt traten bei 730 Patienten (67,0 %) mindestens ein unerwünschtes Ereignis auf, ohne signifikante Unterschiede zwischen den Gruppen (Thymosin α1: 66,4 % vs. Placebo: 67,6 %; Gruppendifferenz −1,2 %; 95-%-KI −6,8 % bis 4,4 %; P = 0,70). Die häufigsten unerwünschten Ereignisse waren Anämie (10,7 %), gefolgt von Fieber (9,6 %), abdomineller Distension (5,4 %) und Gerinnungsstörungen (4,8 %). Es traten keine unerwarteten schwerwiegenden Nebenwirkungen im Zusammenhang mit Thymosin α1 auf.
In einer explorativen Analyse der Immunmarker zeigte sich nach einer Woche Behandlung in beiden Studienarmen eine ähnliche Veränderung der monozytären HLA-DR-Expression, der Lymphozytenzahl und des prozentualen Anteils regulatorischer T-Zellen. Die absolute Veränderung (Gruppendifferenz −1,7; 95-%-KI −3,0 bis −0,6; P = 0,02) und die prozentuale Veränderung (Gruppendifferenz 9 %; 2 % bis 15 %; P = 0,006) des Neutrophilen-Lymphozyten-Verhältnisses waren in der Thymosin α1-Gruppe jedoch größer als in der Placebo-Gruppe.
Folgerung der Autoren
Diese Studie fand keine eindeutigen Belege dafür, dass Thymosin α1 die 28-Tage-Gesamtmortalität bei erwachsenen Patienten mit Sepsis reduziert. Das gute Sicherheitsprofil des Medikaments bei der Behandlung von Sepsis wurde jedoch bestätigt. Zusätzlich könnte Thymosin α1 möglicherweise vorteilhafte Effekte bei Patienten im Alter von 60 Jahren und älter sowie bei Patienten mit chronischen Erkrankungen haben. Zukünftige Forschung sollte sich auf diese Patienten konzentrieren, um potenzielle therapeutische Vorteile zu klären.
Wu, J. et al. The efficacy and safety of thymosin α1 for sepsis (TESTS): multicentre, double blinded, randomised, placebo controlled, phase 3 trial. BMJ. 2025; 388:e082583. doi: 10.1136/bmj-2024-082583
Wu, J. et al. Corrections: The efficacy and safety of thymosin α1 for sepsis (TESTS): multicentre, double blinded, randomised, placebo controlled, phase 3 trial. BMJ. 2025; 389:r1098. doi: 10.1136/bmj.r1098
18.06.2025
INFEKTIO_Podcast | Startschwierigkeiten – Die Neugeborenensepsis
Der Podcast consilium infectiorum bietet medizinischem Fachpersonal praxisrelevante Themen der klinischen Infektiologie und unterstützt dabei, evidenzbasierte Behandlungsoptionen für Patienten
auszuwählen.
In jeder Folge diskutiert Infektiologe Prof. Mathias Pletz aus Jena mit einem Expertengast einen klinischen Schwerpunkt – fundiert und dennoch in entspannter Gesprächsatmosphäre.
Besonders praktisch: Für jede Folge können Sie bis zu einem Jahr nach Veröffentlichung CME-Punkte sammeln, indem Sie die zugehörigen CME-Fragen beantworten.
In der aktuellen Folge ist Prof. Dr. Christian Gille aus Heidelberg zu Gast. Gemeinsam widmen sie sich dem Thema Neugeborenensepsis.
18.06.2025
Rückkehr eliminierter Infektionskrankheiten bei sinkenden Impfraten in den USA
Die flächendeckende Durchführung von Routineimpfungen im Kindesalter hat in den USA zur Eliminierung verschiedener Infektionskrankheiten geführt. Allerdings sind die Impfraten in den letzten Jahren rückläufig, und es gibt politische Debatten über eine Reduzierung des Kinderimpfplans. Eine aktuelle Simulationsstudie untersuchte nun die möglichen Folgen sinkender Impfraten für die Wiederkehr von Masern, Röteln, Poliomyelitis und Diphtherie.
Die Modellierung erfolgte für alle 50 US-Bundesstaaten und den District of Columbia über einen Zeitraum von 25 Jahren. Dabei wurden Daten zur Demografie, Bevölkerungsimmunität und zum Importrisiko für die jeweiligen Infektionskrankheiten berücksichtigt. Mit den aktuellen bundesstaatlichen Impfraten prognostiziert das Modell, dass Masern in 83 % der Simulationen nach durchschnittlich 20,9 Jahren wieder endemisch werden könnten. Dabei würden über 25 Jahre schätzungsweise 851.300 Masernfälle (95-%-Konfidenzintervall [KI] 381.300 bis 1,3 Millionen Fälle) auftreten. Bei einem 10-prozentigen Rückgang der Masern-Mumps-Röteln-Impfung rechnet das Modell mit 11,1 Millionen Masernfällen (95-%-KI 10,1 bis 12,1 Millionen) über 25 Jahre. Bei einer 5-prozentigen Steigerung der Impfrate würden dagegen nur etwa 5800 Fälle (95-%-KI 3100 bis 19.400) erwartet.
Bei einem Rückgang der Routineimpfungen um 50 % prognostiziert das Modell über 25 Jahre 51,2 Millionen Masernfälle (95-%-KI 49,7 bis 52,5 Millionen), 9,9 Millionen Rötelnfälle (95-%-KI 6,4 bis 13,0 Millionen), 4,3 Millionen Poliomyelitisfälle (95-%-KI 4 Fälle bis 21,5 Millionen) und 197 Diphtheriefälle (95-%-KI 1 bis 1000). Dies würde zu schwerwiegenden Komplikationen führen: 51.200 Fälle (95-%-KI 49.600 bis 52.600) mit neurologischen Folgeerscheinungen nach Masern, 10.700 Fälle (95-%-KI 6700 bis 14.600) mit kongenitalem Rötelnsyndrom, 5400 Fälle (95-%-KI 0 bis 26.300) mit paralytischer Poliomyelitis sowie insgesamt 10,3 Millionen Krankenhauseinweisungen (95-%-KI 9,9 bis 10,5 Millionen) und 159.200 Todesfälle (95-%-KI 151.200 bis 164.700).
In diesem Szenario würden Masern nach durchschnittlich 4,9 Jahren (95-%-KI 4,3 bis 5,6 Jahre) endemisch werden, Röteln nach 18,1 Jahren (95-%-KI 17,0 bis 19,6 Jahre). Poliomyelitis würde in etwa der Hälfte der Simulationen (56 %) nach durchschnittlich 19,6 Jahren (95-%-KI 14,0 bis 24,7 Jahre) endemisch. Die Wahrscheinlichkeit einer endemischen Übertragung von Diphtherie wäre selbst bei diesem starken Impfrückgang gering.
Die Modellierung zeigte deutliche regionale Unterschiede beim Risiko für Ausbrüche und die Rückkehr zu einer endemischen Übertragung. Texas wies dabei das höchste Risiko für Masernausbrüche auf.
Die Ergebnisse waren robust in verschiedenen Sensitivitätsanalysen, wobei die Basisreproduktionszahl und die Importrate der Erreger den größten Einfluss auf die Resultate hatten.
Folgerung der Autoren
Basierend auf den Schätzungen dieser Modellierungsstudie würden sinkende Impfraten im Kindesalter die Häufigkeit und das Ausmaß von Ausbrüchen zuvor eliminierter impfpräventabler
Infektionskrankheiten erhöhen und schließlich zu deren Rückkehr auf ein endemisches Niveau führen. Der Zeitpunkt und die kritische Schwelle für die Rückkehr zur Endemizität unterscheiden sich dabei
erheblich je nach Krankheit, wobei Masern wahrscheinlich als erste Erkrankung zurückkehren und dies möglicherweise bereits unter den aktuellen Impfraten geschehen könnte, wenn keine Verbesserung der
Impfabdeckung und der Reaktion des öffentlichen Gesundheitswesens erfolgt. Diese Erkenntnisse unterstreichen die Notwendigkeit, Routineimpfungen im Kindesalter mit hoher Durchimpfungsrate
fortzusetzen, um ein Wiederauftreten impfpräventabler Infektionskrankheiten in den USA zu verhindern.
Kommentar der Herausgeber
Diese Modellrechnungen basieren auf konstanten Impfraten. Dagegen ist jedoch ebenso denkbar, dass ein gehäuftes Wiederauftreten dieser Erkrankungen die Gefährlichkeit dieser in weiten Kreisen der
Bevölkerung vergessenen und verharmlosten Infektionen wieder in Erinnerung rufen und Impfraten auch konsekutiv ansteigen könnten. Betroffen wären insbesondere Kinder, Alte und Immunsupprimierte.
Allerdings sollten alle Anstrengungen unternommen werden, dass es gar nicht erst zu einem weiteren Abfall der Impfraten kommt.
Kiang, M. V. et al. Modeling Reemergence of Vaccine-Eliminated Infectious Diseases Under Declining Vaccination in the US. JAMA. 2025; published online April 24, 2025.
doi: 10.1001/jama.2025.6495
21.05.2025
WHO aktualisiert Liste der prioritären antibiotikaresistenten Erreger für 2024
Die Antibiotikaresistenz stellt eine der größten Herausforderungen für die globale Gesundheit dar. Im Jahr 2019 wurden schätzungsweise 4,95 Millionen Todesfälle mit antibiotikaresistenten Erregern in Verbindung gebracht, wobei Länder mit niedrigem und mittlerem Einkommen überproportional betroffen waren.
Die Weltgesundheitsorganisation (WHO) hat nun ihre „Bacterial Priority Pathogens List" (BPPL) für 2024 aktualisiert. Diese Liste, die erstmals 2017 veröffentlicht wurde, dient als Orientierungshilfe für Investitionen in Forschung und Entwicklung sowie als Grundlage für Maßnahmen zur Überwachung und Kontrolle von Antibiotikaresistenzen. Die aktualisierte Liste umfasst 15 Familien antibiotikaresistenter Erreger, die in die Kategorien „kritisch", „hoch" und „mittel" eingestuft wurden.
In der Kategorie der kritischen Priorität finden sich Gram-negative Bakterien, die gegen Reserveantibiotika resistent sind. Dazu gehören Acinetobacter baumannii und verschiedene Erreger aus der Ordnung der Enterobacterales sowie Rifampicin-resistente Mycobacterium tuberculosis. Diese Einstufung basiert auf ihrer Fähigkeit, Resistenzgene zu übertragen, der Schwere der von ihnen verursachten Infektionen und Erkrankungen sowie ihrer erheblichen globalen Krankheitslast, insbesondere in Ländern mit niedrigem und mittlerem Einkommen.
Die Aufnahme von Salmonella und Shigella in die Kategorie hoher Priorität spiegelt ihre zunehmende Resistenz gegen bestehende Behandlungen und die hohe Infektionslast wider, die mit diesen Erregern verbunden ist.
Zu den weiteren Erregern mit hoher Priorität gehören antibiotikaresistente Pseudomonas aeruginosa und Staphylococcus aureus aufgrund ihrer globalen Bedrohung, insbesondere im Gesundheitswesen. Auch Neisseria gonorrhoeae wurde in diese Kategorie aufgenommen, da multiresistente Stämme die Behandlungsoptionen einschränken. Ein weiterer Erreger von besonderer Bedeutung für die öffentliche Gesundheit ist der antibiotikaresistente Enterococcus faecium, der aufgrund seiner Fähigkeit, Resistenzelemente über das gesamte One-Health-Spektrum zu übertragen, als besonders wichtig eingestuft wird.
In der Kategorie mittlerer Priorität listet die BPPL 2024 Streptokokken der Gruppen A und B, Streptococcus pneumoniae und Haemophilus influenzae auf. Dies weist auf einen dringenden Handlungsbedarf hin, insbesondere im Hinblick auf vulnerable Bevölkerungsgruppen in ressourcenarmen Umgebungen.
Die Bekämpfung der Antibiotikaresistenz im Gesundheitssektor erfordert globale Anstrengungen in mehreren Schlüsselbereichen: robuste Maßnahmen zur Infektionsprävention und -kontrolle, die Sicherstellung eines gerechten Zugangs zu Diagnostik und Behandlung, eine aufmerksame Überwachung zur Erkennung neuer Resistenzentwicklungen sowie erhebliche Investitionen in Forschung und Entwicklung für neue Medikamente, Diagnostika und Präventionstools.
Mehr Informationen zur WHO Bacterial Priority Pathogens List, 2024
21.05.2025
INFEKTIO_Podcast | Vom Furunkel zur Fasziitis – Haut- und Weichgewebeinfektionen
Der Podcast consilium infectiorum bietet medizinischem Fachpersonal praxisrelevante Themen der klinischen Infektiologie und unterstützt dabei, evidenzbasierte Behandlungsoptionen für Patienten
auszuwählen.
In jeder Folge diskutiert Infektiologe Prof. Mathias Pletz aus Jena mit einem Expertengast einen klinischen Schwerpunkt – fundiert und dennoch in entspannter Gesprächsatmosphäre.
Besonders praktisch: Für jede Folge können Sie bis zu einem Jahr nach Veröffentlichung CME-Punkte sammeln, indem Sie die zugehörigen CME-Fragen beantworten.
In der aktuellen Folge ist Prof. Dr. Christian Eckmann aus Hann Münden zu Gast. Gemeinsam widmen sie sich dem Thema Haut- und Weichgewebeinfektionen.
21.05.2025
Gepotidacin zur Behandlung unkomplizierter Harnwegsinfekte in den USA zugelassen
Die US-amerikanische Food and Drug Administration (FDA) hat unter dem Namen Blujepa das neue orale Antibiotikum Gepotidacin zur Behandlung von Frauen und Mädchen ab 12 Jahren mit unkomplizierten Harnwegsinfektionen, verursacht durch Escherichia coli, Klebsiella pneumoniae, Citrobacter freundii complex, Staphylococcus saprophyticus oder Enterococcus faecalis, zugelassen [1].
Schätzungen zufolge sind 50-60 % der erwachsenen Frauen in ihrem Leben mindestens einmal von einer Harnwegsinfektion betroffen, die in den allermeisten Fällen durch E. coli verursacht wird [2]. Wenn im Harntrakt keine relevanten, funktionellen oder anatomischen Anomalien, keine relevanten Nierenfunktionsstörungen und keine relevanten Vor- bzw. Begleiterkrankungen vorliegen, die eine Harnwegsinfektion bzw. gravierende Komplikationen begünstigen, wird die Harnwegsinfektion als unkompliziert eingestuft [3].
Gepotidacin ist ein neuartiges Antibiotikum mit Triazaacenaphthylen-Struktur und damit der erste Vertreter einer neuen Wirkstoffklasse. Gepotidacin wirkt bakterizid, indem es sowohl die DNA-Gyrase als auch die Topoisomerase IV inhibiert und damit die bakterielle DNA-Replikation hemmt [1,4]. Im Unterschied zu den Fluorchinolonen interagiert Gepotidacin mit anderen Bindungsstellen auf den beiden Typ-II-Topoisomerasen und induziert dabei enzymvermittelte Einzelstrang- statt Doppelstrang-DNA-Brüche [4].
Blujepa enthält 750 mg Gepotidacin (als Gepotidacin-Mesylat) pro Tablette, die Einnahme erfolgt zweimal täglich über 5 Tage zu den Mahlzeiten, um das Risiko für gastrointestinale Beschwerden zu minimieren [1]. Eine Dosisanpassung bei leichter bis moderater Nieren- oder Leberfunktionseinschränkung ist nicht erforderlich.
Die Wirksamkeit und Sicherheit von Gepotidacin wurden in zwei randomisierten, doppelblinden Phase-III-Nichtunterlegenheitsstudien (EAGLE-2 und EAGLE-3) an nicht-schwangeren Frauen und Mädchen ab
12 Jahren (mind. 40 kg Körpergewicht) untersucht [5]. Eingeschlossen wurden Patientinnen mit mindestens zwei Symptomen eines unkomplizierten Harnwegsinfekts (Dysurie, Häufigkeit, Dringlichkeit,
Unterleibsschmerzen) sowie dem Nachweis von Nitrit im Urin und/oder dem Vorliegen einer Pyurie. Die Patientinnen erhielten über die Dauer von fünf Tagen entweder zweimal täglich 750 mg Gepotidacin
als Tablette oder zweimal täglich 100 mg Nitrofurantoin als Kapsel (25 % Nitrofurantoin makrokristallin, 75 % Nitrofurantoin-Monohydrat), sowie zusätzlich die jeweils andere Darreichungsform als
Placebo zur besseren Verblindung. Der kombinierte primäre Endpunkt galt als erreicht, wenn an Tag 10 (bis 13) sowohl eine klinische Heilung der Symptome als auch eine mikrobiologische
Eradikation
(< 10³ koloniebildende Einheiten (KBE)/ml im Urin) erreicht wurde.
In der Zwischenanalyse wurden Patientinnen berücksichtigt, bei denen vollständige mikrobiologische Daten verfügbar waren und ein Nitrofurantoin-sensibler Keim zu Studienbeginn nachgewiesen werden konnte. In EAGLE-2 erreichten unter diesen Bedingungen 50,6 % (162/320) der Patientinnen unter Gepotidacin und 47,0 % (135/287) der Patientinnen unter Nitrofurantoin den kombinierten primären Endpunkt (adjustierte Differenz 4,3 %; 95 %-Konfidenzintervall (KI) –3,6 bis 12,1). In EAGLE-3 führte die Behandlung mit Gepotidacin bei 58,5 % (162/277) und mit Nitrofurantoin bei 43,6 % (115/264) der Patientinnen zum Therapieerfolg (adjustierte Differenz 14,6 %; 95 %-KI 6,4 bis 22,8). Damit war Gepotidacin in beiden Studien einer Therapie mit Nitrofurantoin nicht unterlegen, in EAGLE-3 war Gepotidacin der Behandlung mit Nitrofurantoin zudem überlegen. Gepotidacin zeigte dabei auch numerisch eine bessere Wirksamkeit gegenüber arzneimittelresistenten E. coli-Isolaten, die Extended Spectrum β-Lactamasen (ESBL) exprimierten bzw. fluorchinolon- oder multiresistent waren.
Die häufigsten unerwünschten Nebenwirkungen von Gepotidacin sind Diarrhö (16 %), Übelkeit (9 %) und Bauchschmerzen (4 %) [1]. Außerdem kann unter Gepotidacin eine dosisabhängige Verlängerung der QTc-Zeit auftreten.
Gepotidacin ist nach langer Zeit der erste Vertreter einer neuen Antibiotikaklasse. Der Wirkmechanismus ist ähnlich den Fluorchinolonen, wobei Gepotidacin auch bei einer Fluorchinolon-Resistenz noch wirksam sein kann. Angesichts des Auftretens von Antibiotikaresistenzen könnte Gepotidacin eine zusätzliche orale Therapieoption für die Behandlung unkomplizierter Harnwegsinfekte sein, die durch multiresistente E. coli verursacht werden. Ob sich die aufgrund des dualen Wirkmechanismus bestehende Hoffnung auf ein geringeres Potential für eine Resistenzentwicklung erfüllt, wird sich erst im Zuge der breiten Anwendung zeigen. Derzeit wird außerdem die Wirksamkeit von Gepotidacin zur Behandlung von urogenitalen Infektionen durch Neisseria gonorrhoeae, einschließlich multiresistenter Stämme, untersucht.
1 U.S. Food & Drug Administration (FDA). Blujepa (Gepotidacin): Full Prescribing Information. Mar 2025. URL: https://www.accessdata.fda.gov/drugsatfda_docs/label/2025/218230s000lbl.pdf [13.04.2025]
2 Medina M., Castillo-Pino E. An introduction to the epidemiology and burden of urinary tract infections. Ther Adv Urol. 2019; 11:3-7. doi: 10.1177/1756287219832172
3 Deutsche Gesellschaft für Urologie e. V. S3 Leitlinie: Epidemiologie, Diagnostik, Therapie, Prävention und Management unkomplizierter, bakterieller, ambulant erworbener Harnwegsinfektionen bei Erwachsenen – Aktualisierung 2024. Langversion, 3.0, AWMF Registernummer: 043/044. URL: https://register.awmf.org/de/leitlinien/detail/043-044 [13.04.2025]
4 Watkins R. et al. Gepotidacin: a novel, oral, ‘first-in-class’ triazaacenaphthylene antibiotic for the treatment of uncomplicated urinary tract infections and urogenital gonorrhoea. J Antimicrob Chemother. 2023; 78(5):1137-1142. doi: 10.1093/jac/dkad060
5 Wagenlehner F. et al. Oral gepotidacin versus nitrofurantoin in patients with uncomplicated urinary tract infection (EAGLE-2 and EAGLE-3): two randomised, controlled, double-blind, double-dummy, phase 3, non-inferiority trials. The Lancet. 2024; 403(10428):741-755. doi: 10.1016/S0140-6736(23)02196-7
25.04.2025
Weltweiter Tag der Händehygiene 2025: Es könnten Handschuhe sein - aber es ist immer Händehygiene
Eine der zentralen Maßnahmen zur Vermeidung von Infektionen ist die gründliche Händehygiene. Um auf ihre entscheidende Rolle aufmerksam zu machen, wird jedes Jahr am 5. Mai der Internationale Tag der Händehygiene begangen. Das Datum – der 5.5. – steht symbolisch für die fünf Finger jeder Hand.
Die Weltgesundheitsorganisation (WHO) setzt dieses Jahr mit dem Welttag der Händehygiene 2025 einen wichtigen Fokus auf die korrekte Verwendung von medizinischen Handschuhen und Händehygiene im
Gesundheitswesen. Nach 17 Jahren globaler Kampagnenarbeit steht nun die Botschaft im Mittelpunkt: Medizinische Handschuhe können die Händehygiene nicht ersetzen. Sie können ebenso leicht kontaminiert
werden wie bloße Hände und bieten keinen hundertprozentigen Schutz. Nach jedem Ausziehen der Handschuhe muss eine Händedesinfektion gemäß der "5 Momente der Händehygiene" erfolgen.
Ein wichtiger Aspekt ist auch der Umweltschutz: Der übermäßige Handschuhverbrauch trägt erheblich zum medizinischen Abfall bei. Zwischen Februar und August 2020 entstanden durch 3 Milliarden
Einheiten persönlicher Schutzausrüstung täglich 591 Tonnen Abfall – größtenteils Handschuhe.
Bis 2026 soll die Überwachung der Händehygiene-Compliance als nationaler Schlüsselindikator in allen Referenzkrankenhäusern etabliert werden. Aktuell setzen dies bereits 68% der Länder um.
Die WHO ruft alle Länder und Gesundheitseinrichtungen dazu auf, optimale Händehygienepraktiken und angemessene Handschuhverwendung zu priorisieren.
Alle Details zur globalen WHO-Kampagne und den geplanten Maßnahmen finden Sie hier.
25.04.2025
Europäische Impfwoche 2025: Impfungen für alle sind menschlich möglich
Die Weltgesundheitsorganisation (WHO) richtet auch 2025 wieder die Europäische Impfwoche (European Immunization Week, EIW) in der Europäischen Region aus, um die zentrale Bedeutung von Impfungen für den Gesundheitsschutz hervorzuheben. Der Fokus der jährlich stattfindenden Kampagne, die üblicherweise in der letzten Aprilwoche und dieses Jahr vom 27. April bis zum 3. Mai durchgeführt wird, liegt dabei auf dem wichtigen Ziel, eine gleichmäßig hohe Durchimpfungsrate in allen Bevölkerungsgruppen zu erreichen und dadurch Krankheitsausbrüche effektiv zu verhindern. Unter dem Motto "Impfungen für alle sind menschlich möglich" setzt die EIW ein deutliches Zeichen für einen inklusiven Zugang zu Impfangeboten.
Die diesjährige Kampagne verfolgt einen ganzheitlichen Ansatz: Neben der breiten Streuung von Informationen über Impfstoffe wird besonders betont, dass bei den Bemühungen um einen umfassenden
Gesundheitsschutz durch Impfungen niemand zurückgelassen werden darf.
Ein besonderer Schwerpunkt liegt auf der verstärkten Zusammenarbeit mit jungen medizinischen Fachkräften und Jugendorganisationen, die sich für Impfkampagnen engagieren. Damit baut die WHO gezielt
auf bestehende und neue Partnerschaften, um die jüngere Generation als wichtige Multiplikatoren für das Thema Impfen zu gewinnen.
25.04.2025
INFEKTIO_Podcast | Volle Dosis? Antibiotika-Therapie auf der Intensivstation
Der Podcast consilium infectiorum bietet medizinischem Fachpersonal praxisrelevante Themen der klinischen Infektiologie und unterstützt dabei, evidenzbasierte Behandlungsoptionen für
Patienten auszuwählen.
In jeder Folge diskutiert Infektiologe Prof. Mathias Pletz aus Jena mit einem Expertengast einen klinischen Schwerpunkt – fundiert und dennoch in entspannter Gesprächsatmosphäre.
Besonders praktisch: Für jede Folge können Sie bis zu einem Jahr nach Veröffentlichung CME-Punkte sammeln, indem Sie die zugehörigen CME-Fragen beantworten.
In der aktuellen Folge ist Prof. Dr. Jan Kielstein aus Berlin zu Gast. Gemeinsam widmen sie sich der Antibiotika-Therapie auf der Intensivstation.
25.04.2025
Kurze Behandlungsstrategien für Rifampin-sensible Tuberkulose: Wirksamkeit und Verträglichkeit
Tuberkulose wird in der Regel mit einem 6-monatigen Rifampin-Schema behandelt. Ob eine Strategie mit einer kürzeren Erstbehandlung zu ähnlichen Ergebnissen führen kann, ist unklar.
In der nachfolgenden Studie wurden Teilnehmer mit Rifampin-empfänglicher Lungentuberkulose nach dem Zufallsprinzip entweder einer Standardbehandlung (Rifampin und Isoniazid für 24 Wochen mit
Pyrazinamid und Ethambutol für die ersten 8 Wochen) oder einer Strategie zugewiesen, die eine Anfangsbehandlung mit einem 8-Wochen-Schema oder länger bei persistierender klinischer Erkrankung einer
verlängerten Behandlung umfasste. Es gab hier vier Strategien mit unterschiedlichen Anfangstherapien; die Nichtunterlegenheit wurde in den beiden Strategien mit vollständiger Rekrutierung analysiert,
die Anfangstherapien mit hochdosiertem Rifampin-Linezolid und Bedaquilin-Linezolid (jeweils mit Isoniazid, Pyrazinamid und Ethambutol) erhielten. Der primäre Endpunkt war eine Kombination aus Tod,
fortdauernder Behandlung oder aktiver Erkrankung in Woche 96. Die Nichtunterlegenheitsmarge betrug 12 Prozentpunkte.
Es wurden 674 Teilnehmer in der Intention-to-Treat-Population eingeschlossen. Ein Ereignis mit primärem Endpunkt trat bei 7 der 181 Teilnehmer (3,9 %) in der Standardbehandlungsgruppe auf, verglichen
mit 21 der 184 Teilnehmer (11,4 %) in der Gruppe mit einem anfänglichen Rifampin-Linezolid-Schema und 11 der 189 Teilnehmer (5,8 %) in der Gruppe mit einem anfänglichen Bedaquilin-Linzolid-Schema.
Die mittlere Gesamtbehandlungsdauer betrug 180 Tage in der Standardbehandlungsgruppe, 106 Tage in der Rifampin-Linezolid-Strategiegruppe und 85 Tage in der
Bedaquilin-Linezolid-Strategiegruppe.
Die Inzidenz von unerwünschten Ereignissen des Grades 3 oder 4, von schwerwiegenden unerwünschten Ereignissen und von Todesfällen unterschied sich nicht signifikant zwischen der
Standardbehandlungsgruppe und den beiden Strategiegruppen mit vollständiger Rekrutierung. Fast alle Rückfälle wurden als Schweregrad 1 oder 2 eingestuft; ein Teilnehmer in der
Standardbehandlungsgruppe, fünf in der Rifampin-Linezolid Gruppe und einer in der Bedaquilin-Linezolid Gruppe hatten ein unerwünschtes Ereignis des Schweregrads 3 oder 4, in Form eines Rückfall oder
einer erneuten Therapie.
In einer weiteren Übersichtsarbeit und Meta-Analyse wurden Sicherheitsdaten zu 591 Patienten, die 8 unterschiedliche Therapieregime mit Bedaquilin, Pretomanid und Linezolid (BPaL) erhalten hatten,
untersucht. Bei Patienten, die eine Tagesdosis von 1200 mg Linezolid erhalten hatten, erlitten 35 % ein unerwünschtes Ereignis des Grads 3-4 aber nur 22 % von den Patienten mit einer
Linezolid-Tagesdosis von 600 mg. Diese niedrigere und besser verträgliche Dosis wurde auch in der oben genannten randomisierten Studie verwendet.
Folgerung der Autoren
Die Studie zeigt, dass eine Strategie mit initialer Behandlung mit einem 8-wöchigen Bedaquilin-Linezolid-Regime nicht unterlegen war im Vergleich zur Standardbehandlung und mit einer kürzeren
Gesamtbehandlungsdauer verbunden war. Die Sicherheit war vergleichbar in den drei Gruppen. Dies wurde inzwischen in verschiedenen Studien gezeigt und stellt somit eine vielversprechende Alternative
zur Standardbehandlung von Tuberkulose dar.
Kommentar der Herausgeber
Es ist sehr zu begrüßen, dass immer kürzere Therapieregime für Tuberkulose getestet und für sicher und wirksam befunden werden. Leider haben diese aber auch Probleme mit unerwünschten Ereignissen,
insbesondere mit Linezolid. Daher sind Daten zur ähnlichen Wirksamkeit bei besserer Verträglichkeit einer niedrigeren Tagesdosis von 600 mg erfreulich. Gleichzeitig muss jedoch bedacht werden, dass
gerade Bedaquilin und Linezolid entscheidende Therapiepfeiler von BPaL darstellen, welches die Therapie der multiresistenten (MDR) Tuberkulose durch erheblich verkürzte Therapiedauer und gute
Wirksamkeit revolutioniert hat. Bei zunehmender und breiter Anwendung dieser beiden Medikamente für Tuberkuloseformen, die potente und gut verträgliche Alternativen in Form der bisherigen 6-monatigen
Standardtherapie aufweisen, ist ein rascher Verlust durch Resistenzentwicklung für viel dringlichere Anwendungen bei der MDR-TB zu befürchten.
Paton, N. I. et al. Treatment Strategy for Rifampin-Susceptible Tuberculosis. N Engl J Med. 2023; 388(10):873-887. doi: 10.1056/NEJMoa2212537
Hasan, T. et al. The Safety and Tolerability of Linezolid in Novel Short-Course Regimens Containing Bedaquiline, Pretomanid, and Linezolid to Treat Rifampicin-Resistant Tuberculosis: An Individual Patient Data Meta-analysis. Clin Inf Dis. 2024; 78(3):730-741. doi: 10.1093/cid/ciad653
12.03.2025
Welt-Tuberkulose-Tag 2025
Tuberkulose (TB) bleibt eine der größten Herausforderungen für die globale Gesundheit. Etwa ein Viertel der Weltbevölkerung ist mit dem Erreger Mycobacterium tuberculosis infiziert. Trotz eines Rückgangs der Neuerkrankungen in der WHO-Region Europa um durchschnittlich 4,3 % pro Jahr zwischen 2011 und 2015 stellt die Krankheit weiterhin eine erhebliche Bedrohung dar, insbesondere durch multiresistente TB. Neun der 30 am stärksten betroffenen Länder weltweit befinden sich in dieser Region.
TB wird über die Luft übertragen, wobei eine unbehandelte Person mit aktiver TB durchschnittlich 10–15 Menschen pro Jahr anstecken kann. Eine frühzeitige Diagnose und eine wirksame Behandlung sind entscheidend, um die weitere Ausbreitung zu verhindern. Die WHO verfolgt das Ziel, TB weltweit zu beenden. Der TB-Aktionsplan für die WHO-Region Europa 2016–2020 dient dabei als wichtigstes Leitinstrument, um Fortschritte im Einklang mit der globalen End-TB-Strategie 2016–2035, den Zielen für nachhaltige Entwicklung und dem europäischen Gesundheitsrahmenkonzept Health 2020 zu erzielen.
Aus diesem Grund steht der Welt-Tuberkulose-Tag 2025 unter dem Motto „Ja! Wir können die Tuberkulose beenden: Bekennen, investieren, umsetzen“. Dieses Thema betont die Notwendigkeit, sich zur
Bekämpfung der Krankheit zu verpflichten, Investitionen zu tätigen und konkrete Maßnahmen zur endgültigen Eliminierung umzusetzen.
Die WHO ruft Regierungen, Gesundheitsdienstleister und Gemeinschaften zur Zusammenarbeit auf. Notwendig sind verbesserte Früherkennung, neue Diagnosetests, Medikamente sowie verstärkte Forschung. Der
Welt-Tuberkulose-Tag soll Bewusstsein schaffen, Engagement fördern und den gemeinsamen Kampf gegen TB stärken.
Weitere Informationen zum Aktionsplan, zur Kampagne und der entsprechenden Webinar-Veranstaltung finden Sie untenstehend.
12.03.2025
Veranstaltungen der Paul-Ehrlich-Gesellschaft
Frühjahrstagung der Sektion "Antimykotische Therapie"
Was? Update Antimykotika & Diagnostik
Wo? Haus der Technik, Essen
Wann? 04.-05.04.2025
Frühjahrstagung der PEG
Was? Update Infektionsmedizin (u.a. Leitlinien, ABS, Impfung & antivirale Therapie)
Wo? Volkshaus Jena
Wann? 28.-29.04.2025
12.03.2025
INFEKTIO_Podcast | Besserwisser mit Antibiotika – Etablierung von ABS-Strukturen
Der Podcast consilium infectiorum bietet medizinischem Fachpersonal praxisrelevante Themen der klinischen Infektiologie und unterstützt dabei, evidenzbasierte Behandlungsoptionen für
Patienten auszuwählen.
In jeder Folge diskutiert Infektiologe Prof. Mathias Pletz aus Jena mit einem Expertengast einen klinischen Schwerpunkt – fundiert und dennoch in entspannter Gesprächsatmosphäre.
Besonders praktisch: Für jede Folge können Sie bis zu einem Jahr nach Veröffentlichung CME-Punkte sammeln, indem Sie die zugehörigen CME-Fragen beantworten.
In der aktuellen Folge ist Prof. Dr. Irit Nachtigall aus Berlin zu Gast. Gemeinsam widmen sie sich der Etablierung von ABS-Strukturen
12.03.2025
Zulassungsempfehlung für neuen Impfstoff gegen Chikungunya-Virus
Der Ausschuss für Humanarzneimittel (CHMP) bei der europäischen Arzneimittelbehörde EMA empfiehlt nach seiner Sitzung am 30. Januar 2025 die Zulassungserteilung für Vimkunya, einen neuen Impfstoff gegen das Chikungunya-Virus (CHIKV) [1].
Das Chikungunya-Virus ist in den (sub-)tropischen Regionen Amerikas, Afrikas und Asiens endemisch. In Frankreich wurde 2024 der einzige lokal erworbene Fall auf dem europäischen Festland berichtet (ECDC). Die Übertragung erfolgt durch den Stich einer infizierten Aedes-Mücke und führt nach einer Inkubationszeit von etwa 2-12 Tagen u.a. zu einem plötzlichen Auftreten von hohem Fieber, starken Gelenkschmerzen an Händen und Füßen sowie Hautausschlag. Auch wenn schwere Verläufe selten sind, können neurologische Komplikationen und Todesfälle auftreten. Besonders belastend ist der häufig über mehrere Monate bis sogar Jahre andauernde Genesungsprozess, in denen die Betroffenen von wiederkehrenden Gelenkschmerzen begleitet werden, die nicht selten in einer chronischen Arthritis münden können [2].
Vimkunya ist ein auf virusähnlichen Partikeln (VLP) basierender Totimpfstoff. Er enthält das rekombinant hergestellte Kapsidprotein (C) sowie die Hüllproteine E1 und E2, abgeleitet vom CHIKV-Senegal-Stamm 37997 [1]. Durch eine spontane Zusammenlagerung dieser Strukturproteine, zu den sogenannten virusähnlichen Partikeln, wird die Morphologie des Virus imitiert, was nach der Injektion zu einer effektiven Stimulation der angeborenen und adaptiven Immunantwort führt [3]. Die VLPs sind dabei nicht replikationsfähig, da sie kein virales Erbgut enthalten. Zur Verstärkung der Immunantwort sind die VLPs außerdem an Aluminiumhydroxid als Adjuvans adsorbiert. Der adjuvantierte Totimpfstoff soll als Suspension zur Injektion in einer Fertigspritze erhältlich sein und kann zur aktiven Immunisierung von Personen ab 12 Jahren eingesetzt werden.
Die Immunogenität und Sicherheit des Impfstoffes wurden in zwei randomisierten, doppelblinden und kontrollierten Phase-III-Studien untersucht [4]. Die 3254 eingeschlossenen Personen im Alter zwischen 12 und 65 Jahren erhielten entweder eine Einzeldosis Vimkunya oder eine intramuskuläre Injektion mit Placebo. Die Impfung mit Vimkunya zeigte eine Seroresponse-Rate von 98 % (1 % unter Placebo) an Tag 22, die nach etwa 6 Monaten noch bei 86 % lag. In der Studie an 413 Personen im Alter 65 Jahren und älter war die durch Vimkunya-induzierte Seroresponse-Rate an Tag 22 mit 87 % im Vergleich zu der jüngeren Altersgruppe niedriger. In beiden Studien waren die schützenden Antikörpertiter bei einem Großteil der geimpften Personen bereits an Tag 15 erreicht (Seroresponse-Rate 97 % bzw. 82 %). Die unerwünschten Wirkungen nach der Impfung waren meist mild bis moderat, am häufigsten traten Schmerzen an der Injektionsstelle, Müdigkeit, Kopfschmerzen und Myalgie auf [1,4].
Folgt die Europäische Kommission der Empfehlung des CHMP und wird Vimkunya in Europa zugelassen, wäre es bereits der zweite Impfstoff gegen das Chikungunya-Virus. Mit der Zulassung von Ixchiq im Juni 2024 bestand erstmals die Möglichkeit der aktiven Immunisierung gegen CHIKV. Ixchiq ist ein Lebendimpfstoff und enthält replikationsfähige, abgeschwächte Chikungunya-Viren, mit denen Personen ab 18 Jahren geimpft werden können. Die Impfung mit Ixchiq wird derzeit in Österreich für Reisende in Endemiegebiete empfohlen, in der Schweiz ist der Impfstoff nicht zugelassen [5,6]. Eine Impfempfehlung für Reisende aus Deutschland wird derzeit noch durch die Ständige Impfkommission am Robert Koch Institut (STIKO) erarbeitet.
1 European Medicines Agency (EMA). Vimkunya - summary of opinion. EMA/CHMP/552510/2024; published online Jan 31, 2025. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-vimkunya_en.pdf
2 Auswärtiges Amt. Chikungunyafieber. Stand 20.12.2024. URL:
https://www.auswaertiges-amt.de/de/ReiseUndSicherheit/reise-gesundheit/chikungunyafieber/2562870 [08.02.2025]
3 Klausberger, M. et al. Virusähnliche Partikel – Impfstoffe, die den Eindringling imitieren. Biospektrum. 2024; 30(1):66–69. doi: 10.1007/s12268-024-2112-2
4 Richardson, J. S. et al. Safety and Immunogenicity of an Adjuvanted Chikungunya Virus (CHIKV) Virus-like Particle (VLP) Based Vaccine in Two Pivotal Phase 3 Trials, ≥12 Years of Age. Open Forum
Infect Dis. 2023; 10(Suppl 2):S1270-S1271. doi: 10.1093/ofid/ofad500.2471
5 Bundesministerium für Soziales, Gesundheit, Pflege und Konsumentenschutz (BMSGPK). Impfplan Österreich 2024/2025, Version 1.1 vom 18.12.2024; S. 132-133. URL: https://www.sozialministerium.at/dam/jcr:7b3826a7-9eb5-4835-affd-f6e6e3f62bf4/Impfplan_Österreich_2024-2025_Version_1.1.pdf
6. Bundesamt für Gesundheit (BAG). Chikungunya-Fieber. Stand 11.09.2024. URL: https://www.bag.admin.ch/bag/de/home/krankheiten/krankheiten-im-ueberblick/chikungunya.html [09.02.2025]
12.02.2025
Update | VRE vanA ST612: Weite Verbreitung in der Schweiz bestätigt
Wir berichteten bereits im März und Juni 2024 auf Basis der bisherigen Veröffentlichungen von Swissnoso über die zunehmende Ausbreitung von Vancomycin-resistentem Enterococcus faecium (VRE) vanA ST612. Nun wurde die epidemiologische Untersuchung zur interregionalen Verbreitung abgeschlossen und bestätigt eine weitreichendere Verbreitung als ursprünglich angenommen, insbesondere in den deutschsprachigen Regionen der Schweiz.
Die hohe Detektionsrate klinischer Proben (44 %) und die niedrige Quote positiver Aufnahmescreenings im Vergleich zu klinischen Fällen deuten auf eine erhebliche unbemerkte Transmission hin.
Besonders besorgniserregend ist, dass ein nosokomiales Cluster bislang nicht unter Kontrolle gebracht werden konnte.
Handlungsempfehlungen für Gesundheitseinrichtungen
Erinnerung an die entscheidende Bedeutung der folgenden kritischen Präventions- und Kontrollmaßnahmen:
✅ Striktes Screening von Risikopatienten
✅ Einhaltung von Standard- und Kontaktisolationsmaßnahmen
✅ Systematische Kontaktuntersuchungen
✅ Meldepflicht ab drei verknüpften Fällen
Um die Ausbreitung innerhalb und zwischen Gesundheitseinrichtungen weiter einzudämmen, ist die konsequente Umsetzung der Swissnoso-Empfehlungen zur Prävention und Kontrolle multiresistenter Organismen essenziell und sollte aktiv gefördert werden.
12.02.2025
Zulassungsempfehlung für neue Arzneistoffe zur COVID-19-Prävention
Am 12. Dezember 2024 hat der Ausschuss für Humanarzneimittel (CHMP) bei der europäischen Arzneimittelbehörde EMA einen weiteren COVID-19-Impfstoff (Kostaive) für Erwachsene und einen monoklonalen Antikörper (Kavigale) zur passiven Immunisierung immungeschwächter Personen ab 12 Jahren zur Zulassung empfohlen [1,2].
Kostaive (Zapomeran)
Bei Kostaive handelt es sich um einen RNA-basierten Impfstoff. Er enthält mRNA, die für das Spike-Protein von SARS-CoV-2 codiert [1]. Im Jahr 2020 erhielt der damals weltweit erste mRNA-Impfstoff eine Zulassung zum Schutz vor Infektionen mit SARS-CoV-2. Mittlerweile existieren mehrere, variantenangepasste mRNA-Impfstoffe gegen COVID-19, kürzlich erfolgte auch die Zulassung eines mRNA-Impfstoffs zum Schutz vor Erkrankungen durch das Respiratorische Synzytial-Virus. Alle bisher verfügbaren mRNA-Vakzine basieren auf nicht-replizierender mRNA, von der eine ausreichend hohe Menge enthalten sein muss, um eine adäquate Immunantwort zu induzieren [3].
Im Gegensatz dazu enthält Kostaive eine selbst-replizierende bzw. selbst-amplifizierende mRNA (sa-mRNA), die nicht nur die genetische Information für das Spike-Protein enthält, sondern auch für die virale Replikase codiert. Nach der intramuskulären Injektion der in Lipid-Nanopartikeln verpackten sa-mRNA, erfolgt in den Zellen an der Injektionsstelle neben der Translation in das Spike-Protein auch die Bildung des Enzyms Replikase. Die Replikase vervielfacht einen Teil der mRNA in der Zielzelle, wodurch auch eine erhöhte Menge an Antigen exprimiert werden kann [1,3,4]. Die Verwendung von sa-mRNA soll die im Impfstoff enthaltene mRNA-Menge bei gleichzeitig längerer Produktion größerer Antigenmengen reduzieren. Durch die Erzeugung doppelsträngiger RNA-Intermediate während der Replikation sollen zusätzliche, das angeborene Immunsystem aktivierende Effekte und damit insgesamt Vorteile hinsichtlich der Ausbildung einer langanhaltenden Immunität erzielt werden [3,4].
Die Beurteilung der Wirksamkeit von Kostaive zur Grundimmunisierung gegen COVID-19 war Gegenstand einer randomisierten, Beobachter-verblindeten Phase-IIIb-Studie an 16.107 Personen in Vietnam [5]. Dabei erhielten die Teilnehmer entweder zwei Impfdosen Kostaive (Dosis 5 µg) oder Placebo im Abstand von 28 Tagen und es wurde die Anzahl aufgetretener COVID-19-Fälle in beiden Gruppen bis Tag 92 erfasst. Die Impfstoffwirksamkeit zum Schutz vor COVID-19 jeglicher Schwere betrugt 56,6 % (95 %-Konfidenzintervall (KI): 48,7–63,3), während sie gegen schwere Verläufe 95,3 % (95 %-KI: 80,5–98,9) erreichte, insbesondere bei Infektionen mit der Delta-Variante.
In einer weiteren randomisierten, doppelblinden Phase-III-Studie wurde die Immunogenität und Sicherheit von Kostaive (Dosis 5 µg) als vierte Boosterimpfung mit dem mRNA-Impfstoff BNT162b2 (Pfizer-BioNTech, Dosis 30 µg) verglichen [3]. Die Studie umfasste 828 erwachsene Teilnehmer in Japan, die zuvor drei Dosen eines mRNA-Impfstoffs erhalten hatten. Der primäre Endpunkt zeigte, dass die durch Kostaive induzierte Immunantwort 28 Tage nach der Impfung gegen die Wuhan-Hu-1-Variante der von BNT162b2 nicht unterlegen war, gemessen an neutralisierenden Antikörper-Titern und Seroresponse-Raten. Für die Omikron-Variante BA.4/5 zeigte Kostaive eine überlegene Immunantwort.
Nach der Impfung mit Kostaive traten in den Studien am häufigsten lokale Reaktionen wie Schmerzen an der Injektionsstelle sowie systemische unerwünschte Ereignisse wie Arthralgie, Myalgie, Kopfschmerzen, Schwindel, Müdigkeit, Schüttelfrost und Fieber auf. Die unerwünschten Ereignisse waren überwiegende mild bis moderat und vorübergehend [3,5].
Kavigale (Sipavibart)
Kavigale enthält den Wirkstoff Sipavibart, einen rekombinanten humanen monoklonalen IgG1-Antikörper mit der Fähigkeit, an die Rezeptor-Bindungsdomäne des Spike-Proteins von SARS-CoV-2 zu binden. Auf diesem Weg wird die Interaktion des Spike-Proteins mit dem Wirtsrezeptor ACE-2 gehemmt und das Eindringen des Virus verhindert. Eine so erreichte passive Immunisierung gegen SARS-CoV-2 soll Sipavibart immungeschwächte Personen ab 12 Jahren mit eingeschränkter Impfantwort vor einer symptomatischen COVID-19-Erkrankung schützen [2].
In den vergangenen Jahren der Pandemie wurden bereits monoklonale Antikörper und -kombinationen für die Therapie und die Prä-Expositionsprophylaxe (PrEP) von COVID-19 eingesetzt. Aktuellen Empfehlungen zufolge soll eine PrEP mit den SARS-CoV-2-neutralisierenden monoklonalen Antikörper Tixagevimab/Cilgavimab (Evusheld) nur noch in begründeten Einzelfällen in Betracht gezogen werden [6]. Der Grund dafür ist die fehlende (Tixagevimab) bzw. reduzierte (Cilgavimab) Neutralisationskapazität in in-vitro-Untersuchungen für mehrere derzeit zirkulierende Omikron-Sublinien infolge von Mutationen im Spike-Protein. Andere, zu Beginn der Pandemie eingesetzte, Antikörper sind auf Grund der fehlenden Wirksamkeit gar nicht mehr verfügbar oder werden nicht mehr empfohlen (z.B. Casirivimab / Imdevimab).
Da für eine wirksame PrEP bis dato Wirkstoffe mit breiter neutralisierender Aktivität gegenüber den vorherrschenden Virus-Varianten fehlten, wurde der lang wirkende monoklonale Antikörper Sipavibart entwickelt [7]. Sipavibart wurde aus den B-Zellen von rekonvaleszenten Patienten nach einer SARS-CoV-2-Infektion gewonnen. In der noch laufenden, randomisierten, doppelblinden Phase-III-Studie SUPERNOVA wurde die Wirksamkeit von Sipavibart bei 3.335 immungeschwächten Patienten ab 12 Jahren gegenüber Placebo und Tixagevimab/Cilgavimab untersucht. Die Patienten erhielten zwei intramuskuläre Injektionen mit je 300 mg Sipavibart oder der Vergleichssubstanz im Abstand von 6 Monaten. Ersten Ergebnissen zufolge reduzierte Sipavibart im Vergleich zu Tixagevimab/Cilgavimab oder Placebo signifikant die Inzidenz von symptomatischen SARS-CoV-2-Infektionen, unabhängig von der Virus-Variante (Beginn der Studie Dezember 2022). Der Effekt von Sipavibart war erwartungsgemäß größer gegen die Virus-Varianten ohne F456L-Mutation, in deren Anwesenheit bereits eine fehlende Neutralisationswirkung von Sipavibart bekannt ist.
Kavigale ist allgemein gut verträglich, die häufigsten Nebenwirkungen sind Reaktionen an der Injektions- bzw. Infusionsstelle [2].
Beide zur Zulassung empfohlenen Arzneimittel können zur Verbesserung und Erweiterung der Möglichkeiten der aktiven und passiven Immunisierung gegen COVID-19 beitragen. Die Zulassung und Genehmigung des Inverkehrbringens durch die Europäische Kommission ist noch ausstehend. Es bleibt abzuwarten, welchen Stellenwert sowohl Kostaive als auch Kavigale in der Prophylaxe von SARS-CoV-2-Infektionen durch aktuell (und zukünftig) zirkulierende Virus-Varianten einnehmen werden.
1 European Medicines Agency (EMA). Kostaive (Zapomeran) – summary of opinion. EMA/392588/2024; published online Dec 13, 2024. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-kostaive_en.pdf [05.01.2025]
2 European Medicines Agency (EMA). Kavigale (Sipavibart) – summary of opinion. EMA/CHMP/562567/2024; published online Dec 13, 2024. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-kavigale_en.pdf [05.01.2025]
3 Oda, Y. et al. Immunogenicity and safety of a booster dose of a self-amplifying RNA COVID-19 vaccine (ARCT-154) versus BNT162b2 mRNA COVID-19 vaccine: a double-blind, multicentre, randomised, controlled, phase 3, non-inferiority trial. Lancet Infect Dis. 2024; 24(4):351–60. doi: 10.1016/S1473-3099(23)00650-3
4 Schmidt, C. et al. Self-Amplifying RNA Vaccine Candidates: Alternative Platforms for mRNA Vaccine Development. Pathogens. 2023; 12(1):138. doi: 10.3390/pathogens12010138
5 Ho, N.T. et al. Safety, immunogenicity and efficacy of the self-amplifying mRNA ARCT-154 COVID-19 vaccine: pooled phase 1, 2, 3a and 3b randomized, controlled trials. Nat Commun. 2024; 15:4081. doi: 10.1038/s41467-024-47905-1
6 RKI (Robert Koch-Institut). COVID-19-Therapieempfehlungen: Interaktive Orientierungshilfe für Ärztinnen und Ärzte. Stand: 10.10.2024. URL: https://multimedia.gsb.bund.de/RKI/covid-19/dgiin_pv_covid-19-therapie/#/ [08.01.2025]
7 AstraZeneca. SUPERNOVA Phase III trial of sipavibart long-acting antibody met primary endpoints in preventing COVID-19 in immunocompromised patient population. Press Announcement; published online
May 16, 2024. URL: https://www.astrazeneca.com/media-centre/press-releases/2024/supernova-trial-met-covid-19-prevention-endpoint.html [08.01.2025]
15.01.2025
Neues Reserveantibiotikum Meropenem / Vaborbactam verfügbar
Mehr als fünf Jahre nach der Zulassung durch die europäische Arzneimittelbehörde EMA wurde Ende 2024 das Reserveantibiotikum Vaborem (vormals Vabomere) in Deutschland eingeführt. Es kombiniert Meropenem mit dem neuartigen β-Lactamase-Inhibitor (BLI) Vaborbactam zur Behandlung schwerer Infektionen wie u.a. komplizierten Harnwegsinfektionen (cUTI), komplizierten intraabdominellen Infektionen (cIAI) oder nosokomial erworbenen Pneumonien (HAP) [1].
Carbapenem-resistente Enterobacterales (CRE) zählen laut der Weltgesundheitsorganisation (WHO) aufgrund ihrer Verbreitung, Resistenz und der begrenzten Behandlungsmöglichkeiten weiterhin zu den kritischsten Gram-negativen Erregern. Eine Strategie, die durch β-Lactamase-Enzyme vermittelte Resistenz zu überwinden, ist die Kombination von β-Lactam-Antibiotika mit geeigneten BLI.
Vaborbactam, ein Nicht-β-Lactam BLI mit zyklischer Boronsäure-Struktur, hemmt insbesondere β-Lactamasen der Ambler-Klasse A (inkl. Klebsiella pneumoniae Carbapenemase, KPC) sowie AmpC [1,2]. Die Boronsäure-Struktur ist entscheidend für die Hemmung der Enzymaktivität der genannten β-Lactamasen, bei der es zur Ausbildung eines kovalenten Adduktes mit dem hydrolysestabilen Vaborbactam kommt. Gegen β-Lactamasen der Klasse B (Metallo-β-Lactamasen) und Carbapenemasen der Klasse D (z.B. OXA-48) besitzt Vaborbactam keine Aktivität.
Die Zulassung von Vaborem basiert hauptsächlich auf einer randomisierten, kontrollierten und doppelblinden Phase-III-Studie an 545 erwachsenen Patienten mit cUTI oder akuter Pyelonephritis [3]. Die Patienten wurden entweder mit Meropenem/Vaborbactam (2 g/2 g alle 8 h) oder Piperacillin/Tazobactam (4 g/0,5 g alle 8 h) über 10 Tage behandelt, mit der Möglichkeit einer Oralisierung auf Levofloxacin (500 mg alle 24 h). Gemessen am Gesamterfolg nach Ende der intravenösen Behandlung, ein kombinierter primärer Endpunkt aus klinischer Heilung und mikrobiologischer Eradikation, war Meropenem/Vaborbactam einer Therapie mit Piperacillin/Tazobactam nicht unterlegen (98,4 % vs. 94,0 %, Differenz: 4,5 % (95 %-Konfidenzintervall 0,7 – 9,1)). Informationen zur Wirksamkeit gegen CRE konnten in dieser Studie allerdings nicht geliefert werden, da fast keine Meropenem-resistenten Erreger behandelt wurden und so die Angemessenheit der Vaborbactam-Dosis nicht belegt werden konnte [4].
Eine weitere Phase-III-Studie an 77 Patienten mit schweren Infektionen (darunter cUTI, cIAI, HAP) verglich Meropenem/Vaborbactam mit der bestverfügbaren Therapie (Polymyxine, Carbapeneme, Aminoglykoside, Tigecyclin oder Ceftazidim-Avibactam) [5]. Bei den 47 Patienten mit CRE wurden höhere Heilungsraten und eine geringere Sterblichkeit unter Meropenem/Vaborbactam beobachtet. Die Studie diente jedoch nur einem deskriptiven Wirksamkeitsvergleich [4].
Die häufigsten unerwünschten Ereignisse unter der Behandlung mit Meropenem/Vaborbactam waren Kopfschmerz, Diarrhö, Phlebitis an der Infusionsstelle und Übelkeit [1].
Die Kombination des neuen BLI Vaborbactam mit Meropenem kann das Problem der Carbapenem-Resistenz nicht vollständig lösen, stellt jedoch eine willkommene Therapieoption für die Behandlung von
Infektionen durch CRE dar, insbesondere in Anwesenheit von KPC. β-Lactamasen der Klasse B und Carbapenemasen der Klasse D als weitere wichtige Ursachen
der Carbapenem-Resistenz werden allerdings nicht adressiert.
Der Stellenwert der neuen Kombination in der Praxis, insbesondere im Vergleich zu anderen Substanzen mit Wirksamkeit bei CRE (z.B. Imipenem/Cilastatin/Relebactam, Ceftazidim/Avibactam), ist vor dem
Hintergrund der begrenzten klinischen Daten noch offen. In Österreich ist Vaborem bereits seit 2019, in der Schweiz seit 2021 verfügbar.
1 Fachinformation Vaborem (Meropenem/Vaborbactam). Berlin-Chemie. Stand 07/2023. URL: https://www.medical-hub.berlin-chemie.de/sites/g/files/fugoka451/files/products/documents/147730_vaborem_fi-0723.pdf [11.01.2025]
2 Marino, A. et al. Ceftazidime/Avibactam and Meropenem/Vaborbactam for the Management of Enterobacterales Infections: A Narrative Review, Clinical Considerations, and Expert Opinion. Antibiotics.
2023; 12(10):1521. doi: 10.3390/antibiotics12101521
3 Kaye, K. S. et al. Effect of Meropenem-Vaborbactam vs Piperacillin-Tazobactam on Clinical Cure or Improvement and Microbial Eradication in Complicated Urinary Tract Infection: The TANGO I
Randomized Clinical Trial. JAMA. 2018; 319(8):788-799. doi: 10.1001/jama.2018.0438
4 European Medicines Agency (EMA). Assessment report Vabomere (Meropenem/Vaborbactam). Stand 20.09.2018. URL: https://www.ema.europa.eu/en/documents/assessment-report/vabomere-epar-public-assessment-report_en.pdf [11.01.2025]
5 Wunderink, R. G. et al. Effect and Safety of Meropenem-Vaborbactam versus Best-Available Therapy in Patients with Carbapenem-Resistant Enterobacteriaceae Infections: The TANGO II Randomized
Clinical Trial. Infect Dis Ther. 2018; 7(4):439-455. doi: 10.1007/s40121-018-0214-1
15.01.2025
Behandlungsstrategie für Rifampicin-sensible Tuberkulose
Tuberkulose wird in der Regel mit einem 6-monatigen Rifampicin-Schema behandelt. Ob eine Strategie mit einer kürzeren Erstbehandlung zu ähnlichen Ergebnissen führen kann, ist unklar.
In der nachfolgenden Studie wurden Teilnehmer mit Rifampicin-empfänglicher Lungentuberkulose nach dem Zufallsprinzip entweder einer Standardbehandlung (Rifampicin und Isoniazid für 24 Wochen mit Pyrazinamid und Ethambutol für die ersten 8 Wochen) oder einer Strategie zugewiesen, die eine Anfangsbehandlung mit einem 8-Wochen-Schema, einer verlängerten Behandlung bei persistierender klinischer Erkrankung, eine Überwachung nach der Behandlung und eine erneute Behandlung bei einem Rückfall umfasste. Es gab hier vier Strategien mit unterschiedlichen Anfangstherapien; die Nichtunterlegenheit wurde in den beiden Strategien mit vollständiger Rekrutierung analysiert, die Anfangstherapien mit hochdosiertem Rifampicin-Linezolid und Bedaquilin-Linezolid (jeweils mit Isoniazid, Pyrazinamid und Ethambutol) erhielten. Der primäre Endpunkt war eine Kombination aus Tod, fortdauernder Behandlung oder aktiver Erkrankung in Woche 96. Die Nichtunterlegenheitsmarge betrug 12 Prozentpunkte.
Es wurden 674 Teilnehmer in der Intention-to-Treat-Population eingeschlossen. Ein Ereignis mit primärem Endpunkt trat bei 7 der 181 Teilnehmer (3,9 %) in der Standardbehandlungsgruppe auf, verglichen mit 21 der 184 Teilnehmer (11,4 %) in der Strategiegruppe mit einem anfänglichen Rifampicin-Linezolid-Schema und 11 der 189 Teilnehmer (5,8 %) in der Strategiegruppe mit einem anfänglichen Bedaquilin-Linezolid-Schema. Die mittlere Gesamtbehandlungsdauer betrug 180 Tage in der Standardbehandlungsgruppe, 106 Tage in der Rifampicin-Linezolid-Strategiegruppe und 85 Tage in der Bedaquilin-Linezolid-Strategiegruppe.
Die Inzidenz von unerwünschten Ereignissen des Grades 3 oder 4, von schwerwiegenden unerwünschten Ereignissen und von Todesfällen unterschied sich nicht signifikant zwischen der
Standardbehandlungsgruppe und den beiden Strategiegruppen mit vollständiger Rekrutierung. Fast alle Rückfälle wurden als Schweregrad 1 oder 2 eingestuft; ein Teilnehmer in der
Standardbehandlungsgruppe, fünf in der Rifampicin-Linezolid-Strategiegruppe und einer in der Bedaquilin-Linezolid-Strategiegruppe hatten ein unerwünschtes Ereignis des Schweregrads 3 oder 4, in Form
eines Rückfall oder einer erneuten Therapie. Die Ergebnisse zur Therapiesicherheit in den beiden Strategiegruppen mit unvollständiger Rekrutierung waren mit denen der anderen beiden Strategiegruppen
vergleichbar. Die Häufigkeit von unerwünschten Ereignissen des Grades 3 oder 4 und von schwerwiegenden unerwünschten Ereignissen war in den drei Gruppen ähnlich.
Kommentar der Herausgeber
Die Studie zeigt, dass eine Strategie mit initialer Behandlung mit einem 8-wöchigen Bedaquilin-Linezolid-Regime nicht unterlegen war im Vergleich zur Standardbehandlung und mit einer kürzeren Gesamtbehandlungsdauer verbunden war. Die Sicherheit war vergleichbar in den drei Gruppen. Dies wurde inzwischen in verschiedenen nachfolgenden Publikationen bestätigt. Die Studie zeigt somit eine vielversprechende Alternative zur Standardbehandlung von Tuberkulose.
Paton, N. I. et al. Treatment Strategy for Rifampin-Susceptible Tuberculosis. N Engl J Med. 2023; 388(10):873-887. doi: https://doi.org/10.1056/nejmoa2212537
Hasan, T. et al. The Safety and Tolerability of Linezolid in Novel Short-Course Regimens Containing Bedaquiline, Pretomanid, and Linezolid to Treat Rifampicin-Resistant Tuberculosis: An Individual
Patient Data Meta-analysis. Clin Infect Dis. 2024; 78(3):730-741. doi: https://doi.org/10.1093/cid/ciad653
18.12.2024
S1-Leitlinie zur „Ambulante parenterale Antiinfektivatherapie (APAT)“
Die ambulante parenterale Antiinfektivatherapie (APAT) bezeichnet die intravenöse oder intramuskuläre Verabreichung von Antiinfektiva außerhalb des Krankenhauses. Sie kann im häuslichen Umfeld, in
Ambulanzen, Praxen oder stationären Pflegeeinrichtungen erfolgen.
Die ambulante Therapiesteuerung erfolgt im APAT-Team unter infektiologischer Leitung und in Zusammenarbeit mit den Hausärztinnen und Hausärzten. Regionen, in denen diese infektiologische Expertise
nicht vorhanden ist, sollen im Rahmen regionaler und überregionaler Sektor-übergreifender Infektiologie-Netzwerke Kontakt zu einem Behandlungszentrum mit Infektiologie in ihrer Umgebung
aufnehmen.
Zur Auswahl der Patienten für eine APAT soll eine Checkliste mit Auswahlkriterien angewendet werden. APAT-Patienten sollen sowohl im stationären als auch im ambulanten Setting identifiziert werden.
Auch Patienten mit besonderen Lebensumständen, ältere Menschen, Menschen, die Drogen injizieren, oder wohnungslose Menschen können unter bestimmten Voraussetzungen eine parenterale
Antiinfektivatherapie in einer ambulanten Einrichtung als APAT erhalten.
Die Auswahl des Gefäßkatheters für die parenterale Verabreichung der Antiinfektiva soll im Rahmen der Patienten-Evaluation durch das APAT-Team erfolgen. Sie hängt maßgeblich von spezifischen
Eigenschaften der Patienten, der ausgewählten Medikation, der vorhandenen Infrastruktur zur Anlage und Pflege und besonders von der geplanten Dauer der APAT ab. Wichtig sind regelmäßige Kontrollen
der Kathetereinstichstelle und Verbandswechsel. Die Patienten sollen in der Regel einmal wöchentlich von behandelnden Ärztinnen und Ärzten im ambulanten Bereich zur Kontrolle gesehen werden.
Grundsätzlich kann jede Infektionserkrankung mit Therapieindikation mittels APAT versorgt werden, solange keine orale Therapiemöglichkeit besteht, die Erkrankung eine ambulante Behandlung erlaubt,
die Kriterien zur Auswahl von Patienten erfüllt werden und die Infrastruktur zur Versorgung vorhanden ist. Voraussetzung für eine sichere und effektive Therapie ist die Betreuung durch
multiprofessionelle APAT-Teams, die intersektoral im Krankenhaus und im ambulanten Bereich zusammenarbeiten. Eine APAT muss prinzipiell immer leitliniengerecht und nach Antimicrobial Stewardship
(AMS)-Prinzipien erfolgen. Orale Therapieoptionen sollen gegenüber parenteralen Therapieformen priorisiert werden.
Zu den chemisch-physikalischen Kriterien, die bei der Auswahl eines Antiinfektivums für die APAT beachtet werden sollen, zählen das Dosierungsintervall eines Antiinfektivums, zuverlässige
Stabilitätsdaten und weitere physikalische und chemische Eigenschaften des Arzneistoffs in Bezug auf das Infusionssystem, das Lösungsmittel, die Konzentration, die Verwendung von
stabilitätsunterstützenden Puffern und die Temperatur, unerwünschte Arzneimittelwirkungen (UAW) und das Interaktionspotenzial in Bezug auf die gesamte Therapie.
Für weitere Informationen über die Leitlinie finden Sie über den nachfolgenden Button.
18.12.2024
Zulassungsempfehlung für pentavalenten Meningokokken-Impfstoff
Der Ausschuss für Humanarzneimittel (CHMP) bei der europäischen Arzneimittelbehörde EMA sprach in seiner Sitzung vom 19. September 2024 eine Zulassungsempfehlung für den Impfstoff Penbraya zur aktiven Immunisierung gegen invasive Meningokokken-Erkrankungen aus [1].
Invasive Meningokokken-Erkrankungen werden durch Neisseria meningitidis verursacht [1,2]. Häufig kommt es nach anfänglichen Anzeichen einer oberen Atemwegsinfektion plötzlich zu allgemeinen Symptomen wie Kopfschmerzen, Fieber oder Schüttelfrost, die sich innerhalb kurzer Zeit zu einem schweren, lebensbedrohlichen Krankheitsbild wie Meningitis und/oder Sepsis entwickeln können. Großflächige Hauteinblutungen sind insbesondere bei septischen Verläufen ausgeprägt, bei einer Meningitis sind zudem Nackensteifigkeit und Erbrechen charakteristisch. Die Letalität einer isolierten Meningokokken-Meningitis beträgt in Deutschland 1 %, bei einer Sepsis rund 13 % und bei Sepsis mit Waterhouse-Friderichsen-Syndrom ca. 33 %. Invasive Meningokokken-Erkrankungen werden im Wesentlichen durch Meningokokken der Serogruppen A, B, C, W, X und Y verursacht, die sich anhand der Zusammensetzung ihrer Kapselpolysaccharide unterscheiden. In Deutschland liegt die Inzidenz bei unter 0,4 Erkrankungen pro 100.000 Einwohner pro Jahr, für die Mehrheit der Erkrankungen sind Erreger der Serogruppe B (ca. 60 %), weniger häufig Erreger der Serogruppen C, W und Y (jeweils ca. 10 bis 15 %) verantwortlich [2].
Bei Penbraya handelt es sich um den ersten pentavalenten Meningokokken-Impfstoff, der zur aktiven Immunisierung von Personen ab 10 Jahren zur Vorbeugung invasiver Meningokokken-Erkrankungen durch die Neisseria meningitidis-Serogruppen A, C, W, Y und B eingesetzt werden soll. Dabei enthält Penbraya die Kapselpolysaccharide der Serogruppen A, C, W und Y konjugiert an Tetanus-Toxoid [1,3]. Für die Serogruppe B wurden Oberflächenproteine als Antigen gewählt, da auf Grund des Vorhandenseins identischer Polysaccharidstrukturen auf der B-Kapsel und auf menschlichen Nervenzellen kein Konjugatimpfstoff entwickelt werden konnte [2]. Dementsprechend enthält Penbraya außerdem das rekombinant hergestellte Faktor-H-Bindungsprotein (fHbp) der Unterfamilien A und B der Serogruppe B [1,3].
In einer randomisierten, einfachblinden, multizentrischen Nichtunterlegenheitsstudie der Phase-III wurde die Wirksamkeit und Sicherheit von Penbraya an Personen zwischen 10 und 25 Jahren untersucht [3]. Dabei wurden die Personen entweder mit Penbraya geimpft (2 Dosen im Abstand von 6 Monaten) oder mit einer Kombination aus einem quadrivalenten Konjugatimpfstoff (Serogruppen A, C, W und Y; einmalige Applikation zum Zeitpunkt 0) und einem monovalenten Subunitimpfstoff (Serogruppe B; 2 Dosen im Abstand von 6 Monaten). Die Seroresponse-Raten nach der Impfung mit Penbraya waren dabei dem herkömmlichen kombinierten Impfschema nicht unterlegen. Nach der Applikation von Penbraya wurde am häufigsten von Schmerzen an der Injektionsstelle, Müdigkeit, Kopf- und Muskelschmerzen sowie Schwellungen und Rötungen an der Injektionsstelle berichtet.
In Deutschland, Österreich und Schweiz stehen zur Immunisierung gegen Meningokokken derzeit monovalente Konjugatimpfstoffe (Serogruppe C), monovalente Meningokokken-B-Impfstoffe und quadrivalente Konjugatimpfstoffe (Serogruppen A, C, W, Y) für unterschiedliche Altersgruppen zur Verfügung. Für eine vollständige Abdeckung der Serogruppen A, B, C, W, Y müssen Impfstoffe kombiniert werden. Sofern die Europäische Kommission der Empfehlung des CHMP folgt und Penbraya durch die EMA zugelassen wird, ist es der erste zugelassene pentavalente Meningokokken-Impfstoff. Die Ständige Impfkommission am Robert-Koch-Institut (STIKO) arbeitet derzeit an einer Evaluation der Sicherheit und Wirksamkeit der verschiedenen Impfstoffe sowie der Modellierung verschiedener Impfstrategien für die Auffrischimpfung im Jugendalter, der pentavalente Impfstoff könnte dabei bereits berücksichtigt werden [4].
1 European Medicines Agency (EMA). Penbraya - summary of opinion. EMA/424272/2024; published online Sep 20, 2024. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-penbraya_en.pdf
2 Robert Koch Institut (RKI). Meningokokken, invasive Erkrankungen (Neisseria meningitidis). RKI-Ratgeber. Stand Januar 2024. URL: https://www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_Meningokokken.html#doc2374538bodyText1 [13.11.2024]
3 U.S. Food & Drug Administration (FDA). Penbraya (Meningococcal Groups A, B, C, W, and Y Vaccine). Full Prescribing Information. September 2024. URL: https://labeling.pfizer.com/ShowLabeling.aspx?id=19937&format=pdf
4 Ständige Impfkommission (STIKO). Protokoll der 107. Sitzung der Ständigen Impfkommission (STIKO) am 12. und 13.03.2024. URL: https://www.rki.de/DE/Content/Kommissionen/STIKO/Sitzungen/Protokolle/Sitzung_107.pdf?__blob=publicationFile [13.11.2024]
20.11.2024
Neue orale Therapieoption bei unkomplizierten Harnwegsinfekten in den USA zugelassen
Die US-amerikanische Food and Drug Administration (FDA) hat unter dem Namen Orlynvah ein neues orales Antibiotikum für die Therapie unkomplizierter Harnwegsinfekte bei Frauen zugelassen [1].
Orlynvah ist eine Kombination aus dem Thiopenem Sulopenem und Probenecid. Sulopenem liegt dabei als Prodrug in Form der Esterverbindung Sulopenem-Etzadroxil vor, die nach oraler Aufnahme durch die intestinalen Esterasen zum aktiven Sulopenem hydrolysiert wird [2,3]. Der Kombinationspartner Probenecid wird normalerweise als Urikosurikum eingesetzt, da auf Grund seiner kompetitiven Hemmung der organischen-Anionen-Transporter (OAT) in der Niere die tubuläre Rückresorption von Harnsäure verringert wird. Die OAT-Hemmung hat allerdings auch eine Reduktion der OAT-vermittelten renalen Clearance von Sulopenem zur Folge, wodurch dessen Halbwertszeit verlängert, und die Plasmakonzentration der antimikrobiell wirksamen Substanz erhöht werden [2,3].
Als Vertreter der Peneme zählt Sulopenem zu den β-Lactam-Antibiotika und seine bakterizide Wirkung basiert auf der Hemmung der bakteriellen Zellwandsynthese infolge der Bindung an Penicillin-bindende-Proteine (PBP) [2]. In vitro besitzt Sulopenem ein breites Wirkspektrum gegen Gram-positive, Gram-negative und anaerobe Bakterien. Es zeigt, wie Ertapenem, eine Wirksamkeit gegen multiresistente Gram-negative Erreger wie Enterobacterales, die bestimmte Extended Spectrum β-Lactamasen (ESBL) oder AmpC exprimieren aber wie Ertapenem ebenfalls eine Lücke gegen Pseudomonas aeruginosa [2-4]. Während die Sulopenem-Aktivität auch in Anwesenheit einiger β-Lactamasen und ESBLs bestehen bleibt, können Resistenzen u.a. durch die Veränderung der PBPs oder die Bildung von Carbapenemasen entstehen [2,3]. Orlynvah soll als Reserveantibiotikum nur zur Therapie von unkomplizierten Harnwegsinfektionen zur Anwendung kommen, die durch Escherichia coli, Klebsiella pneumoniae oder Proteus mirabilis verursacht werden und für die nur begrenzte oder keine alternativen oralen Behandlungsmöglichkeiten verfügbar sind [2].
Orlynvah enthält jeweils 500 mg Sulopenem-Etzadroxil und 500 mg Probenecid in Form einer Zweischichttablette. Die empfohlene Dosierung beträgt eine Tablette zweimal täglich zu den Mahlzeiten über einen Zeitraum von fünf Tagen. Eine Dosisanpassung bei einer leichten oder moderaten Einschränkung der Nierenfunktion ist nicht erforderlich [2].
Die Wirksamkeit und Sicherheit von Orlynvah wurde in mehreren kontrollierten, randomisierten, doppelblinden Phase-III-Studien bei unkomplizierten und komplizierten Harnwegsinfektionen untersucht. Darunter in SURE-1, einer Nichtunterlegenheitsstudie, in der 1671 eingeschlossene erwachsene Frauen mit einer unkomplizierten Harnwegsinfektion 1:1 randomisiert wurden [4]. Die Infektion wurde entweder mit 500 mg Sulopenem (als Sulopenem-Etzadroxil, in Kombination mit 500 mg Probenecid) zweimal täglich über fünf Tage oder mit 250 mg Ciprofloxacin zweimal täglich über drei Tage behandelt. Als primärer Endpunkt wurde das Gesamtansprechen, definiert als Kombination aus klinischem und mikrobiologischem Ansprechen, an Tag 12 bewertet. Die Gesamtansprechrate von Sulopenem-Etzadroxil/Probenecid betrug bei Patientinnen mit Ciprofloxacin-resistenten Erregern 62,6 % gegenüber 36,0 % unter Ciprofloxacin und war damit der Therapie mit dem Fluorchinolon überlegen (Differenz 26,6 %; 95 %-Konfidenzintervall 15,1-37,4). Bei Patientinnen mit Ciprofloxacin-sensiblen Erregern erfüllte Sulopenem-Etzadroxil/Probenecid jedoch nicht die Nichtunterlegenheitskriterien. Insgesamt betrachtet (Ciprofloxacin-resistente und -sensible Erreger) waren die Ansprechraten in beiden Gruppen vergleichbar und Sulopenem-Etzadroxil/Probenecid nicht unterlegen. Kritisch anzumerken ist die Vergleichsgruppe. Ciprofloxacin sollte aufgrund der potenziellen Nebenwirkungen und zunehmender Resistenzen nur dann zur Therapie bei unkomplizierten Harnwegsinfektionen verwendet werden, falls keine anderen oralen Antibiotika möglich sind [5].
Die Wirksamkeit von Orlynvah für die Erst- oder Folgebehandlung komplizierter Harnwegsinfektionen oder intraabdomineller Infektionen konnte in klinischen Studien nicht belegt werden [2].
Die am häufigsten unter der Therapie mit Orlynvah berichteten unerwünschten Wirkungen waren Diarrhö, Übelkeit, vaginale Hefepilzinfektionen, Kopfschmerzen und Erbrechen. Es muss außerdem u.a. das Risiko einer Clostridioides-difficile-assoziierten Diarrhö sowie die Bildung von Harnsäure-Nierensteinen beachtet werden [2].
Als erstes oral einzunehmendes Thiopenem könnte die Kombination aus Sulopenem-Etzadroxil/Probenecid eine wichtige Erweiterung der Therapieoptionen für die ambulante Behandlung unkomplizierter Harnwegsinfektionen bei Frauen sein, falls z.B. auf Grund der Resistenzsituation keine anderen antimikrobiellen Wirkstoffe eingesetzt werden können. Eine Sorge, die u.a. von der FDA geäußert wurde und die es äußerst aufmerksam zu beobachten gilt, ist die Möglichkeit für Kreuzresistenzen gegenüber anderen Carbapenemen. Es wäre höchst gefährlich, diese als intravenösen Breitspektrumantibiotika wichtigen Stützpfeiler bei der Behandlung schwerer Infektionen durch einen breiten Gebrauch oraler Carbapeneme zu gefährden.
1 U.S. Food & Drug Administration (FDA). FDA approves new treatment for uncomplicated urinary tract infections in adult women who have limited or no alternative oral antibiotic treatment options; published online Oct 24, 2024. URL: https://www.fda.gov/drugs/news-events-human-drugs/fda-approves-new-treatment-uncomplicated-urinary-tract-infections-adult-women-who-have-limited-or-no [06.11.2024]
2 U.S. Food & Drug Administration (FDA). Orlynvah (Sulopenem etzadroxil and Probenecid): Full Prescribing Information. Oct 2024. URL: https://www.accessdata.fda.gov/drugsatfda_docs/label/2024/213972s000lbl.pdf [06.11.2024]
3 Mangum, B. R. et al. Tebipenem and Sulopenem: Dynamic Duo or Double Trouble?.
Curr Infect Dis Rep. 2024; 26:139-150. doi: 10.1007/s11908-024-00831-1
4 Dunne, W. M. et al. Sulopenem or Ciprofloxacin for the Treatment of Uncomplicated Urinary Tract Infections in Women: A Phase 3, Randomized Trial. Clin Infect Dis. 2023; 76(1): 66-77. doi: 10.1093/cid/ciac738
5 Deutsche Gesellschaft für Urologie e. V. (Hrsg.): S3 Leitlinie: Epidemiologie, Diagnostik, Therapie, Prävention und Management unkomplizierter, bakterieller, ambulant erworbener Harnwegsinfektionen bei Erwachsenen – Aktualisierung 2024. URL: https://register.awmf.org/de/leitlinien/detail/043-044 [16.11.2024]
20.11.2024
Welt-AIDS-Tag 2024: Gemeinsam für Gleichberechtigung und gegen Diskriminierung
Am 1. Dezember ist Welt-AIDS-Tag – ein Tag, der seit über 30 Jahren auf die Rechte und Bedürfnisse HIV-positiver Menschen weltweit aufmerksam macht. Jedes Jahr erinnert er an die rund 40 Millionen Menschen, die aktuell mit HIV leben, sowie an jene, die an den Folgen von HIV und AIDS verstorben sind. Trotz großer Fortschritte in der Therapie und Prävention bleibt die Ungleichheit im Zugang zur Versorgung eine globale Herausforderung.
Das diesjährige Motto des Welt-AIDS-Tags, „Take the rights path“, verdeutlicht die Bedeutung von Menschenrechten im Kampf gegen HIV und AIDS. Insbesondere sogenannte Schlüsselgruppen sind vielfach
benachteiligt und haben ein erhöhtes Risiko, sich mit HIV zu infizieren oder an AIDS zu erkranken. Der Zugang zu Prävention, Beratung und medizinischer Versorgung ist entscheidend – für alle, ohne
Diskriminierung und Vorurteile. „Wir können AIDS beenden, wenn wir die Ungleichheiten beseitigen, die die Krankheit aufrechterhalten“, so UNAIDS-Exekutivdirektorin Winnie Byanyima.
Die aktuelle Kampagne zeigt: Menschen mit HIV können heute bei rechtzeitiger Therapie ein normales Leben führen. Der Ausbruch von AIDS lässt sich verhindern, und das Virus ist unter Therapie nicht mehr übertragbar. Dennoch sind Diskriminierung und Stigmatisierung nach wie vor Teil ihres Alltags – verursacht durch Unwissenheit und Vorurteile.
Und hier setzt die Kampagne 2024 an: Durch persönliche Einblicke in das Leben HIV-positiver Menschen will sie Berührungsängste abbauen und zeigen, dass HIV kein Grund für Distanz im Alltag ist.
Unterstützen Sie die Kampagne, indem Sie Informationen teilen und das Bewusstsein für ein diskriminierungsfreies Zusammenleben fördern. Durch Aufklärung und Information sollen bestehende
Unsicherheiten abgebaut werden.
20.11.2024
INFEKTIO_Podcast | Eine Herzensangelegenheit – Die bakterielle Endokarditis
Der Podcast consilium infectiorum bietet medizinischem Fachpersonal praxisrelevante Themen der klinischen Infektiologie und unterstützt dabei, evidenzbasierte Behandlungsoptionen für Patienten auszuwählen.
In jeder Folge diskutiert Infektiologe Prof. Mathias Pletz aus Jena mit einem Expertengast einen klinischen Schwerpunkt – fundiert und dennoch in entspannter Gesprächsatmosphäre.
Besonders praktisch: Für jede Folge können Sie bis zu einem Jahr nach Veröffentlichung CME-Punkte sammeln, indem Sie die zugehörigen CME-Fragen beantworten.
In der aktuellen Folge ist Priv.-Doz. Stefan Hagel aus Jena zu Gast. Gemeinsam widmen sie sich dem Thema bakterielle Endokarditis.
20.11.2024
Nasaler Influenza-Impfstoff zur Selbstanwendung zugelassen
Die US-amerikanische Food and Drug Administration (FDA) hat unter dem Namen FluMist einen Impfstoff gegen die saisonale Influenza in Form eines Nasensprays zugelassen, das erstmals auch selbst von der zu impfenden Person angewendet werden darf [1].
Die saisonale Influenza verursachte nach Angaben des U.S. Centers for Disease Control and Prevention (CDC) zwischen 2010 und 2023 jährlich etwa 9,3 bis 41 Millionen Erkrankungen, 100.000 bis 710.000 Krankenhausaufenthalte und 4.900 bis 51.000 Todesfälle in den USA [1]. Obwohl jedes Jahr eine Reihe zugelassener Impfstoffe zur Verfügung stehen, sind die Impfquoten im Vergleich zu den Zeiträumen vor der COVID-19-Pandemie rückläufig [2]. In der Saison 2023/2024 waren Schätzungen zufolge nur etwa die Hälfte der Kinder (≥ 6 Monate) und der Erwachsenen gegen Influenza geimpft, so wenig wie zuletzt vor 12 bzw. vor 6 Jahren. Damit liegt die Durchimpfungsrate weiterhin unter dem nationalen Ziel der Healthy-People-2030-Initiative von 70 % für Personen ≥ 6 Monate [2].
FluMist ist in den USA bereits seit 2007 zur aktiven Immunisierung von Personen zwischen 2 und 49 Jahren im Einsatz [1]. Es handelt sich dabei um einen Lebendimpfstoff, der die von der Weltgesundheitsorganisation (WHO) und FDA jeweils für eine Saison empfohlenen Stämme von Influenza A und B in Form von lebend-attenuierten Viren enthält. In der aktuellen Saison 2024/2025 umfasst das trivalente Vakzin die Stämmen A(H1N1), A(H3N2) und B(Victoria) [3].
Im Gegensatz zu anderen Influenza-Impfstoffen muss FluMist allerdings nicht intramuskulär injiziert werden, sondern wird in Form einer Suspension mittels Zerstäuber in die Nase appliziert [3]. Der nasale Applikationsweg wird ermöglicht durch die gentechnische Veränderung des Wildtypvirus zu kälteadaptierten und temperaturempfindlichen abgeschwächten Reassortanten-Influenzaviren. Diese sind zwar in der Lage, sich im Nasopharynx zu vermehren und dadurch eine Immunreaktion auszulösen, allerdings erfolgt in den unteren Atemwegen und der Lunge auf Grund der wärmeren Temperaturen keine effiziente Replikation [3,4]. Die genannten Eigenschaften ermöglichen die Induktion einer schützenden Immunreaktion, ohne dass eine klinische Erkrankung ausgelöst wird.
Ein Nasenapplikator enthält eine Einzeldosis Impfstoff, die mit jeweils einem Hub pro Nasenloch aufgeteilt wird. Die nadelfreie Applikation musste bisher, wie auch bei anderen Vakzinen, durch medizinisches Fachpersonal bzw. durch einen Gesundheitsdienstleister erfolgen. Nun konnte durch den Zulassungsinhaber MedImmune in einer Studie gezeigt werden, dass auch Pflegepersonal und die Impflinge selbst mit Hilfe der in der Gebrauchsanweisung enthaltenen Informationen den Impfstoff sicher und effektiv applizieren können [1]. Daher erlaubt die Zulassung jetzt erstmalig eine Impfstoffapplikation durch die volljährige zu impfende Person selbst oder eine volljährige Betreuungsperson. Bei der Impfung von Kindern und Jugendlichen zwischen 2 und 17 Jahren wird die Applikation durch eine erwachsene Person empfohlen.
Nach der Impfung gehörten Fieber (Kinder zwischen 2-6 Jahren), laufende Nase und verstopfte Nase (Personen zwischen 2-49 Jahren) sowie Halsschmerzen (Erwachsene zwischen 18-49 Jahren) zu den am häufigsten beobachteten Nebenwirkungen [1,3].
Die neue Möglichkeit der Selbstanwendung des nasalen Impfstoffs könnte die Zugänglichkeit, Flexibilität und den Komfort einer sicheren und effektiven saisonalen Influenzaimpfung erhöhen und die Steigerung der Impfquoten positiv beeinflussen. Es wird davon ausgegangen, dass FluMist ab der Saison 2025/2026 für die Selbstanwendung in den USA zur Verfügung steht.
In Deutschland und Österreich wird in der aktuellen Influenza-Saison ebenfalls das trivalente Influenzavakzin als Nasenspray durch AstraZeneca unter dem Namen Fluenz zur Verfügung gestellt. Allerdings ist es hierzulande nur zur aktiven Immunisierung von Kindern und Jugendlichen zwischen 24 Monaten und dem vollendeten 18. Lebensjahr und für Applikation unter Aufsicht eines Arztes, Apothekers oder von medizinischem Fachpersonal zugelassen [5].
1 U.S. Food & Drug Administration (FDA). FDA Approves Nasal Spray Influenza Vaccine for Self- or Caregiver-Administration. Press Announcement; published online Sep 20, 2024. URL: https://www.fda.gov/news-events/press-announcements/fda-approves-nasal-spray-influenza-vaccine-self-or-caregiver-administration?mtm_source=25 [11.10.2024]
2 Centers for Disease Control and Prevention (CDC). Flu Vaccination Coverage, United States, 2023–24 Influenza Season; published online Sep 20, 2024. URL: https://www.cdc.gov/fluvaxview/coverage-by-season/2023-2024.html [11.10.2024]
3 U.S. Food & Drug Administration (FDA). FluMist (Influenza Vaccine Live, Intranasal): Full Prescribing Information. Sep 2024. URL: https://www.fda.gov/media/180697/download?attachment [11.10.2024]
4 European Medicines Agency (EMA). Assessment report Fluenz (Influenza vaccine, live attenuated, nasal); published online May 21, 2024. URL: https://www.ema.europa.eu/en/documents/assessment-report/fluenz-epar-public-assessment-report_en.pdf-0 [12.10.2024]
5 European Medicines Agency (EMA). Zusammenfassung der Merkmale des Arzneimittels Fluenz (Influenza-Impfstoff, lebend-attenuiert, nasal); published online Jul 22, 2024. URL: https://www.ema.europa.eu/de/documents/product-information/fluenz-epar-product-information_de.pdf [11.10.2024]
23.10.2024
RSV-Impfung ab sofort Kassenleistung für ältere Erwachsene und Risikogruppen in Deutschland
Mit der Anpassung der Schutzimpfungsrichtlinie durch den Gemeinsamen Bundesausschuss (G-BA) und deren Veröffentlichung im Bundesanzeiger am 26. September 2024 übernimmt die gesetzliche Krankenversicherung (GKV) in Deutschland nun die Kosten für die Impfung gegen das Respiratorische Synzytial-Virus (RSV).
Anspruch auf die Impfung haben ab sofort alle gesetzlich Versicherten ab 75 Jahren sowie Versicherte zwischen 60 und 74 Jahren, die bestimmte Risikofaktoren aufweisen. Diese Entscheidung basiert auf der Empfehlung der Ständigen Impfkommission (STIKO) und betrifft vor allem Menschen mit Grunderkrankungen oder einem geschwächten Immunsystem, die ein erhöhtes Risiko für schwere Verläufe einer RSV-Infektion haben.
Die RSV-Impfung sollte idealerweise vor Beginn der RSV-Saison erfolgen, um optimalen Schutz zu gewährleisten. Aktuell ist nur eine einmalige Impfung vorgesehen, da die STIKO auf Basis der bisherigen Datenlage noch keine Entscheidung über mögliche Auffrischungsimpfungen getroffen hat. Auch zu einer möglichen Impfung von Schwangeren hat die STIKO bislang keine Empfehlung abgegeben.
23.10.2024
Erster mRNA-Impfstoff gegen Respiratorische Synzytial-Viren (RSV) zugelassen
Seit Herbst 2023 stehen unter den Handelsnamen Arexvy und Abrysvo die weltweit ersten RSV-Impfstoffe zur Verfügung, die vor RSV-assoziierten Erkrankungen der unteren Atemwege und damit einhergehenden Komplikationen schützen sollen. Beide Vakzine gehören zu den Subunit-Impfstoffen, da sie als Antigen das RSV-Fusionsoberflächenprotein (F-Protein, rekombinant hergestellt) enthalten, stabilisiert in der Präfusionskonformation. Die Applikation der Impfstoffe löst eine B- und T-Zellantwort des Immunsystems und damit auch die Bildung von Antikörpern gegen das F-Protein sowie Gedächtniszellen aus, die bei erneutem Antigenkontakt eine schnelle Immunreaktion ermöglichen. Arexvy (RSVPreF3, adjuvantiert) ist zugelassen für die aktive Immunisierung von Erwachsenen ≥ 60 Jahren, Abrysvo (RSVPreF) kann neben der Anwendung bei älteren Erwachsenen gemäß Zulassung auch für die passive Immunisierung von Neugeborenen durch die Impfung der Mutter während der Schwangerschaft eingesetzt werden.
Nach der Zulassung beider Impfstoffe im letzten Jahr setzte sich die Ständige Impfkommission am Robert Koch Institut (STIKO) mit der Erarbeitung einer Impfstrategie und Empfehlungen zum Einsatz der neuen Impfstoffe auseinander. Erst vor wenigen Wochen gab die STIKO dann bekannt, dass alle Personen ≥ 75 Jahren eine einmalige RSV-Impfung mit einem der beiden proteinbasierten Impfstoffe (Arexvy oder Abrysvo) kurz vor der RSV-Saison als Standardimpfung erhalten sollten. Darüber hinaus wird eine Impfung auch Personen im Alter von ≥ 60 Jahren empfohlen, wenn schwere Grunderkrankungen vorliegen oder es sich um Bewohnende von Pflegeheimen handelt.1
Kurz nach der Veröffentlichung der STIKO-Empfehlungen wurde am 23.08.2024 unter dem Handelsnamen mResvia (mRNA-1345) ein weiterer Impfstoff gegen RSV in Europa zugelassen.2 Im Gegensatz zu Arexvy und Abrysvo enthält mResvia allerdings kein Protein als Antigen sondern mRNA, die für das F-Protein in der Präfusionskonformation codiert.3 Die in Lipid-Nanopartikeln verpackte mRNA wird nach der intramuskulären Applikation in die Zellen an der Injektionsstelle aufgenommen, wo eine vorübergehende Translation in das Virusprotein erfolgt. Das dort exprimierte F-Protein löst dann wiederum die Immunantwort und damit u.a. die Bildung von Antikörpern aus. Das gleiche Prinzip macht man sich bereits bei den mRNA-Impfstoffen gegen COVID-19 zu Nutze.
In der laufenden randomisierten, doppelblinden und multizentrischen Phase-II/III Studie ConquerRSV wurde die Wirksamkeit der Impfung gegen RSV-bedingte Erkrankungen der unteren Atemwege mit zwei oder mehr Symptomen untersucht.4 Dazu wurden 35.541 Personen im Alter von ≥ 60 Jahren randomisiert und sollten entweder mit mResvia (n = 17.793) oder Placebo (n = 17.748) geimpft und über 12 Monate nach der Injektion beobachtet werden. Zum Zeitpunkt der Auswertung lag die mediane Nachbeobachtungszeit bei 112 Tagen. Dabei wurde eine Impfstoffwirksamkeit von 83,7 % (95,88 %-Konfidenzintervall (KI); 66,0-92,2) im Hinblick auf die Prävention von RSV-assoziierten Erkrankungen der Atemwege mit mindestens zwei Anzeichen oder Symptomen ermittelt. Ähnliche Ergebnisse zeigten sich in der Verhinderung einer RSV-Erkrankung mit mindestens drei Anzeichen oder Symptomen, bei der die Impfstoffwirksamkeit 82,4 % (96,36 %-KI; 34,8-95,3) betrug. Der Impfstoff zeigte eine Schutzwirkung gegen beide Subtypen RSV A und RSV B. Auch wenn in der mResvia-Gruppe häufiger lokale und systemische unerwünschte Reaktionen auftraten, waren diese meist leicht bis mittelschwer und vorübergehend. Die häufigsten Nebenwirkungen waren Schmerzen an der Injektionsstelle, Müdigkeit, Kopfschmerzen, Myalgie und Arthralgie.
mResvia ist der erste mRNA-Impfstoff gegen RSV, der sich zum Zeitpunkt der Erarbeitung der STIKO-Impfstrategie noch im Zulassungsprozess befand und daher noch nicht Gegenstand der derzeitigen Empfehlungen ist. Laut STIKO ist die Evidenzaufarbeitung des neuen Impfstoffes schnellstmöglich nach der Zulassung geplant.1
1 Falman, A. et al. Beschluss und Wissenschaftliche Begründung zur Empfehlung der STIKO für eine Standardimpfung gegen Erkrankungen durch Respiratorische Synzytial-Viren (RSV) für Personen ≥ 75 Jahre sowie zur Indikationsimpfung von Personen im Alter von 60 bis 74 Jahren mit Risikofaktoren. Epid. Bull. 2024; 32:3-28. doi: 10.25646/12470
2 Europäische Kommission. Kommission genehmigt mRNA-Impfstoff gegen Atemwegsviren. Pressemitteilung; published online Aug 23, 2024. URL: https://germany.representation.ec.europa.eu/news/kommission-genehmigt-mrna-impfstoff-gegen-atemwegsviren-2024-08-23_de [30.08.2024]
3 European Medicines Agency (EMA). mResvia – summary of opinion. EMA/CHMP/285703/2024; published online Jun 27, 2024. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-mresvia_en.pdf [30.08.2024]
4 Wilson, E. et al. Efficacy and Safety of an mRNA-Based RSV Pref Vaccine in Older Adults. N Engl J Med. 2023; 389(24):2233-2244. doi: 10.1056/NEJMoa230707
11.09.2024
STIKO-Empfehlung zur Anwendung des 20-valenten Pneumokokken-Impfstoffs im Säuglings-, Kinder- und Jugendalter
Infektionen mit Pneumokokken (Streptococcus pneumoniae) können bei Menschen aller Altersgruppen Erkrankungen der oberen (Sinusitis, Otitis media) und unteren Atemwege (Pneumonie) verursachen. Derzeit sind etwa 100 verschiedene Pneumokokken-Serotypen bekannt, die große Unterschiede in der Häufigkeit zeigen. Pneumokokken-Erkrankungen werden in „invasiv“ (invasive pneumococcal disease – IPD, definiert als Nachweis aus normalerweise sterilem Material wie Blut, Liquor, Ascites, Punktate) und „nicht-invasiv“ unterschieden (alleiniger Nachweis aus respiratorischem Material). Insbesondere Kinder unter 5 Jahren zählen zur Risikogruppe für schwere IPD wie Blutstrominfektionen oder Meningitis mit möglichen Langzeitfolgen (z.B. Seh-, Hörverlust oder neurologische Defizite) und Todesfällen. Trotz etablierter Impfstrategien ist die Krankheitslast durch IPD in dieser Altersgruppe auf Grund von unzureichenden Impfquoten und dem Auftreten von nicht-impfpräventablen Serotypen in Deutschland und weltweit hoch.
Die derzeit verfügbaren Pneumokokken-Impfstoffe unterscheiden sich sowohl in der Art des Impfstoffs als auch in Art und Anzahl der enthaltenen Serotypen (Tab.1). Für die Grundimmunisierung von Säuglingen zugelassen und von der STIKO empfohlen sind 13- oder 15-valente Pneumokokken-Konjugatimpfstoffe (PCV13, PCV15), entweder als 2+1 Schema (2,4 und 11 Monate) für reifgeborene Säuglinge oder als 3+1 Schema (2,3,4 und 11 Monate) für Frühgeborene. Für Kinder und Jugendliche im Alter von 2 bis 17 Jahren mit Immundefizienz oder sonstigen chronischen Erkrankungen, die mit einem erhöhten Risiko für eine Pneumokokken-Meningitis einhergehen, wird eine Indikationsimpfung empfohlen. Diese besteht aus einer Impfstoffdosis PCV13 oder PCV15 gefolgt von einer Impfstoffdosis des 23-valenten Polysaccharid-Impfstoffs (PPSV23) 6 bis 12 Monate später.
Tab. 1 Übersicht der in den verschiedenen Pneumokokken-Impfstoffen enthaltenen Serotypen
| PCV13 (Prevanar) | PCV15 (Vaxneuvance) | PPSV23 (Pneumovax) | PCV20 (Prevenar20) |
| 1 | 1 | 1 | 1 |
|
2 |
|||
| 3 | 3 | 3 | 3 |
| 4 | 4 | 4 | 4 |
| 5 | 5 | 5 | 5 |
| 6A | 6A | 6A | |
| 6B | 6B | 6B | 6B |
| 7F | 7F | 7F | 7F |
| 8 | 8 | ||
| 9N | |||
| 9V | 9V | 9V | 9V |
| 14 | 14 | 10A | 10A |
| 11A | 11A | ||
| 12F | 12F | ||
| 14 | 14 | 14 | 14 |
| 15B | 15B | ||
| 17F | |||
| 18C | 18C | 18C | 18C |
| 19A | 19A | 19A | 19A |
| 19F | 19F | 19F | 19F |
| 20 | |||
| 22F | 22F | 22F | |
| 23F | 23F | 23F | 23F |
| 33F | 33F | 33F |
Kürzlich wurde mit Prevenar 20 (vormals Apexxnar) ein neuer 20-valenter PCV in Europa zugelassen, der gemäß Zulassung u.a. für die Immunisierung von Säuglingen in einem 3+1 Impfschema und bei Kindern und Jugendlichen als einmalige Einzeldosis eingesetzt werden kann. PCV20 enthält im Vergleich zu PCV13 sieben zusätzliche Serotypen, wodurch insgesamt ca. 53 % der IPD-Fälle bei unter 18-Jährigen abgedeckt werden. Die STIKO hat nun die vorliegenden Daten zum neuen Impfstoff im Hinblick auf eine mögliche Aufnahme in die Empfehlungen für Säuglinge, Kinder und Jugendliche überprüft.
Die Immunogenitätsdaten aus den Zulassungsstudien von PCV20 deuten auf eine im Vergleich zu PCV13 verringerte Immunantwort nach der Impfung hin, gemessen an den durch die Impfung induzierten IgG-Antikörperkonzentrationen. Die Unterschiede sind am deutlichsten nach der 2. bzw. 3. Impfstoffdosis im Säuglingsalter, erst mit Abschluss der Grundimmunisierung unterscheiden sich die Immunogenitätsdaten zwischen den verschiedenen Impfschemata und Impfstoffen weniger stark. Dennoch sind auch nach der abschließenden Impfstoffdosis die IgG-Antikörperkonzentrationen für alle gemeinsam enthaltenen Serotypen unter PCV20 niedriger als bei PCV13. Die Sicherheitsprofile beider Impfstoffe waren vergleichbar.
Es bleibt unklar, ob der Wechsel von PCV13 zu PCV20 durch die Erweiterung der Serotypen bei gleichzeitig intensitätsgeminderter Immunantwort eine zusätzliche Reduktion der Krankheitslast zur Folge haben würde. Aus diesem Grund bleibt die STIKO, basierend auf den bisherigen Daten, bei der Empfehlung für PCV13/PCV15 im 2+1 Schema für gesunde, reifgeborene Neugeborene. Es gibt außerdem Bedenken, ob ein PCV20 3+1 Schema durch den zusätzlichen Impftermin, in dem bereits sehr vollen Impfplan für Neugeborene, zu einer Erniedrigung der Impfquoten führen könnte. Da zur Immunogenität von PCV20 bei Frühgeborenen keine Daten vorliegen, wird auch hier keine Änderung der Anwendung von PCV13/PCV15 im 3+1 Schema empfohlen. Bei Kindern mit Risikofaktoren für einen schweren Verlauf einer Pneumokokken-Erkrankung stehen für die Anwendung von PCV20 noch nicht ausreichend Daten zur Verfügung, sodass noch keine abschließende Entscheidung getroffen werden kann.
Zusammenfassend bleiben alle bisherigen Empfehlungen der STIKO zur Pneumokokken-Impfung im Säuglings-, Kinder- und Jugendalter unverändert bestehen und eine Anwendung von PCV20 in dieser Altersgruppe wird zum jetzigen Zeitpunkt nicht empfohlen.
Ständige Impfkommission (STIKO) beim Robert Koch-Institut. Stellungnahme der STIKO zur Anwendung des 20-valenten Pneumokokken-Konjugatimpfstoffs (PCV20) im Säuglings-, Kindes- und Jugendalter. Epid. Bull. 2024; 31:3-8. doi: 10.25646/12311
11.09.2024
Empfehlungen für Zusammensetzung der saisonalen Influenza-Vakzine 2024/2025
Auf Grundlage der kontinuierlichen globalen Surveillance zirkulierender Influenzaviren gibt die Weltgesundheitsorganisation (WHO) jedes Jahr Empfehlungen für die Virusstämme, die in den saisonalen Impfstoffen enthalten sein sollten, um die Wirksamkeit der Impfung aufrechtzuerhalten. Nun folgte die Europäische Arzneimittelbehörde (EMA) den aktuellen Empfehlungen der WHO und spricht sich für die kommende Saison unter anderem auch für eine Reduktion der Anzahl der in den Vakzinen enthaltenen Virusstämme aus.1
Seit November 2017 empfiehlt die Ständige Impfkommission in Deutschland nur noch die Verwendung quadrivalenter Impfstoffe für die saisonale Immunisierung gegen Influenza. Aus diesem Grund enthielten die in Deutschland, sowie auch in der Schweiz und Österreich, zuletzt verfügbaren Influenza-Vakzine die Antigene von vier Virusstämmen: Influenza A-Virus Subtypen A/H1N1 und A/H3N1 sowie die saisonalen B-Viruslinien B/Victoria und B/Yamagata.
Influenza B/Yamagata zirkulierte jedoch seit März 2020 nicht mehr, was zumindest teilweise auf die öffentlichen Gesundheitsmaßnahmen zurückgeführt wird, die zu Beginn der COVID-19-Pandemie ergriffen wurden. Die einzigen B/Yamagata Nachweise stammten aus den lebenden attenuierten Impfstoffen.1,2 Nach Ansicht der WHO, der FDA und der EMA ist es demnach nicht mehr notwendig, den B/Yamagata-Virusstamm weiter in die Influenza-Vakzine aufzunehmen.
Idealerweise sollte der Stamm daher bereits ab der Saison 2024/2025 zunächst aus allen Lebendimpfstoffen ersatzlos entfernt werden, sodass die Impfstoffe nur noch Antigene der Hauptstämme A/H1N1, A/H3N2 und B/Victoria enthalten und damit zu trivalenten Vakzinen werden.1
Da eine Anpassung eines quadrivalenten Vakzins zu einem trivalenten eine grundlegende Änderung des Impfstoffes bedeutet, müssen die Hersteller zur Zulassung mitunter erneute Prüfungen und Nachweise vorlegen, wenn der Impfstoff nicht bereits früher einmal in einer trivalenten Form zugelassen wurde. Im Interesse der Sicherstellung der Impfstoffversorgung für die kommende Saison sollte die Änderung zur trivalenten Zusammensetzung für alle anderen Impfstoffe daher spätestens für die Saison 2025/2026 abgeschlossen sein.1
Die konkreten für die verschiedenen Impfstofftypen empfohlenen Virusvarianten können den Dokumenten der EMA entnommen werden.
Kommentar der Herausgeber
Nachdem in den letzten präpandemischen Jahren aufgrund der damaligen Influenza-Epidemiologie die quadrivalenten Influenza-Impfstoffe zum Standard wurden, scheint aufgrund des Verschwindens der
B/Yamagata Stämme aus der Zirkulation ein Umdenken an der Zeit. Dies würde die Produktion vereinfachen, Produktionskosten senken sowie Kapazitäten erhöhen. Außerdem könnte sich die Möglichkeit
bieten, eine erhöhte Antigen-Dosis der A(H3N2) Komponente oder zwei verschiedene A(H3N2) Viren in den Impfstoffen der nächsten Generation zu verwenden, da gerade die A(H3N2) Komponente in den letzten
Jahren eine geringere Vakzinwirksamkeit zeigte.
1 European Medicines Agency (EMA). EU recommendations for 2024/2025 seasonal flu vaccine composition; published online Mar 26, 2024 (last updated Jun 3, 2024).
URL: https://www.ema.europa.eu/en/news/eu-recommendations-2024-2025-seasonal-flu-vaccine-composition [10.07.2024]
2 Monto A. S. et al. The End of B/Yamagata Influenza Transmission — Transitioning from Quadrivalent Vaccines. N Engl J Med 2024; 390(14):1256-1258. doi: 10.1056/NEJMp2314801
14.08.2024
STIKO empfiehlt RSV-Impfung für ältere und vulnerable Erwachsene
Die Ständige Impfkommission (STIKO) hat am 08. August 2024 ihre Empfehlung für die Impfung gegen Respiratorische Synzytial-Viren (RSV) bei älteren Erwachsenen veröffentlicht. Die Empfehlung umfasst:
- Menschen ab 75 Jahren
- Personen im Alter von 60-74 Jahren mit schweren Grunderkrankungen oder die in einer Pflegeeinrichtung leben
Ein speziell für ältere Erwachsene entwickelter adjuvantierter RSV-Impfstoff (Arexvy) zeigt eine hohe Wirksamkeit:
- 94,6 % Risikoreduktion für RSV-bedingte Erkrankungen der unteren Atemwege (RSV-LRTD) bei Patienten ab 60 Jahren mit mindestens einer relevanten Komorbidität (z.B. COPD, Asthma, Diabetes Typ 1 oder 2, chronische Herzinsuffizienz, fortgeschrittene Leber- oder Nierenerkrankung)
- 93,8 % Schutzeffekt bei Erwachsenen in der Altersgruppe 70-79 Jahre
- Anhaltende Wirksamkeit über zwei volle RSV-Saisons: 74,9 % bei 70- bis 79-Jährigen und 66,7 % bei Patienten mit mindestens einer Komorbidität
Die STIKO empfiehlt, zeitnah mit dem Impfen zu beginnen, um möglichst viele Risikopatienten zum Beginn der RSV-Saison im Herbst zu schützen. Private Krankenversicherungen übernehmen in der Regel ab der STIKO-Empfehlung die Kosten. Für gesetzlich Versicherte ist in vielen Fällen eine freiwillige Kostenerstattung durch die Krankenkasse möglich. Nach Aufnahme in die Schutzimpfungsrichtlinie wird die RSV-Impfung von allen Krankenkassen erstattet.
14.08.2024
Anstieg der Pertussis-Fälle in Europa
Pertussis (Keuchhusten) ist eine weltweit endemische, meist über mehrere Wochen bis Monate andauernde Erkrankung der Atemwege, die hauptsächlich durch eine Infektion mit dem Gram-negativen Stäbchen Bordetella pertussis verursacht wird. Ein klassisches Symptom bei Kindern stellen die anfallsartig auftretenden Hustenanfälle dar, oft begleitet von inspiratorischem Stridor („Keuchen“), Würgereiz und Erbrechen. Schwere Komplikationen wie bakterielle Superinfektionen und Pneumonien können insbesondere bei Säuglingen auftreten und führen nicht selten zu Krankenhausaufenthalten und Tod durch Atemstillstand. Typisch ist der Ablauf in 3 Phasen: Einer katarrhalischen Phase mit unspezifischen Symptomen, gefolgt von einer paroxysmalen Phase mit den typischen namensgebenden (keuchenden) Hustenattacken ab der 2. Krankheitswoche und schließlich einer Konvaleszenzphase, die prolongiert über mehrere Wochen verlaufen kann. Bei Jugendlichen und Erwachsenen sind die klinischen Manifestationen jedoch weniger charakteristisch und weniger schwer als bei kleineren Kindern. Trotz existierender Impfstoffe ist alle 3 bis 5 Jahre mit größeren Epidemien zu rechnen, da weder die Impfung noch die natürliche Infektion zu einer dauerhaften Immunität führen.1,2
Nachdem zuletzt während den Jahren der COVID-19-Pandemie die Verbreitung von Pertussis sehr begrenzt war, werden seit der 2. Jahreshälfte 2023 weltweit wieder deutlich mehr Fälle registriert. Das Europäische Zentrum für die Prävention und die Kontrolle von Krankheiten (ECDC) berichtet, dass die Anzahl der gemeldeten Fälle in Europa bereits in den ersten 3 Monaten des Jahres 2024 (ca. 32.000 Fälle) höher ist als im Jahr 2023 über einen 12-Monats-Zeitraum (ca. 25.000 Fälle).2 Der zeitliche Verlauf der verstärkten Pertussis-Aktivität sowie die betroffenen Altersgruppen unterscheiden sich zum Teil in den einzelnen europäischen Ländern, wie die folgenden Beispiele aus Dänemark und Italien zeigen.2
In Dänemark war die Pertussis-Inzidenz bereits im August 2023 fünfmal so hoch wie die interepidemische Inzidenz und markierte damit den Beginn der Epidemie, die ihren Höhepunkt im November 2023 erreichte (337 Fälle/100.000 Einwohner) und erst im Januar und Februar 2024 wieder zurückging. Am stärksten betroffen waren Personen im Alter von 10-19 Jahren, was angesichts der in Dänemark nicht empfohlenen Auffrischimpfung für diese Altersgruppe nicht überrascht. Die Inzidenz bei Säuglingen war ebenfalls erhöht, allerdings im Vergleich zu früheren Epidemien in niedrigerem Ausmaß. Gleiches gilt für den Anteil der Kleinkinder bis 2 Jahre, die auf Grund der Infektion stationär behandelt werden mussten. Die Hospitalisierungsrate von 60,4 % lag ebenfalls deutlich unter den Werten früherer Epidemien, was möglicherweise auf den Schutz vor schwerer Pertussis durch geimpfte Mütter zurückzuführen ist, deren Impfquote auf 85 % im Beobachtungszeitraum geschätzt wurde. Ein Todesfall ereignete sich bei einem Frühgeborenen einer ungeimpften Mutter. Mit Beginn des Jahres 2024 wurde die Impfung von Schwangeren als Bestandteil des nationalen Impfprogramms aufgenommen.3
In Italien ist seit Januar 2024 ein deutlicher Anstieg der Pertussis-Fälle zu verzeichnen, der bereits jetzt den größten Pertussis-Ausbruch in den letzten Jahrzehnten darstellt. Neben der Grundimmunisierung im Säuglingsalter zählen Auffrischimpfungen im Vorschulalter, bei Jugendlichen und Erwachsenen zu den empfohlenen Maßnahmen. Im Gegensatz zur Epidemie in Dänemark sind von dem Pertussis-Ausbruch in Italien vor allem Neugeborene und Säuglinge betroffen, von denen bisher 108 stationär behandelt werden mussten, im Vergleich zu 12 Kindern im Jahr 2023. Die Mehrheit der hospitalisierten Kinder war ungeimpft, am häufigsten auf Grund des noch zu geringen Alters. Zwölf Säuglinge zeigten einen schweren Krankheitsverlauf und mussten auf der Intensivstation behandelt werden. Bis zum Ende des Berichtszeitraums wurden 3 Todesfälle bei Neugeborenen gemeldet. Der Ausbruch, der vor allem Neugeborene und ungeimpfte Säuglinge betraf, wird u.a. auf die Nichteinhaltung der Impfempfehlungen während der Schwangerschaft zurückgeführt.4
Die Unterschiede zwischen den einzelnen Ländern können durch die verschiedenen Vorgehensweisen hinsichtlich Impfstrategien, Testungsregimen, Erfassung von Altersgruppen, länderspezifischen Surveillance-Programmen und unterschiedlicher Intensität und Fortdauer der COVID-19 Maßnahmen bedingt sein. Durch die Einflüsse der COVID-19-Pandemie ist beim Vergleich der aktuellen Pertussis-Ausbrüche mit früheren Epidemien allerdings Vorsicht geboten. Dennoch gibt das aktuelle Infektionsgeschehen Anlass, den Fokus auf die Maßnahmen zur Infektionsprävention zu lenken. In den meisten Altersgruppen lässt sich das Pertussis-Risiko durch eine adäquate Immunisierung bzw. Auffrischung minimieren, weswegen das Erreichen und Aufrechterhalten einer hohen Durchimpfungsrate durch rechtzeitigen und vollständigen Abschluss der Grundimmunisierungsserien und den anschließenden auf nationaler Ebene empfohlenen Auffrischungen von besonderer Bedeutung ist. Das ECDC stuft das Gesamtrisiko einer Pertussis-Infektion für nicht oder nur teilweise geimpfte Säuglinge im Alter von weniger als 6 Monaten als am höchsten ein, da sie die Gruppe mit der höchsten Morbidität und Mortalität durch Pertussis darstellen. Vor diesem Hintergrund ist insbesondere die Immunisierung von Müttern und aller Betreuungspersonen von Säuglingen (Cocooning) ein hochwirksamer Ansatz, um Krankheiten und Todesfälle bei Kleinkindern zu verhindern.2
1 Robert Koch-Institut (RKI). RKI-Ratgeber Keuchhusten (Pertussis); published online Feb 26, 2024.
URL: https://www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_Pertussis.html#doc2374534bodyText0 [08.07.2024]
2 European Centre for Disease Prevention and Control (ECDC). Increase of pertussis cases in the EU/EEA; published online May 8, 2024.
URL: https://www.ecdc.europa.eu/sites/default/files/documents/Increase%20in%20pertussis%20cases%20in%20the%20EU-EEA%20-%20May%202024%20FINAL.pdf [08.07.2024]
3 Nordholm A. C. et al. Pertussis epidemic in Denmark, August 2023 to February 2024. Euro Surveill 2024; 29(14):pii=2400160.
doi: 10.2807/1560-7917.ES.2024.29.14.2400160
4 Poeta M. et al. Pertussis outbreak in neonates and young infants across Italy, January to May 2024: implications for vaccination strategies. Euro Surveill 2024; 29(23):pii=2400301.
doi: 10.2807/1560-7917.ES.2024.29.23.2400301
14.08.2024
Antibiotikaresistenzen: Ihre Meinung ist gefragt!
Die zunehmende Resistenz gegen Antibiotika stellt das Gesundheitswesen vor große Herausforderungen. Um dieser Entwicklung entgegenzuwirken, haben das Robert Koch-Institut und das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) eine Umfrage gestartet.
Ziel ist es, einen umfassenden Einblick in die Verordnungspraxis von Antibiotika zu gewinnen. Die Online-Befragung richtet sich an medizinisches Fachpersonal aller Fachrichtungen, sowohl im
ambulanten als auch im stationären Bereich.
Die Teilnahme dauert nur etwa 8 Minuten und wurde bis zum 15.09.2024 verlängert. Jeder Beitrag hilft, die Herausforderung der Antibiotikaresistenzen besser zu verstehen und anzugehen.
Ihre Expertise ist gefragt - nehmen Sie teil und leisten Sie einen wichtigen Beitrag zur Gesundheitsvorsorge!
14.08.2024
Vogelgrippe-Virus A(H5N1) in Kuhmilch – Hitzeinaktivierung und Infektiosität bei Mäusen
Im März 2024 wurde erstmals das hochpathogene aviäre Influenza-Virus (highly pathogenic avian influenza virus, HPAI) des Subtyps H5N1 in Nasenabstrichen und Milch von Milchkühen nachgewiesen – ein Risiko, dass HPAI A(H5N1)-Viren in die menschliche Nahrungskette gelangen könnten. Das Texas A& M Veterinary Medical Diagnostic Laboratory untersuchte Milchproben von einer betroffenen Herde in New Mexico und isolierte daraus acht HPAI A(H5N1)-Viren.
Die Autoren verglichen die Sequenzierungsergbnisse dieser HPAI A(H5N1)-Milchvirus-Isolate mit öffentlich zugänglichen Datenbanken. Die von Kühen und aus Milch isolierten Viren bilden eine genetisch
verwandte Klade, die viele kleinere Kladen von Viren umfasst, die von Katzen, Waschbären, Hühnern und Wildvögeln isoliert wurden. Die Phylogenie ist konsistent mit einem einzigen Eintrag der Viren in
die untersuchte Herde. Die in dieser Studie isolierten Viren gehören zur Klade der bereits publizierten Sequenzen von aus anderen Kühen isolierten HPAI A(H5N1)-Viren, einschließlich eines
menschlichen Isolats, A/Texas/37/2024.
Studien zum Maul- und Klauenseuche-Virus zeigten, dass die Hitzedenaturierung von viruspositiven Milchproben in Folge eine natürlichen Infektion höhere Temperaturen oder längere Inkubationszeiten
(oder beides) erforderte als die Hitzedenaturierung von artifiziell mit Virus versetzter Milch, vermutlich weil Fettglobule und Kaseinmizellen die Viren in viruspositiven Milchproben infolge einer
natürlichen Infektion teilweise schützen könnten. Dementsprechend testeten die Autoren die Hitzedenaturierung von vier HPAI A(H5N1)-viruspositiven Milchproben (NM#93, NM#115, KS#3 und
KS#6).
Unverdünnte Milchproben wurden in einem PCR-Thermocycler bei 63 °C für 5, 10, 20 oder 30 Minuten oder bei 72 °C für 5, 10, 15, 20 oder 30 Sekunden inkubiert. Kontrollproben blieben unbehandelt. Die Hitzebehandlung bei 63 °C reduzierte die Virustiter unter die Nachweisgrenze des TCID50 (50 % tissue-culture infectious dose) Assays (1,5 log10/ml). Die Hitzebehandlung bei 72 °C wurde mit den Standardeinstellungen des PCR-Thermocyclers (d.h. vorgeheizter Deckel bei 105 °C) oder mit einem Metalldeckel (auf 72 °C erhitzt) durchgeführt, der den PCR-Block abdeckte. Nach der Hitzebehandlung wurden die Proben in embryonierte Hühnereier oder Madin-Darby-Hundeniere (MDCK)-Zellen zur Virusnachweis inokuliert. Unter diesen Bedingungen reduzierte die Hitzebehandlung für 15 oder 20 Sekunden die Virustiter um mehr als 4,5 Log-Einheiten, inaktivierte das Virus jedoch nicht vollständig. Die Autoren betonen, dass die in der Laborstudie verwendeten Bedingungen nicht identisch mit der großtechnischen industriellen Behandlung von Rohmilch sind.
Die Stabilität des HPAI A (H5N1)-Virus in Kuhmilch, die bei 4 °C gelagert wird, ist eine weitere wichtige Frage. Für die Milchprobe NM#93 wurde ein Rückgang von nur zwei Log-Einheiten über 5
Wochen festgestellt. HPAI A (H5N1)-Virus kann daher mehrere Wochen lang in roher Milch bei 4 °C infektiös bleiben.
Um das Risiko weiter zu bewerten, das HPAI A(H5N1)-positive Milch für Tiere und Menschen darstellt, wurden BALB/cJ-Mäuse oral mit 50 μl (3×10⁶ pfu) der Probe NM#93 inokuliert. Die Tiere zeigten ab Tag 1 Krankheitszeichen, darunter struppiges Fell und Lethargie. Alle Tiere überlebten bis Tag 4, an dem sie eingeschläfert wurden, um die Virustiter in mehreren Organen zu bestimmen.
Es wurden hohe Virustiter in den Atemwegen nachgewiesen (was darauf hindeutet, dass die Infektion über den Rachen erfolgt sein könnte) und moderate Virustiter in mehreren anderen Organen, was mit
den systemischen Infektionen übereinstimmt, die typischerweise durch HPAI H5-Viren bei Säugetieren verursacht werden. In den Milchdrüsen von zwei Mäusen zeigte sich eine hohe Viruslast - vergleichbar
mit der in der Kuhmilch -obwohl diese Mäuse nicht laktierend waren.
Folgerungen der Autoren
Zusammenfassend deuten die Daten darauf hin, dass HPAI A(H5N1)-Virus in unbehandelter Milch anfällige Tiere infizieren kann, die diese konsumieren. Zusammengefasst stellt HPAI H5-positive Milch ein
Risiko dar, wenn sie unbehandelt konsumiert wird, aber die Hitzedenaturierung unter den hier verwendeten Laborbedingungen reduziert die HPAI H5-Virustiter um mehr als 4,5 Log-Einheiten. Es ist jedoch
zu betonen, dass Laborversuche nicht die kommerziellen Pasteurisierungsprozesse widerspiegeln.
Kommentar der Herausgeber
Diese Studie zeigt, dass HPAI A(H5N1)-Virus in unbehandelter Milch infektiös bleibt und somit ein potenzielles Risiko für Tiere und Menschen darstellt. Eine Hitzebehandlung kann die Viruslast
erheblich reduzieren, jedoch ist weitere Forschung nötig, um die Wirksamkeit industrieller Pasteurisierungsmethoden zu bestätigen. Ein weiterer Grund, um vom Verzehr von Rohmilch abzuraten.
Guan, L. et al. Cow's Milk Containing Avian Influenza A(H5N1) Virus - Heat Inactivation and Infectivity in Mice. N Engl J Med. 2024;391(1):87-90. doi: 10.1056/NEJMc2405495
Nguyen, T.-Q. et al. Emergence and interstate spread of highly pathogenic avian influenza A(H5N1) in dairy cattle. bioRxiv [Preprint] 2024. doi: 10.1101/2024.05.01.591751
19.07.2024
Influenza A(H5N1)-Virusinfektion bei einem Milchviehhalter
Seit 2020 haben sich HPAI A(H5N1)-Viren der Klade 2.3.4.4b weltweit unter Wildvögeln ausgebreitet und zu Ausbrüchen bei Nutzgeflügel und anderen Tieren geführt. Kürzlich wurden Viren der Klade 2.3.4.4b in Milchkühen und in nicht pasteurisierten Milchproben in mehreren US-Bundesstaaten nachgewiesen. Die Autoren berichten über einen Fall einer HPAI A(H5N1) Virusinfektion bei einem Arbeiter auf einer Milchfarm in Texas.
Ende März 2024 entwickelte ein Milchfarmer Rötungen und Unbehagen im rechten Auge. Bei der Untersuchung am selben Tag wurden eine subkonjunktivale Blutung und dünner, seröser Ausfluss im rechten Auge
festgestellt. Die Vitalzeichen waren unauffällig, mit normaler Atemfunktion und einer Sauerstoffsättigung von 97 % bei Raumluft. Die Lungenauskultation war unauffällig. Fieber, Atemwegssymptomen,
Sehänderungen oder anderen Symptome lagen nicht vor. Der Arbeiter berichtete über keinen Kontakt mit kranken oder toten Wildvögeln, Geflügel oder anderen Tieren, jedoch über direkten und engen
Kontakt zu Milchkühen, die gesund erschienen, sowie zu kranken Kühen, die dieselben Krankheitsanzeichen wie Kühe auf anderen Milchfarmen in Nordtexas mit bestätigter HPAI A(H5N1)-Virusinfektion
zeigten (z.B. verminderte Milchproduktion, Appetitlosigkeit, Lethargie, Fieber und Dehydratation). Der Arbeiter gab an, beim Umgang mit Kühen Handschuhe zu tragen, aber keinen Atem- oder Augenschutz
zu verwenden.
Bindehaut- und Nasopharynx-Abstrichproben wurden vom rechten Auge für Influenzatests entnommen. Die Ergebnisse der Echtzeit-RT-PCR-Tests waren bei beiden Proben positiv für Influenza A- und A(H5)-Virus. Auf Basis des A(H5)-Ergebnisses wurde häusliche Isolation empfohlen und eine orale Behandlung mit Oseltamivir (75 mg zweimal täglich für 5 Tage) für den Arbeiter sowie zur Postexpositionsprophylaxe für die Haushaltskontakte des Arbeiters (gleiche Dosierung) verordnet. Am nächsten Tag berichtete der Arbeiter über keine Symptome außer Unbehagen in beiden Augen; bei einer erneuten Untersuchung zeigte sich eine subkonjunktivale Blutung in beiden Augen ohne Sehbeeinträchtigung. In den folgenden Tagen berichtete der Arbeiter über eine Besserung der Konjunktivitis. Atemwegssymptome traten auch im Verlauf nicht auf. Die Haushaltskontakte blieben gesund.
Auf Basis der Echtzeit-RT-PCR und Sequenzierung bestätigten die Centers for Disease Control and Prevention eine HPAI A(H5N1)-Virusinfektion in den am Tag des Symptombeginns entnommenen Bindehaut- und Nasopharynx-Abstrichproben. Zusätzliche klinische Proben für Influenzatests waren nicht verfügbar. Obwohl virale RNA aus der Nasopharynx-Abstrichprobe (Ct-Wert 33) unzureichende PCR-Amplifikate für die Sequenzierung ergab, bestätigten die vollständige Genomsequenzen aus der Bindehautabstrichprobe (Ct-Wert 18), dass das Virus zur Klade 2.3.4.4b (Genotyp B3.13) gehörte, und die erfolgreiche Virusisolierung aus beiden Abstrichproben ergab identische Viren. Alle Genabschnitte waren eng verwandt mit Viren, die in texanischen Milchkühen isoliert wurden und Genotyp B3.13 Viren, die in Wildvögeln in Texas im März 2024 nachgewiesen wurden. Sequenzdaten von vermutlich infizierten Kühen auf der Farm, auf der der Arbeiter tätig war, standen nicht zur Analyse zur Verfügung.
Virensequenzen von Kühen und vom Arbeiter wiesen hauptsächlich aviäre genetische Merkmale auf – es gab keine Veränderungen im Hämagglutinin-Gen, das die Rezeptorbindungsspezifität beeinflusst (z.B. Bindung an α2-6-verknüpfte Sialinsäure-Rezeptoren, die hauptsächlich im oberen menschlichen Respirationstrakt vorkommen) und das Übertragungsrisiko auf Menschen erhöhen könnte. Das im Abstrich des Arbeiters identifizierte Virus wies eine Mutation (PB2 E627K) auf, die mit der viralen Anpassung an Säugetierwirte assoziiert ist und zuvor bei Menschen und anderen Säugetieren, die mit HPAI A(H5N1)-Viren und anderen aviären Influenza A-Virus Subtypen infiziert waren, nachgewiesen wurde, einschließlich A(H7N9) und A(H9N2). Es wurden keine genetischen Marker gefunden, die mit einer verminderten Empfindlichkeit gegenüber von Neuraminidase-Inhibitoren assoziiert sind. Das Hämagglutinin des Virus war eng verwandt mit den zwei möglichen Virusisolaten für eine Impfstoffproduktion. Da Influenza A(H5N1)-Viren pandemisches Potenzial haben, stehen diese Impfviren den Herstellern zur Verfügung und könnten bei Bedarf zur Impfstoffproduktion verwendet werden.
Kommentar der Herausgeber
Dieser Fallbericht unterstreicht die Bedeutung der Überwachung von Zoonosen und der Einhaltung von Schutzmaßnahmen im Umgang mit potenziell infizierten Tieren. Die schnelle Diagnose und Behandlung
sowie die Einbindung von Haushaltskontakten sind entscheidend, um das Risiko einer weiteren Ausbreitung zu minimieren.
Uyeki, T. M. et al. Highly Pathogenic Avian Influenza A(H5N1) Virus Infection in a Dairy Farm Worker. N Engl J Med. 2024;390(21):2028-2029. doi: 10.1056/NEJMc2405371
19.07.2024
Erhöhte Inzidenz von Mycoplasma pneumoniae-Infektionen in den Niederlanden, Frankreich und den USA (2023-2024)
Mycoplasma pneumoniae ist eine häufige Ursache für Infektionen der unteren und oberen Atemwege, insbesondere bei Kindern und jungen Erwachsenen. Charakteristisch sind auch extrapulmonale Symptome wie Erythema exsudativum multiforme und Enzephalitis. Es ist bekannt, dass durch M. pneumoniae verursachte Epidemien weltweit alle paar Jahre auftreten, wobei die letzte Epidemie in einigen europäischen Ländern im Jahr 2019/20 beobachtet wurde. Nach mehreren Jahren mit niedrigen Nachweisraten während der COVID-19 Pandemie wurde in den letzten Monaten des Jahres 2023 ein starker lokaler Anstieg der M.-pneumoniae-Nachweise sowie der M.-pneumoniae-bedingten Einweisungen in verschiedenen Regionen beobachtet.
Die nachfolgende niederländische Studie berichtet über den aktuellen Aufwärtstrend bei den M.-pneumoniae-Nachweisen in einem niederländischen Regionalkrankenhaus und vergleicht diesen mit
den nationalen und europäischen Trends. Um einen detaillierteren Einblick in die aktuelle Epidemiologie von M. pneumoniae zu gewinnen, wurden Daten aus dem Regionalen Gesundheitslabor
Kennemerland (Regional Public Health Laboratory Kennemerland/RPHLK) verwendet. Die Anzahl der M. pneumoniae-Nachweise (von 2017 bis 2023, 257 Nachweise aus 19.989 Tests) und
Krankenhausaufnahmen sowie demografische Daten der Patienten (Alter, Geschlecht, Aufnahmeanlass, Aufenthaltsdauer, Aufnahme auf eine Intensivstation (ICU) und weitere Infektionen) wurden gesammelt.
Eine Krankenhausaufnahme im Zusammenhang mit M. pneumoniae wurde definiert als der Nachweis von M. pneumoniae in einem naso- und/oder oropharyngealen (naso- and/or oropharyngeal
/NP/OP) Abstrich mittels PCR-Tests bis zu zwei Tage vor oder während der Aufnahme. Die aktuellen Daten wurden mit denen von 2019 und 2020, der letzten Periode mit lokal erhöhter M.
pneumoniae-Nachweisrate, verglichen.
Ein starker Anstieg der regionalen M. pneumoniae-Nachweise im Jahr 2023 begann im Oktober. Im Jahr 2023 wurden 133 Patienten mit M. pneumoniae-positiver PCR im Spaarne Gasthuis
(niederländische Klinik) festgestellt, mit einem Medianalter von 28 Jahren. 41,3 % Patienten waren jünger als 18 Jahre, wobei die meisten Kinder in der Alterskategorie 5-11 Jahre waren (n = 27). Bei
Erwachsenen wurden die meisten Nachweise in den jüngsten Alterskategorien gefunden: 18-29 Jahre (n = 16) und 30-39 Jahre (n = 22). Der Vergleich der M. pneumoniae-PCR-Positivität zwischen
2023 (4,1 %; 133/3.227) und 2019/2020 (1,0 %; 68/6.889) zeigte einen signifikanten Anstieg (p < 0,001).
Von den 133 Patienten wurden 81 (60,9 %) stationär aufgenommen, darunter 30 Kinder (37,0 %). Drei Patienten hatten extrapulmonale Manifestationen, alle anderen Patienten wurden mit einer Pneumonie
aufgenommen. Die mediane Hospitalisationsdauer betrug vier Tage und war bei Kindern deutlich kürzer als bei Erwachsenen (2,5 vs. 5 Tage; p < 0,001). Neun erwachsene Patienten (11,1 %) wurden auf
der Intensivstation aufgenommen, meist (n = 7) wegen Hypoxie, von denen drei mechanisch beatmet werden mussten. Vier Patienten wiesen Begleiterkrankungen auf, die möglicherweise zur Einweisung in die
Intensivstation beitrugen (d.h. Lungenkrebs, Herz-Kreislauf-Erkrankungen, Diabetes, Alkohol- und Drogenkonsum sowie neurologische Erkrankungen). 24 (18,0 %) Patienten mit M. pneumoniae
wiesen eine Koinfektion auf, insbesondere mit Rhinoviren (n = 10) und respiratorischen Synzytialviren (RSV) (n = 6) ohne Unterschied zwischen Kindern und Erwachsenen.
Im Vergleich dazu wurde M. pneumoniae in den Jahren 2019 und 2020 insgesamt nur 68-mal nachgewiesen. In diesen Jahren war das mediane Alter signifikant höher: 40 Jahre im Vergleich zu 28
Jahren im Jahr 2023 (p = 0,005). Im Jahr 2023 wurde ein höherer Prozentsatz an Hospitalisationen beobachtet, obwohl knapp statistisch nicht signifikant (p = 0,085); auch der Prozentsatz der
Einweisungen auf der Intensivstation und die Hospitalisationsdauer unterschieden sich nicht signifikant. Auch national gab es Ende 2023 einen steilen Anstieg von M. pneumoniae und weitaus
mehr Fälle als in den Jahren 2019 und 2020.
Eine weitere Studie aus Frankreich berichtet ebenfalls über einen großflächigen Ausbruch von M. pneumoniae-Infektionen der Atemwege mit 218 Fällen (0,8 % von 26.449 getesteten Patienten) in
den Jahren 2023-2024 in Marseille. Das Bakterium zirkulierte ebenfalls vor allem bei Kindern im Alter von < 15 Jahren.
Auch aus den Vereinigten Staaten wurde von einem landesweiten Ausbruch besonders in großen urbanen Zentren von M.-pneumoniae-Infektionen in der ambulanten Bevölkerung im Jahr 2023 berichtet.
Die COVID-19-Pandemie hat die Saisonalität und die epidemiologische Landschaft verschiedener Erreger der Atemwege, einschließlich M. pneumoniae, verändert. Die Erhebungsdaten zeigen, dass
der jüngste Ausbruch von M. pneumoniae mit seiner höheren Prävalenz in der jüngeren Bevölkerung (0-20 Jahre) im Vergleich zu anderen Altersgruppen mit den Ausbrüchen des Erregers vor der
Pandemie vergleichbar ist. Andere respiratorische Erreger waren ähnlich häufig bei Patienten mit und ohne M. pneumoniae Nachweis. Die ICD10-Diagnosecodes erwiesen sich bei der korrekten
Feststellung von Atemwegsinfektionen bei einem Patienten als hochspezifisch, zeigten jedoch eine geringere Sensitivität bei der Identifizierung des verursachenden Organismus. Die ICD10 Kodierungen
deuten darauf hin, dass M. pneumoniae vorwiegend mit Infektionen der oberen Atemwege assoziiert war. Die COVID-19-Pandemie machte die Lücken in den öffentlichen Gesundheitsressourcen der
Vereinigten Staaten deutlich und unterstrich die Notwendigkeit, den Erreger von Atemwegsinfektionen korrekt zu identifizieren, um die Ausbreitung der Infektion und die Auswirkungen auf die
Lebensqualität der Bevölkerung zu minimieren. Angesichts der zunehmenden Bekanntheit der PCR als schnelle und zuverlässige Diagnosemethode zum Nachweis viraler und bakterieller Erreger unterstützt
diese Studie die kontinuierliche Überwachung häufiger und atypischer Erreger der Atemwege als Maßnahme der öffentlichen Gesundheit.
Folgerungen der Autoren
Die drei Studien dokumentieren einen starken Anstieg von M. pneumoniae Infektionen in Europa und Nordamerika, der Ende 2023 begonnen hat mit höheren Fallzahlen als in den letzten und
insbesondere den pandemischen Jahren. Sie zeigen die Bedeutung der Überwachung und Früherkennung von M. pneumoniae-Infektionen, um rechtzeitig geeignete Maßnahmen zu ergreifen und die
öffentliche Gesundheit zu schützen. Um die derzeitige erhöhte Inzidenz genauer zu verstehen, sind Daten z.B. über den Schweregrad, zirkulierende Stämme und die Häufigkeit von Makrolidresistenz
wichtig.
Kommentar der Herausgeber
Die Mykoplasmen-Epidemiologie ist noch nicht gut verstanden. Diese Ausbruchsberichte sind wichtig, weil sie die Bedeutung von Surveillance unterstreichen und das Bewusstsein für diese oft protrahiert
verlaufenden Infektionen schärfen, die derzeit stark gehäuft auftreten. Ob immer Antibiotika notwendig sind, wird derzeit untersucht. Aus therapeutischer Sicht Doxycyclin gegenüber Makroliden bei
diesen Infektionen zu bevorzugen, weil Makrolidresistenzen global zunehmen. Auch empirisch ist Doxycyclin eine gute Option bei ambulant erworbenen Atemwegsinfektionen einschließlich Pneumonien.
Bolluyt, D. C. et al. Increased incidence of Mycoplasma pneumoniae infections and hospital admissions in the Netherlands, November to December 2023. Euro Surveill. 2024;29(4):2300724.
doi: 10.2807/1560-7917.ES.2024.29.4.2300724
Edouard, S. et al. Large-Scale Outbreak of Mycoplasma pneumoniae Infection, Marseille, France, 2023-2024; Emerg Infect Dis. 2024;30(7), published online first.
Upadhyay, P. et al. Mycoplasma pneumoniae Outbreak in 2023: Post-pandemic Resurgence of an Atypical Bacterial Pathogen. Cureus. 2024;16(4):e58757.
doi: 10.7759/cureus.58757
19.06.2024
Information zum Start des Härtefallprogramms zu Aztreonam/Avibactam (Emblaveo®)
Emblaveo® zur Behandlung von erwachsenen Patienten und Patientinnen mit komplizierten intraabdominellen Infektionen, nosokomial erworbenen Pneumonien – einschließlich beatmungsassoziierten Pneumonien – sowie komplizierten Harnwegsinfektionen, Pyelonephritis einbegriffen, wird nach aktuellem Stand im September 2024 in den deutschen Markt eingeführt. Um die Zeit bis zur Markteinführung zu überbrücken, hat Pfizer ein Härtefallprogramm für Aztreonam-Avibactam eingerichtet, dem das BfArM in Deutschland zugestimmt hat.
Weitere Informationen sind in der Übersicht der aktuell laufenden und bestätigten Arzneimittel-Härtefallprogramme des BfArM verfügbar: BfArM - Compassionate Use - Aktuell laufende und bestätigte Arzneimittel-Härtefallprogramme.
Eine Behandlung kann nur erfolgen, wenn nach definierten Kriterien nachgewiesen wird, dass keine zugelassenen Therapieoptionen für eine zufriedenstellende Behandlung der Infektion verfügbar sind.
Ärztinnen und Ärzte, die die Teilnahme einer Patientin oder eines Patienten planen, werden gebeten, eine entsprechende Anfrage direkt an Clinigen Healthcare Ltd., einem Spezialisten für die
Durchführung von Early Access Programmen, zu richten. Dies ist auf zwei Wegen möglich:
1. Per E-Mail an medicineaccess@clinigengroup.com, oder
2. Direkt über das Online-Portal ClinigenDirect: Log In (clinigengroup.com)
Für die Dokumentation aller patientenrelevanten Daten und die Bewertung der Eignung ist in jedem Fall eine Anmeldung über ClinigenDirect notwendig.
19.06.2024
Update | Vancomycin-resistenten Enterococcus faecium (VRE) vanA ST612 in der Schweiz
Im März informierten wir Sie bereits über die interregionale Verbreitung und die dazugehörigen Maßnahmen von Vancomycin-resistenten Enterococcus faecium (VRE) in der Schweiz. Gerne möchten wir Ihnen ein Update über die momentane Situation geben.
Bitte beachten Sie das untenstehende Dokument mit allgemeinen Informationen und aktualisierten Empfehlungen.
Zum Berich [Stand: 31. Mai 2024]
19.06.2024
Wirksamkeit und Sicherheit von Azithromycin bei unteren Atemwegsinfektionen mit niedrigem Procalcitonin-Wert
Infektionen der unteren Atemwege werden häufig mit Antibiotika behandelt, obwohl in vielen Fällen eine virale Ursache vorliegt. Es ist unklar, ob niedrige Procalcitonin-Spiegel Patienten unteren Atemwegsinfektionen identifizieren können, die nicht von Antibiotika profitieren. In der nachfolgend vorgestellten Studie wurde die Wirksamkeit und Sicherheit von Azithromycin gegenüber Placebo bei der Behandlung unteren Atemwegsinfektionen bei Patienten mit niedrigem Procalcitonin untersucht.
Hierzu wurde eine randomisierte, doppelblinde, Studie in fünf US-Studienzentren durchgeführt. Eingeschlossen wurden Erwachsene mit klinischem Verdacht auf eine nicht-pneumonische Infektion der
unteren Atemwege – also einer Bronchitis – und einer Symptomdauer von mindestens 24 Stunden bis maximal 28 Tagen. Patienten mit einer Procalcitonin-Konzentration von 0,25 ng/ml oder weniger wurden
nach dem Zufallsprinzip (1:1) mit Stratifizierung nach Standort entweder einer oralen Azithromycin-Gabe von 500 mg an Tag 1, gefolgt von 250 mg täglich über 4 Tage oder einem entsprechenden Placebo
zugeteilt. Der primäre Endpunkt war die Wirksamkeit von Azithromycin im Vergleich zu Placebo in Bezug auf die klinische Verbesserung an Tag 5 in der Intention-to-Treat-Population. Die
Nichtunterlegenheitsmarge betrug 12,5 %. Unerwünschte Ereignisse wie Bauchschmerzen, Erbrechen, Durchfall, allergische Reaktionen oder Hefepilzinfektionen wurden als sekundärer Endpunkt erfasst.
Zwischen Dezember 2017 und März 2020 wurden 691 Patienten gescreent, 499 wurden eingeschlossen und nach dem Zufallsprinzip entweder Azithromycin (n = 249) oder Placebo (n = 250) zugewiesen. Eine
klinische Verbesserung an Tag fünf wurde bei 148 (63 %) von 238 Teilnehmenden mit vollständigen Daten in der Placebogruppe und bei 155 (69 %) von 227 Teilnehmenden mit vollständigen Daten in der
Azithromycin-Gruppe in der Intention-to-Treat-Analyse beobachtet. Die unerwünschten Ereignisse und der Schweregrad der unerwünschten Ereignisse unterschieden sich am Tag fünf nicht signifikant
zwischen den Gruppen, mit Ausnahme von verstärkten Bauchschmerzen unter Azithromycin 47 von 204 Teilnehmenden im Vergleich zu Placebo 35 von 221.
Folgerungen der Autoren
Placebo war bei Erwachsenen mit einer Infektion der unteren Atemwege und einer niedrigen Procalcitonin-Konzentration im Hinblick auf die klinische Verbesserung an Tag fünf nicht schlechter als
Azithromycin. Unter Berücksichtigung sowohl der Raten der klinischen Verbesserung als auch der unerwünschten Ereignisse an Tag fünf ist unklar, ob Antibiotika bei Patienten mit unteren
Atemwegsinfektionen und niedrigem Procalcitonin indiziert ist.
Kommentar der Herausgeber
Diese Studie unterstützt das Konzept, dass bei Erwachsenen mit Atemwegsinfektionen und niedrigem Procalcitonin auf Antibiotika verzichtet werden kann, ohne das Risiko für schlechteren Verlauf zu
erhöhen.
Tsalik, E. L. et al. Efficacy and safety of azithromycin versus placebo to treat lower respiratory tract infections associated with low procalcitonin: a randomised, placebo-controlled, double-blind, non-inferiority trial. Lancet Infect Dis. 2023;23(4):484-495. doi: 10.1016/S1473-3099(22)00735-6
22.05.2024
INFEKTIO_podcast | Das Masernvirus - Der lange Weg zur Masern-Elimination
In der aktuellen Episode ihrer Podcast-Reihe „Wissenschaft trifft Praxis“ beleuchtet Sybille Somogyi die momentane Situation rund um das Masernvirus. Als Referentin für Infektionsschutz und Hygiene spricht sie mit ihren Gästen, Prof. Dr. Annette Mankertz und Dr. Dorothea Matysiak-Klose, über den Fortschritt bei der Eliminierung der Masern in Deutschland. Zudem thematisieren sie, ob die endemische Übertragung des Masernvirus dauerhaft unterbrochen werden kann und wie man eine Impfreaktion von einer tatsächlichen Masernerkrankung unterscheiden kann.
22.05.2024
Aztreonam-Avibactam – ein neues Antibiotikum zur Bekämpfung von Infektionen mit multiresistenten Bakterien
Die European Medicines Agency (EMA) hat empfohlen, eine Marktzulassung in der Europäischen Union (EU) für Emblaveo (Aztreonam-Avibactam) zu gewähren. Das Medikament ist indiziert zur Behandlung
von komplizierten intraabdominalen und Harnwegsinfektionen, nosokomialer Pneumonie und Infektionen, die durch bestimmte Arten von Bakterien (aerobe Gram-negative) verursacht werden, wenn
Behandlungsoptionen begrenzt sind.
Infektionen durch multi-resistente Gram-negative Bakterien, stellen ein ernstes Problem für die öffentliche Gesundheit dar, da die Patienten nur begrenzte oder manchmal gar keine
Behandlungsmöglichkeiten haben. Infektionen durch multiresistente Bakterien verursachen in der EU schätzungsweise 35.000 Todesfälle pro Jahr.
Emblaveo ist eine fest-dosierte Kombination von zwei Wirkstoffen, Aztreonam und Avibactam. Aztreonam ist bereits einzeln für die Anwendung in der EU zugelassen, und Avibactam ist für die Anwendung in
Kombination mit einem anderen Antibiotikum (Ceftazidim) zugelassen. Aztreonam ist ein Monobactam-Antibiotikum, das zur Gruppe der β-Lactame gehört. Es verhindert, dass die Bakterien ihre Zellwände
aufbauen und ist gegenüber den β-Lactamasen der Ambler Klasse B (Metallo-β-Lactamasen, MBL) stabil.
Avibactam blockiert die Wirkung vieler β-Lactamasen der Ambler-Klassen A, C und D. Diese Enzyme ermöglichen es den Bakterien, β-Lactam-Antibiotika wie Aztreonam abzubauen, wodurch sie gegen die
Wirkung des Antibiotikums resistent werden. Durch die Blockierung dieser Enzyme stellt Avibactam die Wirkung von Aztreonam gegen Aztreonam-resistente Bakterien wieder her.
Emblaveo kann als Infusion verabreicht werden.
Der Ausschuss für Humanarzneimittel (Committee for Medicinal Products for Human Use / CHMP) der EMA hat festgestellt, dass die Vorteile von Emblaveo die Risiken für Patienten mit Infektionen durch
Gram-negative Bakterien überwiegen, wenn es nur wenige therapeutischen Optionen gibt. Aztreonam hat sich als wirksam bei der Behandlung einer Reihe schwerwiegender Infektionen erwiesen.
Mikrobiologische Daten deuten darauf hin, dass Aztreonam in Kombination mit Avibactam bei Infektionen durch viele multi-resistente Gram-negative Erreger wirksam sein wird.
Emblaveo wurde im Rahmen des beschleunigten Bewertungsverfahrens der EMA evaluiert, da es als eine Substanz von erheblichem öffentlichem Gesundheitsinteresse angesehen wird.
Die Empfehlung der EMA basiert auf den bereits verfügbaren Sicherheits- und Wirksamkeitsdaten für jeden Wirkstoff sowie den Ergebnissen zweier randomisierter Phase-III-Studien, die vom Hersteller
eingereicht wurden. Die Studien waren nicht darauf ausgelegt, Wirksamkeit nachzuweisen, liefern jedoch Sicherheitsdaten für die Kombination. Dies entspricht den Leitlinien der EMA, die einen
flexiblen Ansatz bei der Entwicklung neuer Antibiotika ermöglichen, die auf multiresistente Erreger abzielen. Die häufigsten Nebenwirkungen von Emblaveo waren Anämie, erhöhte Lebertransaminasen und
Durchfall. Dies steht im Einklang mit den dokumentierten Sicherheitsinformationen für jede der beiden Einzelsubstanzen.
Die vom CHMP verabschiedete Stellungnahme ist ein Zwischenschritt in der Zulassung. Die Stellungnahme wird nun an die Europäische Kommission weitergeleitet, um eine Entscheidung über eine EU-weite
Marktzulassung zu treffen. Sobald eine Marktzulassung erteilt wurde, werden Entscheidungen über Preis und Erstattung auf der Ebene jedes Mitgliedstaats getroffen, wobei die potenzielle Rolle oder
Verwendung dieses Arzneimittels im Rahmen des nationalen Gesundheitssystems des jeweiligen Landes berücksichtigt wird.
Folgerung der Autoren
Emblaveo, eine Kombination aus Aztreonam und Avibactam, hat das Potenzial, eine Lücke in der Behandlung schwerer Infektionen durch MRGN zu schließen. Die Sicherheits- und Wirksamkeitsdaten sowie Phase-III-Studien stützen diese Empfehlung, obwohl sie primär auf Sicherheit abzielen und nicht speziell die Wirksamkeit nachweisen. Die Durchführung einer beschleunigten Bewertung reflektiert die Dringlichkeit dieser Situation. Auch wenn die Empfehlung einen Schritt in Richtung Zulassung darstellt, müssen noch weitere Entscheidungen bezüglich der Preisgestaltung und Erstattung getroffen werden.
European Medicines Agency (EMA). New antibiotic to fight infections caused by multidrug-resistant bacteria. published online Mar 22, 2024. URL: https://www.ema.europa.eu/en/news/new-antibiotic-fight-infections-caused-multidrug-resistant-bacteria [23.04.2024]
24.04.2024
Zwei Impfstoffe gegen Influenza A (H5N1) zur Zulassung empfohlen
Der Ausschuss für Humanarzneimittel (CHMP) der europäischen Arzneimittelagentur (EMA) hat sich in seiner Sitzung vom 22. Februar 2024 für die Zulassung von zwei Impfstoffen gegen den Influenza-Subtyp A (H5N1) ausgesprochen. Celldemic® und Incellipan® von der Firma Sequirus sollen zur aktiven Immunisierung gegen H5N1 („Vogelgrippe“) bei Erwachsenen und Säuglingen ab sechs Monaten eingesetzt werden können.1,2
Mit dem Begriff „Vogelgrippe“ ist in erster Linie die aviäre Influenza gemeint, eine durch Influenza-A-Viren bei Vögeln ausgelöste Erkrankung. Die Zirkulation verschiedener H5-Viren, darunter die für Vögel hochpathogenen Influenza-Viren A(H5N1), A(H5N8) und A(H5N6), hat in der Vergangenheit wiederholt zu Ausbrüchen in Wildvogel- und Geflügelpopulationen, teilweise auch bei Säugetieren, geführt. Typischerweise ist die Übertragungsrate dieser Viren auf den Menschen eher gering, allerdings kann eine erfolgte Infektion zu schweren Krankheitsverläufen führen. In Deutschland wurden bislang keine Fälle von aviärer Influenza beim Menschen gemeldet. Nach Angaben der Weltgesundheitsorganisation wurden weltweit seit 2003 über 2600 humane Erkrankungen und 1100 Todesfälle mit aviärer Influenza verzeichnet.3
Bei Celldemic® und Incellipan® handelt es sich um adjuvantierte Proteinimpfstoffe, die 7,5 µg der Oberflächenantigene Hämagglutinin (H) und Neuraminidase (N) pro Dosis enthalten. Hämagglutinin und Neuraminidase sind beim natürlichen Virus essenziell für das Eindringen in die Wirtszelle und die Freisetzung neu gebildeter Viruspartikel. Beide Glykoproteine kommen in unterschiedlichen Varianten vor (H1, H2, etc.), anhand derer die Einteilung der Influenza-A-Viren in die verschiedenen Subtypen erfolgt. Für die beiden Impfstoffe werden diese Antigene aus inaktivierten A/turkey/Turkey/1/2005 (H5N1)-ähnlichen Viren (NIBRG 23) gewonnen, die in Madin-Darby-Canine-Kidney (MDCK)-Zellkulturen gezüchtet werden. Um die Immunantwort zu verstärken, wird das Adjuvans M59C.1 eingesetzt. Für die Ausbildung einer robusten Immunantwort, ist die Applikation von zwei Impfstoffdosen im Abstand von drei Wochen erforderlich.1-4
Der Unterschied zwischen den beiden Impfstoffen liegt in ihrem vorgesehenen Einsatzzeitpunkt. Während Celldemic® als zoonotischer Influenza-Impfstoff künftig bereits zum Einsatz kommen soll, wenn bei Ausbrüchen der aviären Influenza eine mögliche Pandemie erwartet wird (präpandemisch), soll Incellipan® als Influenza-Pandemieimpfstoff nur bedingt zugelassen werden. Letzteres bedeutet, dass Incellipan® erst verwendet werden darf, wenn die Grippepandemie offiziell ausgerufen wurde (pandemisch). In diesem Fall erfolgt auf Grundlage der Musterzulassung eine Anpassung des Impfstoffs an den pandemieauslösenden Virusstamm und die „endgültige“ Zulassung kann in einem beschleunigten Verfahren schneller durchlaufen werden, da die Qualität, Sicherheit und Wirksamkeit bereits mit anderen potenziellen Pandemiestämmen geprüft wurden.1,2,5
Mit beiden Impfstoffen konnte eine robuste Immunantwort bei Erwachsenen und Kindern drei Wochen nach der Verabreichung der zweiten Impfstoffdosis erreicht werden. Celldemic® und Incellipan® sind gut verträglich, bei Erwachsenen traten nach der Impfung am häufigsten lokale Reaktionen wie Schmerzen an der Injektionsstelle und allgemeine Symptome wie Müdigkeit, Kopfschmerzen, Unwohlsein sowie Muskel- und Gelenkschmerzen auf. Ähnliche Reaktionen zeigten sich auch bei Kindern, dabei wurde zusätzlich auch über Appetitlosigkeit, Übelkeit, Fieber, Reizbarkeit und Veränderung der Essgewohnheiten berichtet.1,2
Auch wenn derzeit nicht davon ausgegangen wird, dass sich die aviäre Influenza zeitnah zu einem Pandemierisiko für die Allgemeinbevölkerung entwickelt, werden dennoch entsprechende Vorbereitungen getroffen. Celldemic® und Incellipan® sind aber nicht die ersten Impfstoffe für den präpandemischen bzw. pandemischen Einsatz. Ein Vorteil der neuen Impfstoffkandidaten liegt jedoch vor allem in der Skalierbarkeit der Produktion, wodurch im Vergleich zur Virusvermehrung in Hühnereiern in kürzerer Zeit größere Mengen Impfstoff produziert werden könnten. Durch die Verwendung von Säugetierzellkulturen wird wegen der höheren Ähnlichkeit zum humanen Wirtsorganismus eine geringere Virusmodifikation und damit eine gesteigerte Impfstoffwirksamkeit angenommen.6
Für die endgültige Zulassung ist noch die Zustimmung der EU-Kommission ausstehend. Doch auch dann ist der zukünftige Einsatz beider Vakzine noch ungewiss. Laut aktuellen Empfehlungen des Robert-Koch-Instituts sollen Personen mit einem erhöhten Expositionsrisiko durch aviäre Influenza A lediglich gegen humane Influenzaviren geimpft werden.7
1 European Medicines Agency (EMA). Celldemic – summary of opinion. EMA/71755/2024; published online Feb 23, 2024. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-celldemic_en.pdf
2 European Medicines Agency (EMA). Incellipan – summary of opinion. EMA/71759/2024; published online Feb 23, 2024. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-incellipan_en.pdf
3 Robert Koch Institut (RKI). RKI zu humanen Erkrankungen mit aviärer Influenza (Vogelgrippe); published online Nov 6, 2023. URL: https://www.rki.de/DE/Content/InfAZ/Z/ZoonotischeInfluenza/Vogelgrippe.html [11.04.2024]
4 Robert Koch Institut (RKI). Influenza (Teil 1): Erkrankungen durch saisonale Influenzaviren- RKI-Ratgeber; published online Jan 19, 2018. URL: https://www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_Influenza_saisonal.html [11.04.2024]
5 European Medicines Agency (EMA). Vaccines for pandemic influenza; published online. URL: https://www.ema.europa.eu/en/human-regulatory-overview/public-health-threats/pandemic-influenza/vaccines-pandemic-influenza [11.04.2024]
6 Gärtner, B. C. et al. Zellkulturbasierte Influenzaimpfstoffe: eine effektive Impfstoffoption für unter 60-Jährige. Wien Klin Wochenschr 2024;136(Suppl 2):35-42. doi: 10.1007/s00508-024-02327-3
7 Robert Koch Institut (RKI). Empfehlungen des Robert Koch-Instituts zur Prävention bei Personen mit erhöhtem Expositionsrisiko durch (hochpathogene) aviäre Influenza A/H5; published
online Feb 23, 2024. URL: https://www.rki.de/DE/Content/InfAZ/Z/ZoonotischeInfluenza/Empfehlungen_1.pdf?__blob=publicationFile [11.04.2024]
24.04.2024
Internationaler Tag der Händehygiene am 5. Mai 2024
Zu einem der wichtigsten Infektionspräventionsmaßnahmen gehört die Händehygiene. Aus diesem Grund wird jedes Jahr am 5. Mai die Aufmerksamkeit auf den Internationalen Tag der Händehygiene gelenkt, um das Bewusstsein für die Bedeutung der Händehygiene bei der Verhinderung von Infektionen zu stärken. Händewaschen ist eine einfache, aber wirksame Methode zur Prävention und Verringerung der Übertragung von Krankheitserregern, wie Viren und Bakterien, die Infektionen verursachen können. Dies ist besonders wichtig in Gesundheitseinrichtungen, in denen Patient:innen, Mitarbeitende und Besuchende einem erhöhten Risiko für Infektionen ausgesetzt sein können. Das Datum des 5.5. soll hierbei die fünf Finger jeder Hand symbolisieren.
Auch in diesem Jahr begleitet die WHO den 5. Mai mit der Kampagne „SAVE LIVES: Clean Your Hands” (RETTE LEBEN: säubere deine Hände). Der diesjährige Slogan lautet „Why is sharing knowledge about hand hygiene still so important? Because it helps stop the spread of harmful germs in healthcare.” („Warum ist die Vermittlung von Wissen über die Händehygiene immer noch so wichtig? Weil sie dazu beiträgt, die Ausbreitung schädlicher Keime im Gesundheitswesen zu verhindern.“).
Die Ziele des World Hand Hygiene Day 2024 sind:
- Stärkung von Lernkonzepten, um die Durchführung innovativer und effektiver Schulungen zu ermöglichen, die das Gesundheits- und Pflegepersonal in die Lage versetzen, die Händehygiene und IPC (Infection Prevention and Control) vor Ort durch verbesserte Kenntnisse, Fähigkeiten und Verhaltensweisen zu verbessern.
- Förderung des Zugangs zu innovativen Schulungsressourcen für Händehygiene und IPC für Beschäftigte im Gesundheits- und Pflegebereich.
- Sensibilisierung für die Bedeutung von Wissen und Lernen über Händehygiene zum richtigen Zeitpunkt, um verschiedene Infektionskrankheiten zu verhindern.
- Förderung von Mess- und Evaluierungsmechanismen zur Bewertung der Auswirkungen von Schulungen und Fortbildungen zu IPC-Standards und -Praktiken, einschließlich der Händehygiene und ihren Auswirkungen auf die Prävention von Healthcare-Associated Infections (HAI) und Antimicrobial Resistance (AMR).
24.4.2024
Ceftriaxon zur Verhinderung einer frühen beatmungsbedingten Lungenentzündung bei Patienten mit akuter Hirnverletzung
Bei Patienten mit akuter Hirnverletzung besteht ein hohes Risiko einer beatmungsassoziierten Pneumonie (ventilator-associated pneumonia/VAP). Der Nutzen einer kurzen Antibiotikaprophylaxe ist nach wie vor umstritten. Das Ziel in der nachfolgenden vorgestellten Studie war es, die Wirkung einer frühen Einzeldosis des Antibiotikums Ceftriaxon auf das Auftreten einer frühen VAP bei Patienten mit schweren Hirnverletzungen, die mechanisch beatmet werden mussten, zu untersuchen.
Hierzu wurde eine multizentrische und randomisierte Studie in acht französischen Universitätskliniken durchgeführt. Nach dem Zufallsprinzip wurden komatöse (Glasgow Coma Scale score [GCS] ≤ 12)
erwachsene Patienten (Alter ≥ 18 Jahre), die nach einer akuten Hirnverletzung mindestens 48 Stunden lang mechanisch beatmet werden mussten, innerhalb der ersten 12 Stunden nach der Trachealintubation
einmalig mit 2 g Ceftriaxon oder Placebo behandelt. Die Patienten erhielten keine selektive Dekontamination des Oropharynx und des Verdauungstrakts. Der primäre Endpunkt war der Anteil der Patienten,
die zwischen dem 2. und 7. Tag der mechanischen Beatmung eine frühe VAP entwickelten, die von maskierten Prüfern bestätigt wurde. Die Analyse wurde in der modifizierten Intention-to-Treat-Population
durchgeführt, die alle nach dem Zufallsprinzip zugewiesenen Patienten umfasste.
Von Oktober 2015 bis Mai 2020 wurden 345 Patienten nach dem Zufallsprinzip (1:1) Ceftriaxon (n = 171) oder Placebo (n = 174) zugewiesen; 330 erhielten die zugewiesene Intervention und 319 wurden in
die Analyse aufgenommen (162 in der Ceftriaxon-Gruppe und 157 in der Placebo-Gruppe). In der analysierten Patientengruppe waren 153 (48 %) Frauen. 15 Patienten erhielten nach der Randomisierung nicht
die zugewiesene Intervention und 11 zogen ihre Einwilligung zurück. Die Auswertung bestätigte 93 Fälle von VAP, darunter 74 frühe Infektionen. Die Inzidenz der frühen VAP war in der Ceftriaxon-Gruppe
signifikant niedriger als in der Placebo-Gruppe (23 [14 %] gegenüber 51 [32 %], p = 0,030), wobei Ceftriaxon keine mikrobiologischen Auswirkungen und keine unerwünschten Wirkungen zuzuschreiben
waren. Interessant war insbesondere, dass in der Ceftriaxon-Gruppe auch die sekundären Endpunkte bis zum Tag 28 signifikant besser abschnitten: Es gab weniger VAP, mehr Beatmungs-freie Tage, mehr
Antibiotika-freie Tage (21 vs. 15, p < 0,0001) und auch die Mortalität war niedriger (15 % vs. 25 %).
Folgerung der Autoren
Bei Patienten mit akuten Hirnverletzungen verringerte eine einzige Ceftriaxon-Dosis das Risiko einer frühen VAP. Auf Basis der Studienergebnisse wird empfohlen, dass eine frühe Einzeldosis Ceftriaxon in die VAP-Präventions-Bündel bei Patienten mit Hirnverletzungen, die mechanisch beatmet werden müssen, aufgenommen werden sollte.
Kommentar der Herausgeber
Diese Studie unterstützt frühere kleinere Untersuchungen dahingehend, dass eine Einmaldosis von Ceftriaxon bei beatmeten Patienten mit akuter Hirnverletzung sinnvoll sein dürfte. Nicht nur war die Rate von VAP niedriger, sondern konnten mit einer Mortalitätsreduktion und einer Reduktion des Antibiotikaverbrauchs zwei entscheidende Vorteile aufgezeigt werden.
Dahyot-Fizelier C. et al. Ceftriaxone to prevent early ventilator-associated pneumonia in patients with acute brain injury: a multicentre, randomised, double-blind, placebo-controlled, assessor-masked superiority trial. Lancet Respir Med. 2024; published online first Jan 19, 2024. doi: 10.1016/S2213-2600(23)00471-X
13.03.2024
Zulassungsempfehlung für neue Cephalosporin β-Lactamase-Inhibitor-Kombination
Der Ausschuss für Humanarzneimittel (CHMP) bei der europäischen Arzneimittelbehörde EMA sprach sich in seiner Sitzung vom 25. Januar 2024 für die Zulassung des neuen Antibiotikums Exblifep® aus. Das Arzneimittel von Advanz Pharma Limited soll zur Behandlung von komplizierten Harnwegsinfektionen und nosokomialer Pneumonien bzw. damit assoziierter Bakteriämien eingesetzt werden.1
Die zunehmende Prävalenz von β-Lactamasen mit erweitertem Spektrum (ESBL) stellt eine bedeutende Herausforderung für die antimikrobielle Therapie dar. Diese Enzyme sind in der Lage, die meisten β-Lactam-Antibiotika zu hydrolysieren, einschließlich Cephalosporine der 3. und 4. Generation, und können so den vermehrten Einsatz von Reservesubstanzen wie Carbapenemen erforderlich machen. Um dieser Herausforderung zu begegnen, sind neue therapeutische Optionen erforderlich. Eine Strategie besteht darin, β-Lactame mit neuartigen β-Lactamase-Hemmern zu kombinieren, die die antibakterielle Aktivität gegen β-Lactam-resistente Erreger wiederherstellen können.2,3
Exblifep® enthält den bekannten Wirkstoff Cefepim, ein Cephalosporin der 4. Generation, das durch die Hemmung der Peptidoglykan-Zellwandsynthese bakterizid wirkt und ein breites Wirkspektrum gegen Gram-negative Erreger aufweist. Kombiniert wird Cefepim mit dem neuen Wirkstoff Enmetazobactam, welches als β-Lactamase-Inhibitor die Hydrolyse von Cefepim verhindert. Enmetazobactam (= N-Methyl-Tazobactam) ist eine strukturelle Weiterentwicklung von Tazobactam. Die Methylierung des Tazobactam-Moleküls ist mit Vorteilen hinsichtlich der Zellpenetration assoziiert, wodurch es die Wirksamkeit von Cefepim gegen ESBL der Ambler-Klasse A wiederherstellen kann. Exblifep® soll als Pulver für ein Konzentrat zur Herstellung einer Infusionslösung mit 2g Cefepim und 0,5g Enmetazobactam erhältlich sein.1-3
Das neue Antibiotikum wurde in der randomisierten, kontrollierten und doppelblinden Phase-III-Studie ALLIUM an Erwachsenen mit kompliziertem Harnwegsinfekt einschließlich Pyelonephritis einer Therapie mit Piperacillin-Tazobactam gegenübergestellt. Die 1041 eingeschlossenen Patienten wurden 1:1 randomisiert und erhielten entweder Piperacillin-Tazobactam (4,5 g i.v. alle 8 h) oder Cefepim-Enmetazobactam (2,5 g i.v. alle 8 h) über einen Zeitraum von mindestens 7 bis maximal 14 Tagen. Der primäre Endpunkt war erreicht, wenn die Patienten am 14. Tag nach Beginn der Therapie klinisch geheilt waren und die initiale Bakterienlast im Urin auf < 103 koloniebildende Einheiten/ml gesenkt werden konnte. In die Auswertung des Endpunkts gingen die Ergebnisse von 678 Patienten ein. Dabei erreichten 273 von 345 Patienten unter Cefepim-Enmetazobactam (79,1 %) und 196 von 333 Patienten (58,9 %) unter Piperacillin-Tazobactam den aus klinischer Heilung und mikrobiologischer Eradikation zusammengesetzten Endpunkt. Das neue Antibiotikum erfüllte mit einer Differenz von 21,2 Prozentpunkten (95 % Konfidenzintervall 14,3 % – 27,9 %) die Anforderungen einer Nicht-Unterlegenheit gegenüber Piperacillin-Tazobactam. Bei differenzierter Betrachtung zeigte sich an Tag 14 insbesondere eine signifikant höhere mikrobiologische Eradikationsrate unter Cefepim-Enmetazobactam (82,9 % vs. 64,9 %), während es bei den klinischen Heilungsraten aber keinen signifikanten Unterschied zwischen den Behandlungsgruppen gab (92,5 % vs. 88,9 %).3
Behandlungsbedingte Nebenwirkungen waren im Allgemeinen leicht und traten etwas häufiger unter Cefepim-Enmetazobactam auf. Das Nebenwirkungsprofil des neuen Antibiotikums umfasst am häufigsten Schmerzen und Entzündungen an der Infusionsstelle, Durchfall, Hautausschlag und Kopfschmerzen.1,3
Die Kombination von Cefepim mit dem neuen β-Lactamase-Inhibitor Enmetazobactam stellt eine vielversprechende neue Therapieoption bei Infektionen mit ESBL-Bildner dar. In der ALLIUM-Studie waren allerdings insgesamt nur 142 Patienten mit ESBL-bildenden Keimen vertreten, innerhalb derer mehr Patienten unter der neuen Kombination den primären Endpunkt erreichten als unter Piperacillin-Tazobactam. Im Rahmen einer spanischen Untersuchung wurde die Aktivität von Cefepim in Kombination mit verschiedenen neuartigen β-Lactamase-Inhibitoren gegen carbapenemaseproduzierende Enterobacterales-Isolate getestet. Durch die Hinzunahme von Enmetazobactam konnte u.a. eine Verbesserung der Aktivität gegenüber OXA-48-produzierenden Isolaten gezeigt werden, auch wenn diese im Vergleich mit anderen getesteten β-Lactamase-Inhibitoren am geringsten ausfiel.4
Es sind jedoch noch weitere Daten notwendig, um den zukünftigen Stellenwert und den potenziellen Beitrag zur Einsparung des Carbapenemeinsatzes von Cefepim-Enmetazobactam zu beurteilen. Nach der positiven Stellungnahme des CHMP ist noch die Zustimmung der EU-Kommission für die endgültige Entscheidung über das Inverkehrbringen nötig.
1 European Medicines Agency (EMA). Exblifep-summary of opinion. EMA/CHMP/15483/2024; published online Jan 25, 2024. URL: https://www.ema.europa.eu/en/documents/smop-initial/chmp-summary-positive-opinion-exblifep_en.pdf
2 Papp-Wallace K.M. et al. Beyond piperacillin-tazobactam: cefepime and AAI101 as a potent β-lactam− β-lactamase inhibitor combination. Antimicrob Agents Chemother. 2019;63(5):e00105-19. doi: 10.1128/aac.00105-19
3 Kaye K.S. et al. Effect of cefepime/enmetazobactam vs piperacillin/tazobactam on clinical cure and microbiological eradication in patients with complicated urinary tract infection or acute pyelonephritis: a randomized clinical trial. Jama. 2022;328(13):1304-14. doi: 10.1001/jama.2022.17034
4 Vázquez-Ucha J.C. et al. Assessment of Activity and Resistance Mechanisms to Cefepime in Combination with the Novel β-Lactamase Inhibitors Zidebactam, Taniborbactam, and
Enmetazobactam against a Multicenter Collection of Carbapenemase-Producing Enterobacterales. Antimicrob Agents Chemother. 2022;66(2):e0167621. doi: 10.1128/AAC.01676-21
13.03.2024
Informationen und Maßnahmen – interregionalen Verbreitung von Vancomycin-resistenten Enterococcus faecium (VRE) in der Schweiz
Am 16. Februar informiert Swissnoso im Namen des Bundesamtes für Gesundheit (BAG) und in Zusammenarbeit mit der Schweizerischen Gesellschaft für Infektiologie (SSI), der Schweizerischen Gesellschaft für Spitalhygiene (SGSH) und dem Nationalen Referenzlaboratorium zur Früherkennung und Überwachung neuartiger Antibiotikaresistenzen (NARA) über das vermehrte Auftreten und die schnelle interregionale Verbreitung von Vancomycin-resistenten Enterococcus faecium (VRE) vanA ST612 in der Schweiz.
Ein bedeutendes Merkmal dieses VRE vanA ST612 ist die verminderte Empfindlichkeit gegenüber Daptomycin, was die antibiotische Therapie bei einer Infektion beeinträchtigen kann. Bitte
beachten Sie die ausführliche Warnung des NARA vom 13. Februar 2024.
Zwischen Juli 2022 und Dezember 2023 wurden in fünf Kantonen verwandte Isolate (n = 35) identifiziert. Weitere Isolate mit VRE vanA ST612 wurden im Kanton St. Gallen entdeckt, jedoch steht der genetische Vergleich mit den Ausbruchsisolaten noch aus. Insgesamt wurden 40-50 Patienten identifiziert, hauptsächlich als Träger.
Derzeit liegen nur begrenzte epidemiologische Informationen vor, da die interregionale Verbreitung erst kürzlich erkannt wurde. Angesichts der Ausbreitung dieser eng verwandten Isolate muss davon
ausgegangen werden, dass es ein unbekanntes Reservoir gibt.
Die vorläufigen Empfehlungen von Swissnoso zum Umgang mit diesem Erreger sind folgend im Detail nachzulesen:
Zur Meldung (Stand: 16. Februar 2024)
Eine Anpassung der Empfehlungen wird fortlaufend je nach Entwicklung der epidemiologischen Lage angepasst. Bei weiteren Fragen kontaktieren Sie bitte das BAG über media@bag.admin.ch.
13.03.2024
Cycloserin und Linezolid bei Tuberkulose-Meningitis
Die Fähigkeit von Antituberkulosemedikamenten, die Blut-Hirn-Schranke zu überwinden und das zentrale Nervensystem zu erreichen, ist entscheidend für ihre Wirksamkeit bei der Behandlung von Tuberkulose-Meningitis (TBM). In einer Studie wurde versucht, eine wichtige Wissenslücke zu schließen und Daten über die Fähigkeit neuer Antituberkulosemedikamente in die Zerebrospinalflüssigkeit (CSF) einzudringen zu erheben.
Von Januar 2019 bis Januar 2020 wurde hierzu eine klinisch-pharmakologische Studie bei Patienten durchgeführt, die in Tiflis, Georgien, wegen TBM behandelt wurden. Serielle Serum- und Liquorproben
wurden während des Krankenhausaufenthalts der Patienten entnommen.
Insgesamt wurden 17 wegen TBM behandelte Patienten (8 mit bestätigter Erkrankung) eingeschlossen; alle erhielten Linezolid, ein Teil zusätzlich Cycloserin, Clofazimin, Delamanid und Bedaquilin. Alle
Liquormessungen von Bedaquilin, Clofazimin und Delamanid lagen unterhalb der Nachweisgrenze. Die medianen Liquorkonzentrationen von Cycloserin betrugen nach 2 bzw. 6 Stunden 15,90 und 15,10 µg/ml mit
einem adjustierten Liquor/Serum-Verhältnis von 0,52 und 0,66. Die Liquorkonzentrationen von Linezolid betrugen 0,90 und 3,14 µg/ml nach 2 bzw. 6 Stunden, mit einem adjustierten
Liquor/Serum-Verhältnis von 0,25 bzw. 0,59. Die Liquor-Serum-Konzentrationen von Linezolid wurden durch die gleichzeitige Verabreichung von Rifampin nicht beeinflusst.
Folgerung der Autoren
Die Studie zeigt eine geringe Liquor-Penetration von Bedaquilin, Clofazimin und Delamanid und im Gegensatz dazu eine mäßige bis hohe Liquor-Penetration von Linezolid bzw. Cycloserin. Die
Ergebnisse legen nahe, dass Linezolid und Cycloserin vielversprechende Optionen für die Behandlung von TBM sind, insbesondere bei multiresistenten Isolaten, bei denen ein erfolgreicher Ausgang die
seltene Ausnahme ist.
Kempker, R. R. et al. Cycloserine and Linezolid for Tuberculosis Meningitis: Pharmacokinetic Evidence of Potential Usefulness. Clin Infect Dis. 2022; 75(4):682-689. doi: 10.1093/cid/ciab992
14.02.2024
STIKO – Neue Meningokokken-B-Impfempfehlung für Säuglinge
Die Ständige Impfkommission (STIKO) empfiehlt nun die Impfung aller Säuglinge ab dem Alter von 2 Monaten gegen Meningokokken der Serogruppe B (MenB) mit dem Impfstoff 4CMenB (Bexsero). Trotz der Seltenheit invasiver MenB-Erkrankungen ist deren Verlauf oft schwerwiegend, besonders bei Säuglingen und Kleinkindern unter 5 Jahren, mit dem höchsten Risiko im ersten Lebensjahr. Die STIKO schlägt vor, die Impfserie frühzeitig mit drei Dosen nach dem 2+1 Schema zu beginnen: im Alter von 2, 4 und 12 Monaten, ergänzt durch Nachholimpfungen bis zum 5. Geburtstag.
Aus Praktikabilitätsgründen soll diese zusätzliche Impfung möglichst zusammen mit anderen, für diesen Zeitpunkt empfohlenen Impfungen erfolgen. Obwohl die Koadministration verschiedener Impfstoffe sicher ist, kann sie zu verstärkten Impfreaktionen wie Fieber oder Schmerzen führen. Besonders der Bexsero-Impfstoff verursacht häufig Fieber, weshalb eine prophylaktische Gabe von Paracetamol bei Kindern unter 2 Jahren empfohlen wird, um Fieber zu vermeiden. Diese Paracetamol-Prophylaxe, die zeitgleich mit der Impfung beginnen sollte, beeinträchtigt nicht die Immunantwort.
Die Einführung der MenB-Impfung als Standard für Säuglinge zielt darauf ab, die Zahl invasiver Meningokokken-Erkrankungen zu senken und schwere Erkrankungsfolgen bei Säuglingen und Kleinkindern zu verhindern. Diese Empfehlung erweitert die bisherige Indikationsimpfung für bestimmte Risikogruppen und trägt zum besseren individuellen Schutz bei.
14.02.2024
RKI – Aufruf zum Melden von Ralstonia pickettii
In Deutschland wurde seit September 2023 eine Zunahme von Ralstonia pickettii-Nachweisen beobachtet, die mit einem nosokomialen Ausbruch in Australien in Verbindung steht. Die Weltgesundheitsorganisation informierte am 12. Dezember 2023 über diesen Ausbruch. R. pickettii, ein Gram-negatives, opportunistisch pathogenes Bakterium, kann vor allem bei Immunsupprimierten und Menschen mit Zystischer Fibrose Infektionen auslösen. Kontaminierte Kochsalzlösungen wurden als Infektionsquelle identifiziert. In Australien wurden über 40 Fälle gemeldet, zurückgeführt auf Kochsalzlösung eines indischen Herstellers, was zu einem Rückruf und Auslieferungsstopp führte. Die Produkte dieses Herstellers sind auch in der EU erhältlich.
Die Antibiotika-Resistenz-Surveillance (ARS) registrierte 2023 in Deutschland 20 Fälle von R. pickettii, mit einem deutlichen Anstieg der Nachweise in Blutkulturen von September bis November. Erste Analysen zeigen geringfügige genetische Unterschiede zwischen den deutschen Isolaten und dem australischen Ausbruchsstamm. Eine direkte Verbindung zu den kontaminierten Produkten wurde bisher nicht festgestellt. Die Ermittlungen zu weiteren Fällen und potenzieller Produktkontamination laufen.
Es wird gebeten, alle R. pickettii-Nachweise an das zuständige Gesundheitsamt zu melden. Alle R. pickettii-Isolate mit Probenentnahme seit August 2023 sollten zunächst bis einschließlich 31.3.2024 zur Typisierung an das Konsiliarlabor für Mukoviszidose-Bakteriologie am Universitätsklinikum Frankfurt am Main gesendet werden.
14.02.2024
Hochdosierter dual-antibiotisch beladener Zement für Hüft-Prothesen
Hüftfrakturen sind die häufigsten Frakturen, die im Krankenhaus behandelt werden müssen. Die Verwendung von Antibiotika-beladenem Knochenzement bei Hüftfrakturen, die mit einer Hemiarthroplastik behandelt werden, ist umstritten. In der nachfolgenden Studie war das Ziel, die Rate der tiefen postoperativen Infektionen bei Patienten zu vergleichen, die einen hochdosierten, mit zwei Antibiotika beladenen Zement im Vergleich zu Standardzement mit nur einem einzigen Antibiotikum erhielten.
In dieser randomisierten Studie wurden Personen im Alter von mindestens 60 Jahren mit einer Hüftfraktur untersucht, die in 26 britischen Krankenhäusern behandelt wurden. Die Patienten, die sich einer
zementierten Hemiarthroplastik unterzogen, wurden nach dem Zufallsprinzip im Verhältnis 1:1 entweder einem Standardzement (Heraeus Palacos R+G Zement mit 0,5 g Gentamicin pro 40 g mix Zement,) oder
einem hochdosierten, mit zwei Antibiotika beladenen Zement (Heraeus Copal G+C Zement mit 1 g Gentamicin und 1 g Clindamycin pro 40 g mix Zement) zugewiesen. Sowohl die Patienten als auch die Prüfer
waren hinsichtlich der Behandlungsgruppe maskiert. Der primäre Endpunkt war eine tiefe postoperative Infektion innerhalb von 90 Tagen nach Randomisierung gemäß der Definition der US-Centers for
Disease Control and Prevention in einer randomisierten Population. Sekundäre Endpunkte waren Lebensqualität, Sterblichkeit, Antibiotikaverbrauch, Mobilität und Aufenthaltsstatus am Tag 120.
Zwischen August 2018 und August 2021 wurden 4936 Patienten nach dem Zufallsprinzip entweder der Standardversorgung mit einem mit Antibiotika beladenen Zement (2453 Patienten) oder einem hochdosierten, mit zwei Antibiotika beladenen Zement (2483 Patienten) zugewiesen. 38 (1,7 %) von 2183 Patienten mit Follow-up-Daten in der Gruppe mit einfach antibiotisch belastetem Zement hatten bis 90 Tage nach der Randomisierung eine tiefe Infektion der Operationsstelle, ebenso wie 27 (1,2 %) von 2214 Patienten in der Gruppe mit hochdosiertem dual antibiotisch belastetem Zement. Auch bei den sekundären Endpunkten gab es keinen Vorteil für den Dualantibiotika-beladenen Hochdosiszement.
Folgerung der Autoren
In dieser Studie führte die Verwendung von hochdosiertem, mit einem dualen Antibiotikum beladenen Zement nicht zu einer Verringerung der Rate tiefer postoperativer Infektionen bei Patienten im Alter von 60 Jahren oder älter, die eine Hemiarthroplastik nach einer intrakapsulären Hüftfraktur erhielten.
Kommentar der Herausgeber
Die ist die größte randomisierte Studie zu dieser Fragestellung, die den bisher aus Observationsstudien vermuteten Vorteil des Dualantibiotika-beladenen Hochdosiszements nicht bestätigen kann. Die Power dieser Studie war mit 90 % sehr hoch. Es gab auch keine Unterschiede in den sekundären Endpunkten Mobilität, Mortalität und Lebensqualität. Ob Clindamycin der beste Kombinationspartner in dieser Indikation war, ist allerdings fraglich.
Agni, N. R. et al. High-dose dual-antibiotic loaded cement for hip hemiarthroplasty in the UK (WHiTE 8): a randomised controlled trial. Lancet. 2023; 402(10397):196-202.
doi: 10.1016/S0140-6736(23)00962-5
17.01.2024
OPS-Codes für Reserveantibiotika
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) hat kürzlich die finale Version der OPS-Codes 2024 (Operationen- und Prozedurenschlüssel) veröffentlicht.
Laut dem BfArM wurden in die aktuelle Ausgabe 160 Anregungen von Kliniken, Krankenkassen, medizinischen Fachgesellschaften sowie vielen weiteren Organisationen im Gesundheitsweisen integriert, unter anderem auch für die Applikation von Reserveantibiotika (6-00g ff.)
Eine Übersicht über die Applikation von Medikamenten, unter anderem von Reserveantibiotika, finden Sie hier.
17.01.2024
►COVID-19 Kompendium (4., erw. u. akt. Auflage)
►COVID-19 Erkrankungen weltweit
Website der Johns Hopkins University
►COVID-19 Erkrankungen in Deutschland (Landkreise)